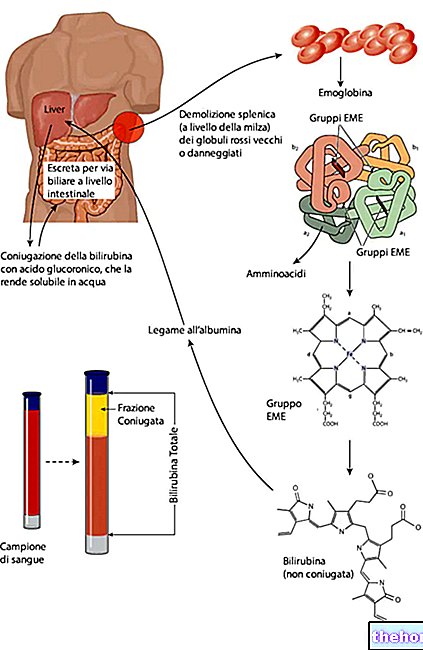
Aktive ingredienser: Tacrolimus (Tacrolimus monohydrat)
Protopic 0,03% salve
Protopic pakningsindsatser fås til pakningsstørrelser:- Protopic 0,03% salve
- Protopic 0,1% salve
Indikationer Hvorfor bruges Protopic? Hvad er det for?
Det aktive stof i Protopic, tacrolimus monohydrat, er et immunmodulerende middel.
Protopic 0,03% salve er indiceret til behandling af moderat til svær atopisk dermatitis (eksem) hos voksne, der ikke reagerer tilstrækkeligt, eller som er intolerante over for konventionelle behandlinger såsom topiske kortikosteroider og hos børn (2 år og ældre), som de ikke reagerede på tilstrækkeligt til konventionelle behandlinger såsom topiske kortikosteroider.
Hvis moderat til svær atopisk dermatitis er forsvundet eller næsten forsvundet efter behandling af eksacerbationer i op til 6 uger, og hvis der opstår hyppige eksacerbationer (4 eller flere om året), kan de forebygges eller forlænges. De forekommer ikke ved brug af Protopic 0,03% salve to gange om ugen.
Ved atopisk dermatitis er der en overreaktion af hudens immunsystem, der forårsager hudbetændelse (kløe, rødme, tørhed). Protopic modificerer det unormale immunrespons og lindrer hudbetændelse og kløe.
Kontraindikationer Når Protopic ikke bør bruges
Brug ikke Protopic
- Hvis du er allergisk (overfølsom) over for tacrolimus eller et af de øvrige indholdsstoffer i Protopic eller over for makrolidantibiotika (dvs. azithromycin, clarithromycin, erythromycin).
Forholdsregler ved brug Hvad du skal vide, før du tager Protopic
Fortæl det til din læge
- hvis du har "leversvigt.
- hvis du har hudsygdomme (neoplasi), eller hvis du har et svækket (immunkompromitteret) immunsystem, uanset årsagen.
- hvis du har en medfødt hudsygdom som Nethertons syndrom, lamellær ichthyosis (udbredt afskalning af huden forårsaget af fortykkelse af det ydre hudlag) eller hvis du lider af generaliseret erythroderma (rødme ved betændelse og afskalning af hele huden).
- hvis du oplever kutan Graft Versus Host Disease (en hudimmunreaktion, som er en almindelig komplikation hos knoglemarvstransplantationspatienter).
- hvis du har hævede lymfeknuder i starten af behandlingen.Hvis dine lymfeknuder hæver under behandling med Protopic, skal du kontakte din læge.
- hvis du har inficerede læsioner. Påfør ikke salven på inficerede læsioner.
- Fortæl det til din læge, hvis du bemærker nogen ændring i hudens udseende.
- Sikkerheden ved at bruge Protopic over en længere periode er ukendt. Et meget begrænset antal mennesker, der har brugt Protopic salve, har haft maligniteter (f.eks. Hud eller lymfomer). Der er imidlertid ikke vist en sammenhæng med Protopic salvebehandling.
- Undgå at udsætte din hud i lange perioder for sollys eller kunstigt lys, f.eks. Et solarium. Hvis du tilbringer tid udendørs efter påføring af Protopic, skal du bruge en solcreme og bære behageligt tøj, der beskytter din hud mod solen. Kontakt også din læge for anden passende metoder til solbeskyttelse. Hvis du har fået ordineret helioterapi, skal du fortælle det til din læge, at du bruger Protopic, og at det ikke anbefales at bruge Protopic og solterapi på samme tid.
- Hvis din læge ordinerer Protopic til dig to gange om ugen for at undgå en ny debut af din atopisk dermatitis, skal din tilstand revurderes af din læge mindst hver 12. måned, selvom sygdommen er under kontrol. Hos børn skal vedligeholdelsesbehandlingen stoppes efter 12 måneder for at kontrollere, om der stadig er behov for fortsat behandling.
Børn
- Protopic salve er ikke godkendt til brug til børn under 2 år. Den bør derfor ikke bruges i denne aldersgruppe. Kontakt din læge.
- Effekten af Protopic behandling på udviklingen af immunsystemet hos børn, især unge, er ikke fastslået.
Interaktioner Hvilke lægemidler eller fødevarer kan ændre virkningen af Protopic
Fortæl det til din læge eller på apoteket, hvis du tager anden medicin eller har brugt det for nylig, også uden recept.
Du kan bruge fugtgivende cremer og lotioner under Protopic behandling, men de kan kun påføres det samme behandlede område to timer før eller to timer efter Protopic påføring.
Effekten af samtidig brug af Protopic med andre præparater, der skal påføres huden eller ved indtagelse af orale kortikosteroider (f.eks. Kortison) eller medicin, der påvirker immunsystemet, er ikke undersøgt.
Protopic med alkoholholdige drikkevarer
Når du bruger Protopic, kan drikke alkoholiske drikke forårsage skylning af ansigt eller hud og fornemmelser af varme
Advarsler Det er vigtigt at vide, at:
Graviditet og amning
Brug ikke Protopic, hvis du er gravid eller ammer.
Spørg din læge eller apotek til råds, før du tager medicin
Dosis, metode og administrationstidspunkt Sådan bruges Protopic: Dosering
Brug altid Protopic nøjagtigt som din læge har fortalt dig. Hvis du er i tvivl, skal du kontakte din læge eller apotek.
- Påfør et tyndt lag Protopic på de berørte områder af huden.
- Protopic kan påføres det meste af kropsoverfladen, herunder ansigt, hals og områder, der udsættes for bøjning af albuer og knæ.
- Undgå at bruge salven i din næse, mund eller øjne. Hvis salven ved et uheld påføres disse områder, skal området renses helt og / eller skylles med vand.
- Dæk ikke det berørte hudområde med bandager eller forbindinger.
- Vask dine hænder efter påføring af Protopic, medmindre dine hænder også er inden for det område, der skal behandles.
- Inden Protopic påføres efter et bad eller et brusebad, skal du sørge for, at din hud er helt tør.
Anvendelse til børn (2 år og ældre)
Påfør Protopic 0,03% salve to gange om dagen i tre uger, en gang om morgenen og en gang om aftenen. Derefter skal salven bruges en gang dagligt på hvert berørt hudområde, indtil eksemet er helet.
Voksne (16 år og derover)
To styrker af Protopic (Protopic 0,03% og Protopic 0,1% salve) er tilgængelige for voksne patienter (16 år og ældre). Din læge vil beslutte, hvilken dosis der er bedst for dig.
Generelt begynder behandlingen med Protopic 0,1% to gange om dagen, en gang om morgenen og en gang om aftenen, indtil eksemet er forsvundet.Baseret på eksemets svar vil lægen afgøre, om hyppigheden af applikationer vil blive reduceret, eller hvis den lavere styrke (Protopic 0,03%) kan bruges.
Behandl berørte hudområder, indtil eksemet heler. Generelt ser du forbedring inden for en uge. Spørg din læge om andre former for behandling, hvis du ikke kan se nogen synlig forbedring efter to uger.
Din læge kan ordinere dig til at bruge Protopic salve to gange om ugen, efter at din atopisk dermatitis er forsvundet eller næsten er forsvundet (Protopic 0,03% til børn og Protopic 0,1% til voksne). Protopic salve skal påføres en gang om dagen, to gange om ugen (f.eks. , Mandag og torsdag) på de områder af din krop, der normalt påvirkes af atopisk dermatitis, 2-3 dage bør gå mellem applikationer uden Protopic-behandling.
Hvis symptomerne dukker op igen, skal du vende tilbage til at bruge Protopic to gange om dagen som beskrevet ovenfor og aftale en tid med din læge for at kontrollere din behandling.
Overdosering Hvad skal jeg gøre, hvis du har taget for meget Protopic
Hvis du ved et uheld sluger salven
Hvis du ved et uheld sluger salven, skal du kontakte din læge eller apotek så hurtigt som muligt. Forsøg ikke at fremkalde opkastning.
Hvis du har glemt at bruge Protopic
Hvis du glemmer at smøre salven på det planlagte tidspunkt, skal du anvende den, så snart du husker det, og derefter fortsætte som foreskrevet. Spørg din læge eller apoteket, hvis du har yderligere spørgsmål om brugen af Protopic.
Bivirkninger Hvad er bivirkningerne af Protopic
Som al anden medicin kan Protopic forårsage bivirkninger, men ikke alle får bivirkninger.
Meget almindelig (kan forekomme hos mere end 1 ud af 10 personer):
- Fornemmelse af forbrænding og kløe
Disse symptomer er normalt milde til moderate og forsvinder generelt inden for en uge efter start af behandling med Protopic.
Almindelig (kan forekomme hos op til 1 ud af 10 personer):
- Rødme
- Følelse af varme
- Smerte
- Øget hudfølsomhed (især ved varme og kulde)
- Hud prikken
- Udslæt Lokal hudinfektion uanset specifikke årsager, herunder men ikke begrænset til: betændte eller inficerede hårsække, forkølelsessår, generaliserede herpes simplex -infektioner)
- Ansigtsrødme eller hudirritation efter indtagelse af alkoholholdige drikkevarer er også almindelige reaktioner
Ikke almindelig (kan forekomme hos færre end 1 ud af 100 personer):
- Acne
Der er rapporteret om infektioner på applikationsstedet hos børn og voksne efter behandling to gange ugentligt. Impetigo, en overfladisk bakteriel hudinfektion, der normalt forårsager blærer eller sår på huden, er blevet rapporteret hos børn.
Rosacea (rødme i ansigtet), pseudo-rosacea dermatitis og ødem på applikationsstedet er blevet rapporteret i perioden efter markedsføringen.
Siden dets tilgængelighed på markedet har et meget lille antal mennesker, der har brugt Protopic salve, haft maligne tumorer (f.eks. Lymfomer, herunder hudlymfomer eller andre hudkræftformer). Imidlertid er der ikke påvist eller udelukket en sammenhæng med Protopic salvebehandling baseret på de foreliggende data til dato.
Indberetning af bivirkninger
Tal med din læge eller apotek, hvis du får bivirkninger, herunder mulige bivirkninger, som ikke er nævnt i denne indlægsseddel. Du kan også indberette bivirkninger direkte via det nationale rapporteringssystem anført i tillæg V. Ved at rapportere bivirkninger kan du hjælpe med at give mere information om sikkerheden ved dette lægemiddel.
Udløb og opbevaring
Opbevar Protopic utilgængeligt for børn.
Brug ikke Protopic efter den udløbsdato, der står på tuben og kartonen efter EXP. Udløbsdatoen refererer til den sidste dag i måneden.
Må ikke opbevares ved temperaturer over 25ºC.
Lægemidler må ikke bortskaffes via spildevand eller husholdningsaffald. Spørg din apotek om, hvordan du skal smide medicin, du ikke længere bruger. Dette vil hjælpe med at beskytte miljøet.
Hvad indeholder Protopic
- Den aktive ingrediens er tacrolimus monohydrat. Et gram Protopic 0,03% salve indeholder 0,3 mg tacrolimus (som tacrolimus monohydrat).
- Øvrige indholdsstoffer er hvid vaselin, flydende paraffin, propylencarbonat, hvid bivoks og fast paraffin.
Hvordan Protopic ser ud og pakningens indhold
Protopic er en hvid, let gullig salve. Den fås i rør med 10, 30 eller 60 gram salve. Ikke alle pakningsstørrelser er nødvendigvis markedsført. Protopic fås i to styrker (Protopic 0,03% og Protopic 0,1% salve).
Indlægsseddel: AIFA (Italian Medicines Agency). Indhold offentliggjort i januar 2016. De foreliggende oplysninger er muligvis ikke opdaterede.
For at få adgang til den mest opdaterede version er det tilrådeligt at få adgang til webstedet AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttige oplysninger.
01.0 LÆGEMIDLETS NAVN
PROTOPISK 0,03% OLIE
02.0 KVALITATIV OG KVANTITATIV SAMMENSÆTNING
1 g Protopic 0,03% salve indeholder 0,3 mg tacrolimus som tacrolimus monohydrat (0,03%).
Den fulde liste over hjælpestoffer findes i afsnit 6.1.
03.0 LÆGEMIDDELFORM
Salve.
Hvid til let gul salve.
04.0 KLINISKE OPLYSNINGER
04.1 Terapeutiske indikationer
Protopic 0,03% salve er indiceret til voksne, unge og børn fra 2 år.
Behandling af eksacerbationer
Voksne og unge (16 år og derover)
Behandling af moderat til svær atopisk dermatitis hos voksne, der ikke reagerer tilstrækkeligt, eller som er intolerante over for konventionelle behandlinger såsom topiske kortikosteroider.
Pædiatrisk population (2 år og ældre)
Behandling af moderat til svær atopisk dermatitis hos børn, der ikke har reageret på konventionelle behandlinger såsom topiske kortikosteroider.
Vedligeholdelsesbehandling
Behandling af moderat til svær atopisk dermatitis til forebyggelse af eksacerbationer og til forlængelse af eksacerbationsfrie intervaller hos patienter med meget hyppige eksacerbationer (4 eller flere gange om året), der har oplevet en indledende respons på behandling, der varer maksimalt 6 uger med tacrolimus salve to gange dagligt (læsioner forsvandt, næsten forsvandt eller forekommer i en mild form).
04.2 Dosering og indgivelsesmåde
Protopisk behandling bør initieres af læger med erfaring i diagnosticering og behandling af atopisk dermatitis.
Protopic fås i to styrker, Protopic 0,03% og Protopic 0,1% salve.
Dosering
Behandling af eksacerbationer
Protopic kan bruges til kortvarig behandling og til intermitterende langtidsbehandling. Langsigtet behandling behøver ikke at være kontinuerlig.
Protopisk behandling skal begynde ved det første tegn og symptomer. Hvert berørt hudområde bør behandles med Protopic, indtil læsionerne er forsvundet, næsten er forsvundet eller kun er til stede lidt. Derefter betragtes patienter som berettigede til vedligeholdelsesbehandling (se nedenfor). Ved de første tegn på bedring (forværring) af symptomer på sygdommen bør behandlingen genoprettes.
Anvendelse til voksne og unge (16 år og derover)
Behandlingen skal starte med Protopic 0,1% to gange dagligt og skal fortsætte, indtil læsionen er væk. Hvis symptomerne opstår igen, skal behandlingen med Protopic 0,1% genstartes to gange dagligt. Hvis kliniske forhold tillader det, bør der forsøges at reducere hyppigheden af applikationer eller at bruge den lavere styrke, Protopic 0,03% salve.
Forbedring ses normalt inden for en uge efter behandlingsstart. Hvis der ikke ses tegn på forbedring efter to ugers behandling, bør andre behandlingsmuligheder overvejes.
Ældre befolkning
Der er ikke udført specifikke undersøgelser hos den ældre befolkning. Den kliniske erfaring, der var tilgængelig for denne gruppe af patienter, indikerede imidlertid ikke behov for dosisjustering.
Pædiatrisk population
Børn (2 år og ældre) bør bruge den laveste koncentration: Protopic 0,03% salve.
Behandlingen skal starte to gange om dagen i op til tre uger.
Derefter bør hyppigheden af applikationer reduceres til en gang dagligt, indtil læsionen forsvinder (se pkt. 4.4).
Protopic salve bør ikke bruges til børn under 2 år, før der foreligger yderligere data.
Vedligeholdelsesbehandling
Patienter, der reagerer i op til 6 ugers behandling med tacrolimus salve to gange dagligt (læsioner forsvandt, næsten forsvandt eller findes i en mild form) er berettiget til vedligeholdelsesbehandling.
Voksne og unge (16 år og derover)
Voksne patienter bør bruge Protopic 0,1% salve.
Protopic salve skal påføres en gang om dagen to gange om ugen (f.eks. Mandag og torsdag) på de områder, der normalt er ramt af atopisk dermatitis for at forhindre opblussen.
Mellem applikationer bør der gå 2-3 dage uden Protopic behandling.
Efter 12 måneders behandling bør lægen revurdere patientens tilstand for at beslutte, om vedligeholdelsesbehandling skal fortsætte, hvis der ikke foreligger data om sikkerheden ved vedligeholdelsesbehandling ud over 12 måneder.
Hvis tegn på forværring gentager sig, skal behandlingen genoptages to gange dagligt (se tidligere afsnit om behandling af eksacerbationer).
Ældre befolkning
Der er ikke udført specifikke undersøgelser hos den ældre befolkning (se tidligere afsnit om behandling af eksacerbationer).
Pædiatrisk population
Børn (2 år og ældre) bør bruge den laveste koncentration: Protopic 0,03% salve.
Protopic salve skal påføres en gang om dagen to gange om ugen (f.eks. Mandag og torsdag) på de områder, der normalt er ramt af atopisk dermatitis for at forhindre progression til opblussen. Mellem applikationer bør der gå 2-3 dage uden Protopic behandling.
Vurdering af barnets tilstand efter 12 måneders behandling bør omfatte afbrydelse af behandlingen for at fastslå behovet for at fortsætte denne behandling og for at vurdere sygdomsforløbet.
Protopic salve bør ikke bruges til børn under 2 år, før der foreligger yderligere data.
Indgivelsesmåde
Et tyndt lag Protopic salve skal påføres berørte eller normalt berørte områder af huden.
Protopic salve kan påføres alle dele af kroppen, inklusive ansigt, hals og områder, der er udsat for bøjning, med undtagelse af slimhinderne. Protopic salve bør ikke påføres med okklusive forbindinger, da der ikke er udført undersøgelser af denne indgivelsesmåde (se pkt. 4.4).
04.3 Kontraindikationer
Overfølsomhed over for det aktive stof, over for makrolider generelt eller over for et eller flere af hjælpestofferne anført i pkt.6.1.
04.4 Særlige advarsler og passende forholdsregler ved brug
Under brug af Protopic salve bør overdreven eksponering af huden for sollys reduceres, og brugen af ultraviolet (UV) lys udsendt af solarium og UVB- eller UVA -terapi i kombination med psoralener (PUVA) bør undgås (se afsnit 5.3) lægen bør rådgive patienten om en passende solbeskyttelsesmetode, såsom at minimere solens eksponeringstid, bruge et produkt med solcreme og dække huden med passende tøj. Protopic salve bør ikke påføres læsioner, der betragtes som potentielt ondartede eller præ-maligne.
Udviklingen inden for det behandlede område af andre ændringer end eksisterende eksem bør revideres af lægen.
Anvendelse af tacrolimus salve anbefales ikke til patienter med hudbarrierefejl såsom Nethertons syndrom, lamellær ichthyosis, generaliseret erythroderma eller transplantat versus værtsygdom. Disse hudsygdomme kan øge den systemiske absorption af tacrolimus. Oral administration af tacrolimus til behandling af disse hudsygdomme anbefales heller ikke. Der har været rapporter om øgede niveauer af tacrolimus i nærvær af ovennævnte tilstande efter markedsføringen. ...
Der skal udvises forsigtighed, hvis Protopic anvendes til patienter med omfattende hudinddragelse over en længere periode, især hos børn (se pkt.4.2). Patienter, især pædiatriske patienter, bør løbende revurderes under behandling med Protopic for at vurdere reaktionen på behandlingen, og om det er nødvendigt at fortsætte behandlingen.
Hos pædiatriske patienter bør denne revurdering efter 12 måneder omfatte afbrydelse af Protopic -behandlingen (se pkt.4.2).
Potentialet for lokal immunsuppression (resulterende i hudinfektioner eller kræftformer) er ikke kendt på lang sigt (dvs. over en årrække) (se pkt.5.1).
Protopic indeholder det aktive stof tacrolimus, en calcineurinhæmmer. Hos transplanterede patienter har langvarig systemisk eksponering for intens immunosuppression efter systemisk administration af calcineurinhæmmere været forbundet med en øget risiko for at udvikle lymfomer og hudmaligniteter. Tilfælde af maligniteter, herunder kutane neoplasmer (f.eks. Kutane T-cellelymfomer) og andre typer lymfomer og hudkarcinomer er blevet rapporteret hos patienter, der bruger tacrolimus salve (se pkt.4.8). Protopic bør ikke anvendes til patienter med medfødt eller erhvervet immundefekt eller til patienter, der gennemgår behandlinger, der forårsager immunsuppression.
Patop behandlede patienter med atopisk dermatitis viste ingen signifikante systemiske koncentrationer af tacrolimus.
Lymfadenopatier rapporteret i kliniske forsøg var ualmindelige (0,8%). De fleste af disse tilfælde var relateret til infektioner (hud, luftveje, tænder) og blev løst med "passende antibiotikabehandling.Transplantationspatienter behandlet med immunsuppressiv behandling (f.eks. Systemisk tacrolimus) har en øget risiko for at udvikle lymfomer; derfor bør patienter, der modtager Protopic, som udvikler lymfadenopati, overvåges for at sikre, at lymfadenopati forsvinder. Lymfadenopati til stede på tidspunktet for behandlingens start bør evalueres og overvåges. I tilfælde af vedvarende lymfadenopati bør ætiologien undersøges. I mangel af en klar ætiologi for lymfadenopati eller ved tilstedeværelse af akut infektiøs mononukleose, bør seponering af Protopic overvejes.
Effekten af Protopic salvebehandling på immunsystemet udvikling af børn under 2 år er ikke fastslået (se afsnit 4.1).
Protopic salve er ikke blevet evalueret for sin sikkerhed og effekt ved behandling af inficeret atopisk dermatitis. Inden behandlingen påbegyndes med Protopic salve, skal de inficerede områder behandles. Patienter med atopisk dermatitis er disponeret for overfladiske hudinfektioner. Behandling med Protopic kan være forbundet med en øget risiko for folliculitis og herpesvirale infektioner (herpes simplex dermatitis [eczema herpeticus], herpes simplex [forkølelsessår], Kaposis varicelliforme udslæt) (se pkt. 4.8). I nærvær af disse infektioner skal vægten af risiko og fordel forbundet med brug af Protopic afvejes.
Blødgøringsmidler kan ikke påføres det samme område i de 2 timer før eller efter påføring af Protopic salve. Samtidig brug af andre topiske præparater er ikke undersøgt. Der er ingen erfaring med samtidig brug af systemiske steroider eller immunsuppressive midler.
Kontakt med øjne og slimhinder bør undgås. Hvis det ved et uheld påføres disse områder, skal området rengøres omhyggeligt og / eller skylles med vand.
Anvendelse af Protopic salve til patienter med okklusive forbindinger er ikke undersøgt Brug af okklusive forbindinger anbefales ikke.
Som med alle aktuelle lægemidler skal patienterne vaske deres hænder efter påføring, medmindre hænderne også er inden for det område, der skal behandles.
Tacrolimus metaboliseres i vid udstrækning i leveren, og selvom blodkoncentrationer efter lokal behandling er lave, skal salven anvendes med forsigtighed til patienter med nedsat leverfunktion (se pkt. 5.2).
04.5 Interaktioner med andre lægemidler og andre former for interaktion
Der er ikke udført topiske lægemiddelinteraktionsundersøgelser med tacrolimus salve.
Tacrolimus metaboliseres ikke i menneskelig hud; dette indikerer, at der ikke er potentielle perkutane interaktioner, som kan påvirke metabolismen af selve tacrolimus.
Tacrolimus metaboliseres, når det er systemisk tilgængeligt, af hepatisk cytochrom P450 3A4 (CYP3A4). Systemisk eksponering efter topisk anvendelse af tacrolimus salve er lav (erythromycin, itraconazol, ketoconazol og diltiazem) hos patienter med udbredt sygdom og / eller erythrodermal sygdom bør gøres med forsigtighed.
Pædiatrisk population
Der blev udført en interaktionsundersøgelse med proteinkonjugatvaccinen mod undergruppe C i Neisseria meningitidishos børn i alderen 2 til 11 år. Der var ingen effekt på den umiddelbare reaktion på vaccinen, på dannelsen af immunhukommelse eller på cellemedieret og humoristisk immunitet (se pkt.5.1).
04.6 Graviditet og amning
Fertilitet
Der er ingen tilgængelige data om fertilitet.
Graviditet
Der er ikke tilstrækkelige data om brugen af tacrolimus salve til gravide Dyrestudier har vist reproduktionstoksicitet efter systemisk administration (se pkt. 5.3) Den potentielle risiko for mennesker er ukendt.
Protopic salve bør ikke bruges under graviditet, medmindre det er absolut nødvendigt.
Fodringstid
Menneskelige data indikerer, at tacrolimus efter systemisk administration udskilles i modermælk Selvom kliniske data har vist, at systemisk eksponering på grund af påføring af tacrolimus salve er minimal, anbefales amning ikke. Behandlingsperiode med Protopic salve.
04.7 Virkninger på evnen til at føre motorkøretøj og betjene maskiner
Protopic salve har ingen eller ubetydelig indflydelse på evnen til at føre motorkøretøj eller betjene maskiner.
04.8 Bivirkninger
Under kliniske undersøgelser oplevede cirka 50% af patienterne en eller anden form for hudirritation i applikationsområdet som en bivirkning. Brændende og kløende fornemmelser er meget almindelige, normalt milde til moderate i sværhedsgrad og med en tendens til at forsvinde inden for en uge efter behandlingsstart.En anden almindelig bivirkning af hudirritation er erytem. , fornemmelse af varme, smerter, paræstesi og udslæt Almindelig er "intolerance over for" alkohol (ansigtsrødme eller hudirritation efter indtagelse af alkoholholdige drikkevarer).
Risikoen for follikulitis, acne og herpesvirale infektioner kan øges.
Bivirkninger, der mistænkes for at være relateret til behandling, er anført nedenfor og kategoriseret efter organ- og systemklassificering. Frekvenser defineres som meget almindelige (≥1 / 10), almindelige (≥1 / 100,
* Bivirkninger blev rapporteret under postmarketingovervågning.
Eftermarkedsføring
Tilfælde af maligniteter, herunder kutane former (f.eks. Kutane T-cellelymfomer) og andre typer lymfomer og hudkarcinomer, er blevet rapporteret hos patienter, der bruger tacrolimus salve (se pkt.4.4).
Vedligeholdelsesbehandling
I en vedligeholdelsesbehandlingsundersøgelse (to gange ugentligt) hos voksne og børn med moderat og svær atopisk dermatitis viste det sig, at følgende bivirkninger forekom hyppigere end i kontrolgruppen: impetigo på applikationsstedet (7, 7% hos børn) og anvendelse infektioner på stedet (6,4% hos børn og 6,3% hos voksne).
Pædiatrisk population
Hyppigheden, typen og sværhedsgraden af bivirkninger hos børn svarer til dem, der er rapporteret for voksne.
Indberetning af formodede bivirkninger
Rapportering af formodede bivirkninger, der opstår efter godkendelse af lægemidlet, er vigtig, da det muliggør kontinuerlig overvågning af lægemidlets fordel / risiko -balance.Professionelle sundhedspersoner anmodes om at rapportere alle formodede bivirkninger via det nationale rapporteringssystem. I "bilag V .
04.9 Overdosering
Overdosering i topisk anvendelse er usandsynligt.
Ved indtagelse kan det være nødvendigt med generelle understøttende foranstaltninger, herunder overvågning af vitale tegn og observation af klinisk status.På grund af salvebærerens art anbefales det ikke at fremkalde opkastning og gastrisk skylning.
05.0 FARMAKOLOGISKE EGENSKABER
05.1 Farmakodynamiske egenskaber
Farmakoterapeutisk klassifikation: andre dermatologiske midler. ATC -kode: D11AH01.
Virkningsmekanisme og farmakodynamisk virkning
Tacrolimus virkningsmekanisme ved atopisk dermatitis er ikke fuldt ud forstået. Mens følgende virkningsmekanismer er blevet observeret, er deres kliniske betydning ved atopisk dermatitis ikke kendt.
Gennem sin binding til et specifikt cytoplasmatisk immunophyllin (FKBP12) hæmmer tacrolimus de calciumafhængige signalveje i T-lymfocytter og forhindrer dermed transkription og syntese af IL-2, IL-3, IL-4, IL-5 og andre cytokiner, f.eks. som GM-CSF, TNF-a og IFN-y.
In vitro, i Langerhans -celler isoleret fra sund hud, reducerer tacrolimus stimulerende aktivitet mod T -celler. Tacrolimus har vist sig at hæmme frigivelsen af inflammatoriske mediatorer fra kutane mastceller, basofiler og eosinofiler.
Hos dyr undertrykte tacrolimus salve inflammatoriske reaktioner i eksperimentelle og spontane dermatitis modeller, der ligner human atopisk dermatitis. Tacrolimus salve reducerede ikke hudtykkelsen og forårsagede ikke hudatrofi hos dyr.
Hos patienter med atopisk dermatitis er forbedringen af hudlæsioner under behandling med tacrolimus salve forbundet med en reduceret ekspression af Fc -receptorer på Langerhans -celler og en reduktion i deres hyperstimulerende aktivitet over for T -celler. Tacrolimus salve har ingen effekt på syntesen af kollagen. hos mand.
Klinisk effekt og sikkerhed
Protopic er blevet evalueret for effektivitet og sikkerhed hos mere end 18.500 patienter, der blev behandlet med tacrolimus salve i fase I til III kliniske undersøgelser. Data fra de seks hovedkliniske undersøgelser er præsenteret nedenfor.
I et randomiseret, dobbeltblindet, 6-måneders studie blev tacrolimus salve 0,1% påført to gange dagligt til voksne med moderat til svær atopisk dermatitis og sammenlignet med en topisk kortikosteroidbaseret behandling (0,1% hydrokortisonbutyrat på bagagerum og lemmer, 1% hydrokortisonacetat på ansigt og hals). Det primære endepunkt var graden af respons efter tre måneder, defineret som procentdelen af patienter, der havde en forbedring på mindst 60% i mEASI (modificeret indeks for eksemets sværhedsgrad og område) i måned 3 fra baseline. Responsgraden i 0,1%tacrolimus -gruppen (71,6%) var signifikant større end i den topiske kortikosteroidgruppe (50,8%; p
Tabel 1 Effekt efter 3 måneder
§ behandling med topisk kortikosteroid = 0,1% hydrokortisonbutyrat på bagagerummet og ekstremiteter, 1% hydrokortisonacetat i ansigt og hals
§ § højere værdier = større forbedring
Forekomsten og arten af de fleste bivirkninger var ens i de to behandlingsgrupper: Forbrænding af huden, herpes simplex, alkoholintolerance (rødme i ansigtet eller hudirritation efter at have drukket alkohol), prikkende fornemmelse, hyperæstesi, acne og svampedermitis forekom hyppigere i tacrolimus -gruppen. Der var ingen klinisk relevante ændringer i laboratorieværdier eller vitale tegn i nogen behandlingsgruppe i løbet af undersøgelsen.
I den anden undersøgelse blev børn i alderen 2-15 år med moderat til svær atopisk dermatitis behandlet to gange dagligt i tre uger med 0,03% tacrolimus salve, 0,1% tacrolimus salve eller hydrokortisonacetatsalve. 1%. Det primære endepunkt i hele undersøgelsen var den gennemsnitlige AUC (område under kurven) som en procentdel af mEASI -scoren fra baseline. Resultaterne af denne multicenter, dobbeltblindede, randomiserede undersøgelse viste, at tacrolimus salve 0,03% og 0,1%, er betydeligt mere effektiv (p
Tabel 2 Effekt i den tredje uge
§ lavere værdier = større forbedring
Forekomsten af lokal hudforbrænding var højere i tacrolimus -grupperne end i hydrokortisongruppen. Pruritus faldt over tid i tacrolimus -grupperne, men ikke i hydrocortisongruppen. Der var ingen relevante kliniske ændringer i laboratoriet eller værdier for vitale tegn i hver behandlingsgruppe i løbet af undersøgelsen.
Formålet med den tredje multicenter, dobbeltblindede, randomiserede undersøgelse var at evaluere effektiviteten og sikkerheden af tacrolimus salve 0,03% påført en eller to gange dagligt sammenlignet med to gange daglig påføring af hydrokortisonacetatsalve 1% hos børn med moderat til svær atopisk dermatitis Behandlingsvarigheden var større end tre uger.
Tabel 3 Effekt i den tredje uge
§ højere værdier = større forbedring
Det primære endepunkt blev defineret som det procentvise fald i mEASI fra baseline til slutningen af behandlingen. Statistisk signifikant forbedring blev observeret med tacrolimus salve 0,03% en eller to gange dagligt sammenlignet med hydrocortisonacetatsalve to gange dagligt (p
I det fjerde, åbne, langsigtede sikkerhedsstudie modtog cirka 800 patienter (alder ≥ 2 år) tacrolimus salve 0,1% i op til fire år, enten intermitterende eller kontinuerligt, hvor 300 patienter modtog behandling i mindst tre år og 79 patienter, der modtog behandling i minimum 42 måneder. Baseret på ændringen fra baseline i EASI -score og påvirket kropsområde viste patienter, uanset alder, forbedring af deres atopisk dermatitis på alle efterfølgende tidspunkter. Endvidere var der ingen tegn på tab af effektivitet under hele det kliniske studie.
Den samlede forekomst af bivirkninger havde en tendens til at falde, efterhånden som undersøgelsen skred frem for alle patienter uanset alder. De tre mest almindelige rapporterede bivirkninger var influenzalignende symptomer (forkølelse, forkølelse, influenza, øvre luftvejsinfektioner osv.), Kløe og forbrænding af huden. Der blev ikke observeret bivirkninger i korttidsundersøgelser og / eller observeret i tidligere undersøgelser i dette langtidsstudie.
Effekten og sikkerheden af tacrolimus salve til vedligeholdelsesbehandling af mild til svær atopisk dermatitis blev evalueret hos 524 patienter i to fase III multicenter kliniske forsøg med lignende design hos henholdsvis voksne patienter (≥16 år) og voksne patienter. 2-15 år).
I begge undersøgelser gennemgik patienter med igangværende sygdom en Open -Label Period (OLP), hvori berørte læsioner blev behandlet med tacrolimus salve to i op til 6 uger. Gange om dagen, indtil forbedringen nåede en forudbestemt score (Investigators Global Assessment - IGA ≤ 2, dvs. læsioner, der forsvandt, næsten forsvandt eller var til stede i en mild form). Herefter begyndte patienterne en periode med dobbeltblind kontrolperiode (DCP) sygdomsbekæmpelse i 12 måneder. Patienter blev randomiseret til at modtage tacrolimus salve (0,1% for voksne, 0,03% for børn) eller køretøj en gang om dagen to gange om ugen, mandage og torsdage.
Efter forekomsten af en sygdomsblussning blev patienterne behandlet med åben tacrolimus salve to gange dagligt i op til 6 uger, indtil IGA -score vendte tilbage til ≤2.
Det primære mål i begge undersøgelser var at vurdere antallet af sygdomsforværringer, der kræver "betydelig terapeutisk intervention" i DCP-perioden, defineret som en forværring med en IGA på 3-5 (dvs. moderat, alvorlig og meget alvorlig sygdom). Alvorlig) i løbet af den første dag af eksacerbationen, der krævede mere end 7 dages behandling. Begge undersøgelser viste en betydelig fordel med to gange ugentligt behandling med tacrolimus salve i forhold til centrale primære og sekundære endepunkter over en 12-måneders periode i en population af patienter med let til svær atopisk I en populationsundersøgelse af patienter med moderat til svær atopisk dermatitis forblev disse forskelle statistisk signifikante (tabel 4). Ingen hændelser blev observeret i disse undersøgelser. bivirkninger ikke tidligere rapporteret.
Tabel 4 Effekt (moderat til svær subpopulation)
DE: Sygdomsforværring
P.
En 7-måneders, dobbeltblind, randomiseret undersøgelse blev udført i parallelle grupper af pædiatriske patienter (2-11 år) med moderat til svær atopisk dermatitis. I den ene arm blev patienterne behandlet med Protopic 0,03% salve (n = 121) to gange dagligt i 3 uger og derefter en gang dagligt, indtil læsioner forsvandt. I kontrolarmen blev patienterne behandlet med 1% hydrocortisonacetat (HA) salve til hoved og hals og 0,1% hydrocortisonbutyratsalve til bagagerum og lemmer (n = 111) to gange dagligt i 2 uger og derefter med HA to gange om dagen i det hele taget berørte områder. I løbet af denne periode modtog alle patienter og kontrolpersoner (n = 44) en primær immunisering og en booster med en proteinkonjugeret vaccine mod undergruppe C i Neisseria meningitidis.
Undersøgelsens primære endepunkt var responsfrekvensen på vaccination, defineret som procentdelen af patienter med en serumbaktericid antistof (SBA) titer ≥8 ved besøg i uge 5. "Responsfrekvensanalysen i uge 5 viste en" ækvivalens mellem behandling grupper (hydrocortison 98,3%, tacrolimus salve 95,4%; 7-11 år: 100%i begge arme) Resultater i kontrolgruppen var ens.
Den primære reaktion på vaccination blev ikke påvirket.
05.2 Farmakokinetiske egenskaber
Kliniske data har vist, at tacrolimus -koncentrationer i den systemiske cirkulation efter lokal administration er minimale og, når de er målbare, forbigående.
Absorption
Data fra raske frivillige indikerer, at der er ringe eller ingen systemisk eksponering for tacrolimus efter enkelt eller gentagen topisk anvendelse af tacrolimus salve.
De fleste patienter (voksne og børn), der blev behandlet for atopisk dermatitis med en eller flere applikationer af tacrolimus salve (0,03 - 0,1%) og spædbørn fra 5 måneders alder, der blev behandlet med tacrolimus salve (0, 03%), havde behandlet legemsoverflade i blodkoncentrationer, den systemiske eksponering (dvs. AUC) for tacrolimus fra Protopic er cirka 30 gange lavere end den, der ses ved en oral immunosuppressiv dosis hos lever- eller nyretransplanterede patienter.Den laveste blodkoncentration af tacrolimus, hvormed den systemiske virkning kan observeres, er ukendt.
Der var ingen tegn på systemisk ophobning af tacrolimus hos patienter (voksne og børn), der blev behandlet i lange perioder (op til et år) med tacrolimus salve.
Fordeling
På grund af den lave systemiske eksponering af tacrolimus salve anses den høje binding af tacrolimus (> 98,8%) til plasmaproteiner ikke for klinisk relevant.
Efter topiske anvendelser af tacrolimus salve frigives tacrolimus selektivt til huden med minimal diffusion i den systemiske cirkulation.
Metabolisme
Der er ikke påvist metabolisme af tacrolimus af menneskelig hud. Systemisk tilgængelig tacrolimus metaboliseres overvejende i leveren af CYP3A4.
Eliminering
Ved intravenøs administration viste det sig, at tacrolimus var et lægemiddel med langsom eliminationshastighed.
Den gennemsnitlige kropsklarering er cirka 2,25 l / t. Eliminering i leveren af systemisk tilgængelig tacrolimus kan reduceres hos personer med alvorlig nedsat leverfunktion eller hos personer, der behandles samtidigt med lægemidler, der er stærke CYP3A4 -hæmmere.
Efter gentagne lokale applikationer af salven blev den gennemsnitlige halveringstid for tacrolimus anslået til 75 timer hos voksne og 65 timer hos børn.
Pædiatrisk population
Tacrolimus 'farmakokinetik efter topisk anvendelse ligner dem, der er rapporteret hos voksne, med minimal systemisk eksponering og ingen tegn på akkumulering (se ovenfor).
05.3 Prækliniske sikkerhedsdata
Toksicitet efter gentagne behandlinger og lokal tolerabilitet
Gentagen topisk anvendelse af tacrolimus salve eller dets bæremiddel på rotter, kaniner og miniaturegris viste sig at være forbundet med milde hudforandringer såsom erytem, ødem og papler.
Hos rotter førte langvarig lokal behandling med tacrolimus til en tilstand af systemisk toksicitet, som involverede ændringer i nyrerne, bugspytkirtlen, øjnene og nervesystemet. Ændringerne skyldes den høje eksponering af gnavere som følge af den høje transdermale absorption af tacrolimus. Den eneste systemiske variation, der blev observeret hos dværgsvin til høje koncentrationer af salve (3%), var en lidt lavere vægtforøgelse hos hunner.
Kaniner viste sig at være særligt følsomme over for intravenøs administration af tacrolimus, da de udviste reversible kardiotoksiske virkninger.
Mutagenicitet
Testene in vitro og in vivo angav ikke et genotoksisk potentiale for tacrolimus.
Kræftfremkaldende egenskaber
Systemiske kræftfremkaldende undersøgelser hos mus (18 måneder) og rotter (24 måneder) afslørede ikke, at der findes kræftfremkaldende potentialer for tacrolimus.
I den dermale kræftfremkaldende undersøgelse, der varede 24 måneder, udført på mus med påføring af 0,1% salve, forekom ingen hudtumorer.I samme undersøgelse blev der observeret en øget forekomst af lymfom, forbundet med høj systemisk eksponering.
Som en del af et fotokarcinogenicitetsstudie blev hårløse albino -mus behandlet kronisk med tacrolimus salve og UV -stråling. "Stigning i antallet af tumorer. Det er ikke klart, om effekten af tacrolimus skyldes en systemisk immunsuppression eller en lokal effekt. En risiko for mennesker kan ikke udelukkes fuldstændigt, da potentialet for lokal immunsuppression ved langvarig brug af tacrolimus salve er ukendt.
Reproduktionstoksicitet
Embryo / fostertoksicitet blev observeret hos rotter og kaniner, men kun ved doser, der gav signifikant maternel toksicitet. Nedsat sædfunktion blev påvist hos hanrotter ved høje subkutane doser af tacrolimus.
06.0 LÆGEMIDDELOPLYSNINGER
06.1 Hjælpestoffer
Hvid vaselin; flydende paraffin; propylencarbonat; hvid bivoks; fast paraffin.
06.2 Uforenelighed
Ikke relevant.
06.3 Gyldighedsperiode
3 år.
06.4 Særlige opbevaringsforhold
Må ikke opbevares over 25 ° C.
06.5 Den umiddelbare emballages art og emballagens indhold
Lamineret rør med lav densitet polyethylen foring, lukket med hvid polypropylen skruelåg.
Pakninger med 10 g, 30 g og 60 g. Ikke alle pakningsstørrelser er nødvendigvis markedsført.
06.6 Brugsanvisning og håndtering
Ingen særlige instruktioner.
Ubrugt medicin og affald fra denne medicin skal bortskaffes i overensstemmelse med lokale regler.
07.0 INDEHAVER AF MARKEDSFØRINGSTILLADELSE
Astellas Pharma Europe B.V. - Sylviusweg 62, 2333 BE Leiden - Holland
08.0 MARKEDSFØRINGSTILLADELSESNUMMER
EU/1/02/201/001 Protopic 0,03% - AIC: 035575012
EU/1/02/201/002 Protopic 0,03% - AIC: 035575024
EU/1/02/201/005 Protopic 0,03% - AIC: 035575051
09.0 DATO FOR FØRSTE TILLADELSE ELLER FORNYELSE AF TILLADELSEN
Dato for første godkendelse: 28/02/2002
Fornyelsesdato: 20.11.2006