Elementaranalysen af proteiner giver følgende gennemsnitsværdier: 55% kulstof, 7% hydrogen og 16% nitrogen; det er klart, at proteiner adskiller sig fra hinanden, men deres gennemsnitlige elementære sammensætning adskiller sig lidt fra værdierne angivet ovenfor .
Grundlovgivningsmæssigt er proteiner makromolekyler dannet af naturlige a-aminosyrer; aminosyrerne forbinder sig gennem amidbindingen, som etableres ved reaktionen mellem en aminogruppe af en a-aminosyre og carboxylen i en anden a-aminosyre.
Denne binding (-CO-NH-) kaldes også en peptidbinding, da den binder peptider (aminosyrer i kombination):
den opnåede er et dipeptid, fordi det består af to aminosyrer. Da et dipeptid indeholder en fri aminogruppe i den ene ende (NH2) og en carboxyl i den anden (COOH), kan det reagere med en eller flere aminosyrer og forlænge kæden både fra højre og fra venstre med samme reaktion set ovenfor.
Reaktionssekvensen (som i øvrigt egentlig ikke er så enkel) kan fortsætte på ubestemt tid: indtil der er en polymer kaldet polypeptid eller protein. Sondringen mellem peptider og proteiner er knyttet til molekylvægten: normalt for molekylvægte højere end 10.000 taler vi om proteiner.
At binde aminosyrer sammen for at opnå selv små proteiner er en vanskelig opgave, selvom der for nylig er blevet udviklet en automatisk metode til fremstilling af proteiner fra aminosyrer, hvilket giver fremragende resultater.
Det enkleste protein består derfor af 2 aminosyrer: efter international konvention starter den ordnede nummerering af aminosyrer i en proteinstruktur fra aminosyren med den frie a-aminogruppe.
kodning for dette protein), som støder på ikke ubetydelige kemiske vanskeligheder.
Det var muligt at bestemme den ordnede sekvens af aminosyrer gennem Edman-nedbrydning: proteinet omsættes med phenylisothiocyanat (FITC); initialt angriber a-amino-nitrogendoubletten phenylisothiocyanatet, der danner thiocarbamylderivatet; efterfølgende cykliserer det opnåede produkt, hvilket giver phenylthiohydantoinderivatet, der er fluorescerende.
Edman har udtænkt en maskine kaldet en sequencer, der automatisk justerer parametrene (tid, reagenser, pH osv.) Til nedbrydning og giver den primære struktur af proteiner (for dette modtog han Nobelprisen).
Den primære struktur er ikke tilstrækkelig til fuldt ud at fortolke proteinmolekylernes egenskaber; det menes, at disse egenskaber på en væsentlig måde afhænger af den rumlige konfiguration, som proteinmolekylerne har tendens til at antage, foldende på forskellige måder: det vil sige at antage, hvad der er blevet defineret som sekundær struktur af proteiner.
Den sekundære struktur af proteiner flimrer, det vil sige, at den har en tendens til at gå i opløsning ved opvarmning; så denaturerer proteinerne sig selv og mister mange af deres karakteristiske egenskaber. Udover opvarmning over 70 ° C kan denaturering også skyldes bestråling eller reaktionernes virkning (f.eks. Fra stærke syrer).
Denaturering af proteiner på grund af den termiske virkning observeres f.eks. Ved opvarmning af æggehviden: det ses at miste sit geléagtige udseende og blive til et uopløseligt hvidt stof. Denaturering af proteiner fører imidlertid til ødelæggelse af deres sekundære struktur, men efterlader deres primære struktur uændret (sammenkædningen af de forskellige aminosyrer).
Proteiner indtager den tertiære struktur, når deres kæde, selvom den stadig er fleksibel trods bøjningen af den sekundære struktur, folder på en sådan måde, at der opstår et forvrænget tredimensionelt arrangement i form af et fast legeme. Ansvarlig for den tertiære struktur er frem for alt disulfidbindinger, der kan etableres mellem cystein -SH spredt langs molekylet.
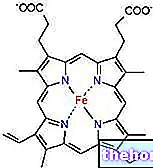
Den kvaternære struktur tilhører derimod kun proteiner dannet af to eller flere underenheder. Hæmoglobin, for eksempel, består af to par proteiner (det vil sige i alle fire proteinkæder) placeret ved en tetraeders hjørner for at give anledning til en sfærisk struktur; de fire proteinkæder holdes sammen af kræfter ioniske og ikke-kovalente bindinger.
Et andet eksempel på en kvaternær struktur er insulin, der ser ud til at bestå af så mange som seks proteinunderenheder arrangeret parvis i hjørnerne af en trekant, i midten hvoraf to zinkatomer er.
Fiberholdige proteiner
De er proteiner med en vis stivhed og har en meget længere akse end den anden; det fibrøse protein, der findes i større mængder i naturen, er kollagen (eller kollagen).
Et fibrøst protein kan antage forskellige sekundære strukturer: a-helix, β-ark og, i tilfælde af kollagen, triple helix; α-helix er den mest stabile struktur efterfulgt af β-arket, mens den mindst stabile af de tre er triple helix.
ret hvis der efter hovedskelettet (orienteret fra bund til top) udføres en bevægelse svarende til skruen på en højre skrue; mens helixen er af venstre hånd hvis bevægelsen er analog med skruen af en venstrehåndet skrue. I de højre α-spiraler er aminosyrernes -R substituenter vinkelret på proteinets hovedakse og vender udad, mens de er i venstre- hånd a -spiraler -R substituenterne vender indad. Højrehåndede a-spiraler er mere stabile end venstrehåndede, fordi mellem vati -R c "er der mindre interaktion og mindre sterisk hindring. Alle a-spiraler, der findes i proteiner, er dextrorotale.
Strukturen af a-helixen stabiliseres af hydrogenbindinger (hydrogenbroer), der dannes mellem carboxylgruppen (-C = O) i hver aminosyre og aminogruppen (-NH) fundet fire rester senere i lineær sekvens.
Et eksempel på et protein med en a-helix-struktur er hårkeratin.
Ved at forlænge a-helixstrukturen udføres overgangen fra a-helix til β-ark; også varmen eller den mekaniske belastning tillader at passere fra a-helixen til β-arkstrukturen.
Normalt er β-arkstrukturer i et protein tæt på hinanden, fordi hydrogenkæder mellem kæder kan etableres mellem dele af selve proteinet.
I fibrøse proteiner er det meste af proteinstrukturen organiseret i et a-helix eller β-ark.
Kugleformede proteiner
De har en næsten sfærisk rumlig struktur (på grund af de mange ændringer i retning af polypeptidkæden); nogle dele af væren kan spores tilbage til en a-helix eller β-arkstruktur, og andre dele kan i stedet ikke tilskrives disse former: arrangementet er ikke tilfældigt, men organiseret og gentaget.
De hidtil omtalte proteiner er stoffer i en fuldstændig homogen sammensætning: det vil sige rene sekvenser af kombinerede aminosyrer; sådanne proteiner siges enkel; der er proteiner, der består af en proteindel og en ikke-proteindel (prostatagruppe) kaldet proteiner konjugere.
, i neglene, i hornhinden og i øjenlinsen, mellem interstitielle rum i nogle organer (f.eks. lever) og så videre.
Dens struktur giver den særlige mekaniske evner; den har stor mekanisk styrke forbundet med høj elasticitet (f.eks. i sener) eller høj stivhed (f.eks. i knogler) afhængigt af den funktion, den skal udføre.
En af de mest nysgerrige egenskaber ved kollagen er dets konstituerende enkelhed: det består af ca. 30% prolin og ca. 30% glycin; de øvrige 18 aminosyrer behøver kun at dele de resterende 40% af proteinstrukturen. Aminosyresekvensen for kollagen er bemærkelsesværdig regelmæssig: for hver tre rester er den tredje glycin.
Proline er en cyklisk aminosyre, hvor R-gruppen binder sig til α-amino-nitrogenet, og det giver det en vis stivhed.
Den endelige struktur er en gentagen kæde med form som en "helix; inden for kollagenkæden er hydrogenbindinger fraværende. Kollagen er en "venstre spiral med en stigning (længde svarende til en drejning af spiralen) større end" α-helixen; kollagenhelixen er så løs, at tre proteinkæder er i stand til at vikle rundt om hinanden og danne en " enkelt reb: triple helix struktur.
Den tredobbelte helix af kollagen er imidlertid mindre stabil end både a-helixen og β-arkstrukturen.
Lad os nu se den mekanisme, hvormed kollagen produceres; overvej f.eks. brud på et blodkar: dette brud ledsages af et utal af signaler med det formål at lukke karret og dermed danne blodproppen.
Koagulation kræver mindst tredive specialiserede enzymer. Efter blodproppen er det nødvendigt at fortsætte med reparationen af vævet; celler tæt på såret producerer også kollagen. For at gøre dette fremkaldes først ekspressionen af et gen, det vil sige organismer, der ud fra informationen fra et gen er i stand til at producere proteinet (den genetiske information transkriberes på mRNA, der forlader kernen og når ribosomerne i cytoplasma, hvor den genetiske information oversættes til protein). Derefter syntetiseres kollagenet i ribosomerne (det ligner en venstre spiral sammensat af ca. 1200 aminosyrer og har en molekylvægt på ca. 150.000 d) og akkumuleres derefter i lumen, hvor det bliver et substrat for enzymer, der er i stand til at udføre posttranslationelle modifikationer (modifikationer af sproget oversat med "mRNA); i kollagen består disse modifikationer i hydroxylering af nogle sidekæder, især prolin og lysin.
Svigt af de enzymer, der fører til disse ændringer, forårsager skørbugt: det er en sygdom, der i første omgang forårsager brud på blodkar, brud på tænderne, som kan efterfølges af interintestinale blødninger og død; det kan skyldes kontinuerlig brug af fødevarer med lang levetid.
På grund af virkningen af andre enzymer sker der efterfølgende andre modifikationer, som består i glykosideringen af hydroxylgrupperne af prolin og lysin (et sukker binder sig til oxygenet i OH); disse enzymer findes i andre områder end lumen, derfor vandrer proteinet, mens det undergår ændringer, inde i det endoplasmatiske retikulum for at ende i sække (vesikler), der lukker sig selv og løsner sig fra nethinden: inde i dem er det indeholdt det glycosiderede pro -kollagenmonomer; sidstnævnte når Golgi-apparatet, hvor bestemte enzymer genkender cysteinet, der er til stede i den carboxy-terminale del af det glykosiderede pro-kollagen og får de forskellige kæder til at nærme sig hinanden og danne disulfidbroer: på denne måde tre kæder af glykosideret pro-kollagen opnås koblet sammen, og dette er udgangspunktet, hvorfra de tre kæder, der indtrænger, spontant giver anledning til den tredobbelte helix. kvæler sig selv, løsner sig fra Golgi -apparatet og transporterer de tre kæder mod cellens periferi, hvor gennem fusen ion med plasmamembranen, trimeteret udvises fra cellen.
I det ekstra cellulære rum er der særlige enzymer, pro-kollagenpeptidaser, som fjerner fra de arter, der udvises fra cellen, tre fragmenter (en for hver helix) af 300 aminosyrer l "en, fra den terminale carboxydel og tre fragmenter (en for hver helix) på ca. 100 aminosyrer hver fra den aminoterminale del: der er stadig en tredobbelt helix bestående af ca. 800 aminosyrer pr. helix kendt som tropokollagen.
Tropocollagen ser ud som en ret stiv stang; de forskellige trimere forbinder kovalente bindinger for at give større strukturer: mikrofibriller. I mikrofibrillerne er de forskellige trimere arrangeret forskudt; mange mikrofibriller udgør tropocollagen bundter.
I knoglerne, mellem kollagenfibrene, er der interstitielle rum, hvor sulfater og fosfater af calcium og magnesium afsættes: Disse salte dækker også alle fibrene; dette gør knoglerne stive.
I sener er interstitielle rum mindre rige på krystaller end i knogler, mens mindre proteiner er til stede end i tropocollagen: dette giver sener elasticitet.
Osteoporose er en sygdom forårsaget af mangel på calcium og magnesium, hvilket gør det umuligt at reparere salte i de interstitielle områder af tropocollagenfibrene.