Aktive ingredienser: Ketorolac
KEVINDOL 20 mg / ml orale dråber, opløsning
Kevindol indlægssedler er tilgængelige til pakningsstørrelser:- KEVINDOL 20 mg / ml orale dråber, opløsning
- KEVINDOL 30 mg / ml injektionsvæske, opløsning
Hvorfor bruges Kevindol? Hvad er det for?
FARMAKOTERAPEUTISK KATEGORI: ikke-steroide antiinflammatoriske / antireumatiske lægemidler
TERAPEUTISKE INDIKATIONER KEVINDOL: administreret intramuskulært eller intravenøst, er det indiceret til kortvarig behandling (maksimalt to dage) af moderat til svær akut postoperativ smerte. I tilfælde af større operationer eller meget alvorlige smerter kan KEVINDOL administreres intravenøst bruges som et supplement til et opioid analgetikum.
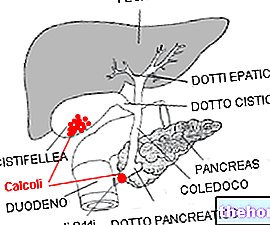
KEVINDOL injektionsvæske, opløsning er også indiceret til behandling af smerter på grund af nyrekolik.
Kontraindikationer Når Kevindol ikke bør bruges
Advarsel: lægemidlet er ikke indiceret ved lette eller kroniske smerter. Kevindol er kontraindiceret i følgende tilfælde
- Overfølsomhed over for det aktive stof eller over for et eller flere af hjælpestofferne.
- Hos patienter med allerede påvist overfølsomhed over for KEVINDOL eller andre NSAID'er og hos patienter, hvor aspirin eller andre hæmmere af prostaglandinsyntese har fremkaldt allergiske manifestationer (alvorlige anafylaktiske reaktioner er observeret hos disse patienter).
- Hele eller delvis syndrom af nasal polypose, angioødem, bronkospasme.
- Astmatiske anfald, rhinitis, urticaria.
- Aktivt mavesår eller en historie med gastrointestinal blødning, sårdannelse eller perforering.
- Ligesom andre ikke-steroide antiinflammatoriske lægemidler er KEVINDOL kontraindiceret hos patienter med alvorlig hjertesvigt.
- KEVINDOL hæmmer trombocytfunktionen og er derfor kontraindiceret hos patienter med tidligere, aktuelle eller formodede cerebrovaskulære blødninger, hos patienter, der har gennemgået højblødningsrisikokirurgi eller ufuldstændig hæmostase og hos patienter med stor risiko for blødning.
- Moderat eller svær nyreinsufficiens (serumkreatinin> 442 µmol / L) eller hos patienter med risiko for nyreinsufficiens på grund af hypovolæmi eller dehydrering.
- Skrumpelever eller alvorligt leversvigt.
- Hæmoragisk diatese.
- Koagulationsforstyrrelser.
- Patienter, der har gennemgået højrisiko blødningskirurgi eller ufuldstændig hæmostase
- Patienter i antikoagulant terapi.
- Samtidig behandling med ASA eller andre ikke-steroide antiinflammatoriske lægemidler og med litiumsalte, probenecid eller pentoxifyllin (se afsnittet Interaktioner).
- Intensive patienter med vanddrivende behandling.
- KEVINDOL hæmmer trombocytfunktionen og forlænger blødningstiden, derfor er det kontraindiceret til brug ved kirurgisk smertestillende profylakse og under operationen, fordi det øger risikoen for blødning.
- Hos børn og unge under 16 år.
- Brug af KEVINDOL er kontraindiceret i tredje trimester af graviditeten, nær og under fødslen og under amning.
Advarsel: Injektionsvæsken, opløsning indeholder ethanol, derfor er brug af epidural eller intratekal vej kontraindiceret.
Forholdsregler ved brug Hvad du skal vide, før du tager Kevindol
Advarsel: KEVINDOL kan ikke betragtes som en simpel smertelindring og skal bruges under nøje overvågning af lægen.
Det bør ikke bruges til behandling af milde eller kroniske smerter.
Nogle epidemiologiske beviser tyder på, at KEVINDOL kan være forbundet med en højere risiko for alvorlig gastrointestinal toksicitet sammenlignet med andre NSAID'er, især når det bruges uden for de godkendte indikationer og / eller i længere perioder (se også afsnit Terapeutiske indikationer, dosis, metode og administrationstid og kontraindikationer).
Samtidig brug af KEVINDOL med andre NSAID'er bør undgås, herunder selektive cyclooxygenase-2-hæmmere.
Uønskede virkninger kan minimeres ved at bruge den laveste effektive dosis i den kortest mulige behandlingstid, der er nødvendig for at kontrollere symptomerne. Inden behandling påbegyndes med KEVINDOL, skal det sikres, at patienten ikke tidligere har haft overfølsomhedsreaktioner over for KEVINDOL, acetylsalicylsyre og / eller andre ikke-steroide antiinflammatoriske lægemidler.
Mave -tarmblødning, sårdannelse og perforering
Gastrointestinal blødning, sårdannelse og perforering, som kan være dødelig, er til enhver tid blevet rapporteret under behandling med alle NSAID'er, med eller uden advarselssymptomer eller en tidligere historie med alvorlige gastrointestinale hændelser.
Ældre borgere
Særlig forsigtighed bør udvises hos ældre eller svækkede patienter, da forekomsten af nogle af de bivirkninger kan være højere end hos yngre patienter. Ældre patienter har en øget hyppighed af bivirkninger på NSAID, især gastrointestinal blødning og perforering, hvilket kan være dødeligt (se afsnit Dosis, metode og tidspunkt for administration).
Svækkede patienter har øget risiko for sårdannelse og blødning. De fleste dødelige gastrointestinale hændelser forbundet med NSAID -brug forekommer hos ældre og / eller svækkede patienter.
Hos ældre personer kan der også forekomme en stigning i eliminationshalveringstiden for lægemidlet og en samtidig reduktion i clearance.Foruden en reduktion i den samlede dosis kan det derfor være hensigtsmæssigt med et længere interval mellem doserne (se afsnit Dosis, metode og tidspunkt for administration).
Gastrointestinale virkninger
KEVINDOL kan forårsage gastrointestinal irritation, sår og blødning hos patienter med eller uden en tidligere gastrointestinal sygdom. Patienter med nuværende eller tidligere inflammatoriske sygdomme i mave -tarmkanalen bør kun gennemgå behandlingen under strengt lægeligt tilsyn. Forekomsten af disse effekter stiger med dosis og behandlingsvarighed.
Brug ikke KEVINDOL og andre ikke-steroide antiinflammatoriske lægemidler på samme tid.
Hos ældre og hos patienter med mavesår, især hvis det er kompliceret med blødning eller perforering (se afsnittet Kontraindikationer), er risikoen for gastrointestinal blødning, sårdannelse eller perforering højere ved øgede doser af NSAID'er, inklusive KEVINDOL injektionsvæske, opløsning. Risikoen for alvorlig gastrointestinal blødning er dosisafhængig. Disse patienter bør starte behandlingen med den lavest tilgængelige dosis. Samtidig behandling med beskyttelsesmidler (f.eks. Misoprostol eller protonpumpehæmmere) bør overvejes for disse patienter og også for patienter, der tager aspirin med lav dosis eller andre lægemidler, der kan øge risikoen for gastrointestinale hændelser (se afsnittet Interaktioner).
NSAID'er bør administreres med forsigtighed til patienter med en historie med mave -tarmsygdom (ulcerøs colitis, Crohns sygdom), da disse tilstande kan forværres (se afsnittet Bivirkninger).
Når der opstår gastrointestinal blødning eller sårdannelse hos patienter, der tager KEVINDOL, skal behandlingen afbrydes.
Patienter, der tidligere har haft gastrointestinal toksicitet, især ældre, bør rapportere eventuelle mavesymptomer (især gastrointestinal blødning), især i de indledende behandlingsstadier.
Der bør udvises forsigtighed hos patienter, der tager samtidige lægemidler, der kan øge risikoen for sårdannelse eller blødning, såsom orale kortikosteroider, antikoagulantia, såsom warfarin, selektive serotonin -genoptagelseshæmmere eller trombocytantæmpende midler såsom aspirin (se afsnittet Interaktioner).
Som med andre NSAID'er, også med KEVINDOL, kan forekomsten og sværhedsgraden af gastrointestinale komplikationer stige med stigende dosis og behandlingsvarighed. Risikoen for alvorlig gastrointestinal blødning er dosisafhængig. Dette gælder især hos ældre patienter, der får en gennemsnitlig daglig dosis på mere end 60 mg / dag KEVINDOL. En historie med mavesår øger chancen for at udvikle alvorlige gastrointestinale komplikationer under behandling med KEVINDOL.
Åndedrætsvirkninger
På grund af interaktionen med metabolismen af arachidonsyre kan lægemidlet forårsage kriser i bronkospasme og muligvis andre pseudo-allergiske fænomener eller chok hos astmatikere og disponerede personer.
Hæmatologiske virkninger
KEVINDOL hæmmer trombocytfunktionen og kan forlænge blødningstiden. KEVINDOL bør administreres med stor forsigtighed til patienter med koagulationsforstyrrelser, og disse bør overvåges nøje.Selvom undersøgelser ikke indikerer en signifikant interaktion mellem KEVINDOL og warfarin eller heparin, blev samtidig brug af KEVINDOL og lægemidler, der forstyrrer hæmostase, herunder terapeutiske doser af antikoagulantia, såsom warfarin, lavdosis heparin (2500-5000 IE hver 12 timer) administreret profylaktisk og dextrans, kan være forbundet med en øget risiko for blødning. KEVINDOL bør administreres med stor forsigtighed til disse patienter, som skal overvåges nøje (se afsnittet Kontraindikationer). Efter markedsføring er der rapporteret postoperative hæmatomer og andre tegn på sårblødning i forbindelse med den peri-operative anvendelse af KEVINDOL injektionsvæske, opløsning. Læger bør overveje den potentielle risiko for blødning, når hæmostase er kritisk, for eksempel i tilfælde af prostata -resektion, tonsillektomi eller kosmetisk kirurgi (se kontraindikationer).
Hudreaktioner
Alvorlige hudreaktioner, nogle af dem dødelige, herunder eksfoliativ dermatitis, Stevens-Johnsons syndrom og toksisk epidermal nekrolyse, er meget sjældent blevet rapporteret i forbindelse med brug af NSAID'er (se afsnittet Bivirkninger). Højere risiko: reaktionens begyndelse forekommer i de fleste tilfælde inden for den første behandlingsmåned. KEVINDOL bør seponeres ved det første udseende af udslæt, slimhinderlæsioner eller andre tegn på overfølsomhed. Natrium / væskeophobning hos patienter med hjerte -kar -sygdom og perifert ødem
Der skal udvises forsigtighed hos patienter med en historie med mild til moderat hypertension og / eller kongestivt hjertesvigt, da væskeretention og ødem er blevet rapporteret i forbindelse med NSAID -behandling.
Væskeretention, hypertension og perifert ødem er blevet observeret hos nogle patienter, der tager NSAID, herunder KEVINDOL, og bør derfor anvendes med forsigtighed til patienter med hjertesvigt, hypertension eller lignende tilstande.
Kardiovaskulære og cerebrovaskulære effekter
Da væskeretention og ødem er blevet rapporteret i forbindelse med brug af NSAID'er, bør patienter med tidligere hypertension og / eller let til moderat kongestiv hjertesvigt monitoreres og advares på passende vis.
Kliniske undersøgelser og epidemiologiske data tyder på, at brugen af selektive cyclooxygenase-2-hæmmere og nogle NSAID'er (især ved høje doser og i lang tid) kan være forbundet med en øget risiko for arterielle trombotiske hændelser (f.eks. Myokardieinfarkt eller slagtilfælde) Selvom KEVINDOL har ikke har vist sig at øge trombotiske hændelser såsom myokardieinfarkt, er der ikke tilstrækkelige data til rådighed til at udelukke denne risiko med KEVINDOL.
Patienter med ukontrolleret hypertension, kongestiv hjertesvigt, kronisk iskæmisk hjertesygdom, perifer arteriel sygdom og / eller cerebral vaskulær sygdom bør kun behandles med KEVINDOL efter grundig overvejelse. En lignende vurdering bør foretages, før behandling af patienter med risikofaktorer for hjerte -kar -sygdomme påbegyndes (f.eks. Hypertension, hyperlipidæmi, diabetes mellitus, rygning).
Nyreeffekter
KEVINDOL, ligesom andre ikke-steroide antiinflammatoriske lægemidler (NSAID'er), hæmmer syntesen af prostaglandiner, som kan forårsage nefrotoksicitet, herunder glomerulonefritis, interstitiel nefritis, papillær nekrose, nefrotisk syndrom og akut nyresvigt.
Derfor kræver KEVINDOL særlige forholdsregler eller kræver, at det udelukkes fra brug, når følgende tilstande er til stede hos patienten: tilstander af nyrehypoperfusion, nyresygdom, levercirrhose eller alvorlig hepatitis.
Patienter med nedsat nyrefunktion
KEVINDOL bør, ligesom andre ikke-steroide antiinflammatoriske lægemidler (NSAID'er), anvendes med forsigtighed til patienter med nedsat nyrefunktion eller med en nyresygdom, da det hæmmer prostaglandinsyntese. Hos sådanne patienter kan administration af KEVINDOL og andre NSAID'er forårsage en reduktion i blodmængde og / eller nyreblodgennemstrømning, hvor prostaglandiner spiller en understøttende rolle i opretholdelsen af renal perfusion. Hos sådanne patienter kan administration af KEVINDOL eller andre NSAID'er resultere i en dosisafhængig reduktion i renal prostaglandinproduktion og kan udløse tydeligt nedsat nyrefunktion eller svigt. Patienter med størst risiko for denne reaktion er patienter med kronisk nedsat nyrefunktion, hjertesvigt, leversvigt, patienter i diuretisk behandling og ældre. Symptomer forsvinder normalt med seponering af KEVINDOL eller andre ikke-steroide antiinflammatoriske lægemidler (NSAID'er).
Da KEVINDOL og dets metabolitter hovedsageligt udskilles af nyrerne, skal der udvises forsigtighed hos patienter med nedsat nyrefunktion under behandling med KEVINDOL. Især er brugen af KEVINDOL til patienter med serumkreatininværdier større end 442 µg / L kontraindiceret.
Lægemidlet er kontraindiceret ved intensiv vanddrivende behandling.
Patienter med nedsat leverfunktion
Milde ændringer i leverfunktionstest er sjældent blevet observeret under behandling med KEVINDOL, dog uden klinisk relevans. Det er imidlertid tilrådeligt at overvåge leverfunktionen hos patienter, hos hvem dette tidligere var nedsat, og afbryde behandlingen med KEVINDOL, hvis der er tegn på alvorlig nedsat leverfunktion.
Anafylaktiske (anafylaktoide) reaktioner
Anafylaktiske (anafylaktoide) reaktioner (herunder, men ikke begrænset til, anafylaksi, bronkospasme, rødme, udslæt, hypotension, larynxødem og angioødem) kan forekomme hos patienter med eller uden en "historie med overfølsomhed over for aspirin, andre NSAID'er eller KEVINDOL. Disse kan også forekomme hos mennesker med en "historie med angioødem, bronkospastisk reaktivitet (f.eks. astma), overfølsomhed og nasal polyposis." Anafylaktoide reaktioner, såsom anafylaksi, kan være dødelige. Derfor bør KEVINDOL anvendes med forsigtighed til patienter med astmahistorie og til patienter med fuldstændigt eller delvis syndrom af nasal polyposis, angioødem og bronkospasme.
Fertilitetsrelaterede forholdsregler
Anvendelse af KEVINDOL injektionsvæske, som med ethvert lægemiddel, der hæmmer prostaglandinsyntese og cyclooxygenase, kan forringe fertiliteten og anbefales ikke til kvinder, der har til hensigt at blive gravide.
KEVINDOL -administration bør seponeres hos kvinder, der har fertilitetsproblemer, eller som er under fertilitetsundersøgelser.
Natrium / væskeophobning hos patienter med hjerte -kar -sygdom og perifert ødem
Væskeretention, hypertension og ødem er blevet rapporteret ved brug af KEVINDOL og bør derfor anvendes med forsigtighed til patienter med hjertesvigt, hypertension eller lignende tilstande.
Narkotikamisbrug og afhængighed
KEVINDOL viste sig at være fri for potentiel afhængighed. Der er ikke observeret abstinenssymptomer efter pludselig seponering af KEVINDOL injektionsvæske, opløsning.
Interaktioner Hvilke lægemidler eller fødevarer kan ændre virkningen af Kevindol
Samtidig brug af KEVINDOL og andre ikke-steroide antiinflammatoriske lægemidler bør undgås.
Kortikosteroider: øget risiko for gastrointestinal sårdannelse eller blødning (se afsnittet Forholdsregler ved brug).
Trombocytplader og selektive serotonin genoptagelseshæmmere (SSRI'er): øget risiko for gastrointestinal blødning (se afsnittet Forholdsregler ved brug).
Hos patienter, der behandles samtidigt med ASA eller andre NSAID'er, synes risikoen for NSAID-relaterede alvorlige bivirkninger at være øget. KEVINDOL hæmmer blodpladeaggregering, reducerer tromboxankoncentrationer og forlænger blødningstiden.I modsætning til aspirin, hvis virkninger er forlængede, vender trombocytfunktionen tilbage til normal inden for 24-48 timer efter behandlingen er stoppet med KEVINDOL.
Antikoagulantia: NSAID'er kan forstærke virkningerne af antikoagulantia, såsom warfarin (se Forholdsregler ved brug) In vitro KEVINDOL forårsager ubetydelig reduktion i plasmaproteinbinding af warfarin.
Pentoxifyllin: Samtidig brug af pentoxifyllin kan øge risikoen for blødning. Probenecid: Samtidig administration af probenecid og KEVINDOL fører til en reduktion af sidstnævnte clearance og til en stigning i distributionsvolumen, øgede plasmakoncentrationer og øget blodtryk. " halveringstid for KEVINDOL. Methotrexat: Det er blevet rapporteret, at nogle lægemidler, der hæmmer prostaglandinsyntese, reducerer syntesen af methotrexat og derfor kan øge dets toksicitet. Nogle lægemidler, der hæmmer prostaglandinsyntese, er blevet rapporteret at hæmme renal clearance. af lithium, hvilket fører til en stigning i plasmakoncentrationen af sidstnævnte. Der har været rapporter om øgede plasmakoncentrationer af lithium under behandling med KEVINDOL.
KEVINDOL tromethamin ændrer ikke proteinbinding af digoxin. In vitro-undersøgelser indikerer, at ved terapeutiske koncentrationer af salicylat (300 µg / ml) blev bindingen af KEVINDOL reduceret fra cirka 99,2 til 97,5%, hvilket repræsenterer en potentiel dobbelt-stigning i plasmakoncentrationen af KEVINDOL, der ikke er bundet. Terapeutiske koncentrationer af digoxin, warfarin, ibuprofen, naproxen, piroxicam, acetaminophen, phenytoin og tolbutamid ændrer ikke proteinbinding af KEVINDOL tromethamin.
Furosemid: KEVINDOL injektionsvæske, opløsning kan interagere med furosemid og reducere dets vanddrivende virkning hos raske normovolemiske forsøgspersoner med ca. 20%, derfor bør der lægges særlig vægt på patienter med hjertesvigt.
Diuretika, ACE -hæmmere og angiotensin II -antagonister: NSAID'er kan reducere virkningen af diuretika og andre antihypertensive lægemidler. Risikoen for akut nyresvigt, som normalt er reversibel, kan øges hos nogle patienter med nedsat nyrefunktion (f.eks. Dehydreret eller ældre patienter), når ACE -hæmmere og / eller angiotensin II -receptorantagonister kombineres med NSAID. Disse interaktioner bør overvejes hos patienter, der tager KEVINDOL samtidigt med ACE -hæmmere eller angiotensin II -antagonister. Derfor bør kombinationen administreres med forsigtighed, især til ældre patienter.
Patienterne skal være tilstrækkeligt hydreret, og overvågning af nyrefunktionen bør overvejes efter initiering af samtidig behandling og periodisk derefter.
KEVINDOL har vist sig at reducere behovet for samtidig opioid analgetika til lindring af postoperative smerter. Antacida påvirker ikke graden af absorption.
Advarsler Det er vigtigt at vide, at:
SÆRLIGE ADVARSLER
Vigtig information om nogle af indholdsstofferne i KEVINDOL injektionsvæske, opløsning Advarsel: Injektionsvæsken indeholder ethanol, må derfor ikke anvendes neuraksielt (epidural eller intratekal).
Denne medicin indeholder 12,7 vol% ethanol (alkohol), f.eks. op til 100 mg pr. portion, svarende til cirka 2,5 ml øl og 1,1 ml vin pr. portion.
Det kan være skadeligt for alkoholikere.
Skal tages i betragtning hos gravide eller ammende kvinder, børn og højrisikogrupper, f.eks. Mennesker med leversygdom eller epilepsi.
For dem, der udøver sportsaktiviteter, kan brugen af medicin, der indeholder ethylalkohol, afgøre positive dopingtest i forhold til de alkoholkoncentrationsgrænser, der er angivet af nogle sportsforbund.
Graviditet og amning
Graviditet
KEVINDOL er kontraindiceret i tredje trimester af graviditeten, under fødsel, fødsel og amning (se kontraindikationer).
KEVINDOL bør kun bruges under graviditet, hvis den potentielle fordel for moderen begrunder den potentielle risiko for fosteret.
Inhibering af prostaglandinsyntese kan påvirke graviditet og / eller embryo / fosterudvikling negativt.
Resultater af epidemiologiske undersøgelser tyder på en øget risiko for abort og hjerte misdannelse og gastroschisis efter brug af en prostaglandinsyntesehæmmer i den tidlige graviditet.Den absolutte risiko for hjerte misdannelser steg fra mindre end 1% til cirka 1,5%. øges med dosis og behandlingsvarighed. Hos dyr har administration af prostaglandinsyntesehæmmere vist sig at forårsage øget tab før og efter implantation og embryoføtal dødelighed.
Derudover er der rapporteret om en øget forekomst af forskellige misdannelser, herunder kardiovaskulære, hos dyr, der fik prostaglandinsyntesehæmmere i den organogenetiske periode.
I graviditetens første og anden trimester bør KEVINDOL kun gives, hvis det er strengt nødvendigt.
Hvis KEVINDOL bruges til kvinder, der forsøger at blive gravide, eller i løbet af graviditetens første og andet trimester, bør dosis holdes lav og behandlingsvarigheden så kort som muligt.
I graviditetens tredje trimester kan alle prostaglandinsyntesehæmmere afsløre
- fosteret til:
- kardiopulmonal toksicitet (med for tidlig lukning af arteriekanalen og pulmonal hypertension);
- nedsat nyrefunktion, som kan udvikle sig til nyresvigt med oligo-hydroamnios;
- moderen og den nyfødte i slutningen af graviditeten til:
- mulig forlængelse af blødningstiden og trombocytblæsningseffekt, der kan forekomme selv ved meget lave doser;
- inhibering af livmoderkontraktioner, der resulterer i forsinket eller langvarig fødsel.
Derfor er KEVINDOL kontraindiceret i tredje trimester af graviditeten.
KEVINDOL bør kun administreres i de første to trimestre af graviditeten, hvis det er strengt nødvendigt. KEVINDOL krydser placenta i et omfang på ca. 10%.
Fertilitet
Brug af KEVINDOL, som med ethvert lægemiddel, der hæmmer prostaglandinsyntese og cyclooxygenase, frarådes til kvinder, der har til hensigt at blive gravide. KEVINDOL bør indstilles til kvinder, der har fertilitetsproblemer eller under fertilitetsundersøgelser.
Hos kvinder i den fødedygtige alder skal enhver graviditet altid udelukkes inden behandlingens start, og der skal sikres en effektiv præventionsdækning under behandlingen.
Arbejde og fødsel
Brugen af lægemidlet tæt på fødslen kan forårsage forsinkelse af selve fødslen; Desuden kan stoffet, hvis det administreres i denne periode, forårsage ændringer i hæmodynamikken i det ufødte barns lille cirkulation med alvorlige konsekvenser for åndedrættet. KEVINDOL er kontraindiceret under fødsel og fødsel, fordi det gennem sin virkning af hæmning af prostaglandinsyntese kan have negative virkninger på fostrets cirkulation og hæmme livmoderkontraktioner og dermed øge risikoen for livmoderblødning.
Fodringstid
KEVINDOL og dets metabolitter er blevet påvist i fosteret og i dyremælk KEVINDOL udskilles i modermælk i små mængder, derfor er det kontraindiceret hos ammende mødre.
Spørg din læge eller apotek til råds, før du tager medicin.
Virkninger på evnen til at føre motorkøretøj og betjene maskiner
Ved brug af KEVINDOL injektionsvæske, kan nogle patienter opleve søvnighed, svimmelhed, svimmelhed, søvnløshed eller depression. Hvis patienter oplever disse eller andre lignende bivirkninger, skal de være forsigtige med at udføre aktiviteter, der kræver opmærksomhed. Vær forsigtig, når de kører bil og ved hjælp af maskiner.
Dosering og anvendelsesmåde Sådan bruges Kevindol: Dosering
Advarsel: injektionsvæsken, opløsning indeholder ethanol, derfor må den ikke bruges epiduralt eller intratekalt.
Parenteralt bør behandlingsvarigheden ikke overstige 2 dage ved bolusadministration og 1 dag ved kontinuerlig infusion.
Den indgivne dosis bør være den laveste effektive dosis i forhold til smerteens sværhedsgrad og patientrespons.
Opløsningen er klar og let gullig, denne farve påvirker ikke lægemidlets effekt og sikkerhed.
Intramuskulær administration
VOKSNE
Voksne rådes til at starte med en dosis på 10 mg, efterfulgt af doser på 10-30 mg, der skal gentages hver 4-6 time efter behov op til maksimalt 90 mg / dag ved hjælp af den laveste effektive dosis.
Behandlingsvarigheden må ikke overstige 2 dage
På overgangsdagen fra parenteral til oral behandling bør den samlede daglige dosis på 90 mg ikke overskrides, husk at den maksimale orale dosis ikke må overstige 40 mg. Dosen bør reduceres tilstrækkeligt hos personer, der vejer mindre end 50 kg.
ÆLDRE (≥ 65 år)
Hos ældre patienter skal doseringen omhyggeligt fastlægges af lægen, som skal evaluere en mulig reduktion i de ovenfor angivne doser. Hos ældre patienter må den maksimale daglige dosis ikke overstige 60 mg / dag.
BØRN
Sikkerhed og effekt hos børn er ikke fastslået, og brugen af lægemidlet er derfor kontraindiceret under 16 år.
Intravenøs administration
INTRAVENOUS ANVENDELSE AF FORBEREDELSEN ER FORBEVARET TIL SYGEHUSER OG PLEJEHUS.
VOKSNE
I situationer præget af svær akut smerte (f.eks. Ved postoperativ smerteangrebsterapi) anbefales en startdosis på 10 mg efterfulgt af doser på 10-30 mg, som om nødvendigt kan gentages efter 4-6 timer ved hjælp af den laveste effektive dosis.Om nødvendigt kan behandlingen fortsætte med længere intervaller; den daglige dosis på 90 mg bør dog ikke overskrides.
ÆLDRE (≥ 65 år)
Hos ældre patienter bør den maksimale daglige dosis dog ikke overstige 60 mg / dag.
BØRN
Sikkerhed og effekt hos børn er ikke fastslået, og brugen af lægemidlet er derfor kontraindiceret under 16 år.
Nyrekolik
Den anbefalede dosering er et 30 mg hætteglas til intramuskulær eller intravenøs administration.
Overdosering Hvad skal man gøre, hvis man har taget en overdosis Kevindol
Symptomer og tegn
Efter en overdosis af KEVINDOL blev følgende fundet: erosiv gastritis, mavesår, mavesmerter, kvalme, opkastning, hyperventilation og nyrefunktion, som forsvandt ved seponering af lægemidlet.
Gastrointestinal blødning kan forekomme. Sjældent kan hypertension, akut nyresvigt, respirationsdepression og koma forekomme efter indtagelse af NSAID'er.
Anafylaktoide reaktioner er blevet rapporteret ved terapeutisk indtagelse af NSAID'er; dette kan ske som følge af overdosering.
Behandling: Der er ingen specifikke modgift.
I tilfælde af overdosering af NSAID'er bør symptomatisk og understøttende behandling anvendes. I tilfælde af utilsigtet indtagelse skal normale sikkerhedsforanstaltninger tilføjes til dette (fremkaldelse af opkastning, mave -skylning, administration af aktivt kul).
Dialyse eliminerer ikke KEVINDOL væsentligt fra blodbanen.
I tilfælde af utilsigtet indtagelse / indtagelse af en overdreven dosis KEVINDOL, skal du straks underrette din læge eller gå til det nærmeste hospital. Spørg din læge eller apotek, hvis du har spørgsmål om brugen af KEVINDOL.
Bivirkninger Hvad er bivirkningerne af Kevindol
Som al anden medicin kan dette forårsage bivirkninger, men ikke alle får det.
Efter markedsføring erfaring
Følgende bivirkninger kan forekomme hos patienter behandlet med Ketorolac; hyppigheden af rapporterede hændelser kendes ikke, da disse hændelser blev rapporteret frivilligt af et ikke-kvantificerbart antal mennesker.
Gastrointestinale lidelser: de mest almindeligt observerede bivirkninger er gastrointestinale. Mavesår, mavesår, perforering eller blødning, nogle gange dødelig, kan forekomme, især hos ældre (se afsnittet Forholdsregler ved brug). Kvalme, opkastning, diarré, flatulens, forstoppelse, dyspepsi er rapporteret efter administration af KEVINDOL. Mavesmerter / ubehag, følelse af fylde, melaena, rektal blødning, hæmatemese, ulcerøs stomatitis, øsofagitis, rapning, gastrointestinal ulceration, pancreatitis, mundtørhed, forværring af colitis og Crohns sygdom (se Forholdsregler ved brug).
Gastritis blev observeret sjældnere.
Infektioner og angreb: aseptisk meningitis
Lidelser i blod og lymfesystem: trombocytopeni, purpura, epistaxis.
Immunsystemforstyrrelser: anafylaksi; anafylaktoide reaktioner såsom anafylaksi kan have fatalt udfald; overfølsomhedsreaktioner såsom bronkospasme, vasodilatation, udslæt, hypotension, larynxødem.
Metabolisme og ernæringsforstyrrelser: anoreksi, hyperkaliæmi, hyponatriæmi
Psykiatriske lidelser: unormal tankegang, depression, søvnløshed, angst, irritabilitet, psykotiske reaktioner, unormal drømmeaktivitet, hallucinationer, eufori, koncentrationsbesvær, døsighed, sløvhed, forvirring. Nervesystemet: hovedpine, svimmelhed, kramper, paræstesi, hyperkinesi, ændret smag.
Øjensygdomme: synsforstyrrelser.
Øre- og labyrintforstyrrelser: tinnitus, høretab, svimmelhed.
Hjertesygdomme: hjertebanken, bradykardi, hjertesvigt. Ødem, hypertension og hjertesvigt er blevet rapporteret i forbindelse med NSAID -behandling.
Karsygdomme: hypertension, vasodilatation, hypotension, hæmatom, rødme, bleghed, postoperativ blødning fra sår. Kliniske undersøgelser og epidemiologiske data tyder på, at brug af COXIB'er og nogle NSAID'er (især ved høje doser og til langtidsbehandlinger) kan være forbundet med en beskeden øget risiko for arterielle trombotiske hændelser (f.eks. Myokardieinfarkt eller slagtilfælde) (se afsnittet Forholdsregler vedrørende brug). Selvom KEVINDOL ikke har vist sig at øge trombotiske hændelser såsom myokardieinfarkt, er der utilstrækkelige data til at udelukke en lignende risiko for KEVINDOL.
Reproduktionssystem og brystsygdomme: infertilitet hos kvinder.
Thorax- og mediastinale lidelser i luftvejene: lungeødem, dyspnø, astma.
Lever og galdeveje: hepatitis, kolestatisk gulsot, leversvigt.
Hud og subkutant væv: angioødem, eksfoliativ dermatitis, øget svedtendens, makulopapulært udslæt, urticaria, kløe, purpura, bulløse reaktioner, herunder Stevens-Johnsons syndrom og toksisk epidermal nekrolyse (meget sjældent).
Muskuloskeletale og bindevævssygdomme: myalgi
Nyrer og urinveje: polyuri, pollakiuri, oliguri, akut nyresvigt, uræmisk-hæmolytisk syndrom, interstitiel nefritis, urinretention, nefrotisk syndrom, flanksmerter (med eller uden hæmaturi, +/- azotaæmi). Som med andre lægemidler, der hæmmer syntese af renale prostaglandiner, kan der forekomme tegn på nedsat nyrefunktion efter administration af KEVINDOL, f.eks. men ikke begrænset til øgede niveauer af kreatinin og kalium.
Generelle lidelser og tilstande på administrationsstedet: asteni, feber, reaktioner på injektionsstedet, ødem, brystsmerter, overdreven tørst.
Undersøgelser: øget blødningstid, øget serumurinstof, øget kreatinin, unormale leverfunktionstests. Overholdelse af instruktionerne i indlægssedlen reducerer risikoen for bivirkninger.
Indberetning af bivirkninger
Tal med din læge eller apotek, hvis du får bivirkninger, herunder mulige bivirkninger, der ikke er anført i denne indlægsseddel. Bivirkninger kan også indberettes direkte via det nationale rapporteringssystem på www.agenziafarmaco.it/it/responsabili. Ved at rapportere bivirkninger kan du hjælpe med at give mere information om lægemidlets sikkerhed.
Udløb og opbevaring
Udløbsdato: se udløbsdatoen, der er trykt på pakken.
Den angivne udløbsdato refererer til produktet i intakt emballage, korrekt opbevaret.
Advarsel: brug ikke medicinen efter den udløbsdato, der står på pakningen. Opbevares i den originale emballage for at beskytte produktet mod lys.
Opbevaringstid efter rekonstituering af injektionsvæsken, opløsning:
I overensstemmelse med reglerne for god farmaceutisk praksis skal de intravenøse opløsninger tilberedes på tidspunktet for infusionen Den rekonstituerede opløsning skal bruges straks, og eventuelle rester skal kasseres.
Lægemidler bør ikke bortskaffes via spildevand eller husholdningsaffald. Spørg din apotek om, hvordan du skal smide medicin, du ikke længere bruger. Dette vil hjælpe med at beskytte miljøet.
OPBEVAR LÆGEMIDLET UTILGÆNGELIGT FOR BØRN
Andre oplysninger
SAMMENSÆTNING
Hvert hætteglas indeholder
Aktiv ingrediens: ketorolac trometamol 30 mg
Hjælpestoffer: ethylalkohol, natriumchlorid, vand til injektionsvæsker.
LÆGEMIDDELFORM OG INDHOLD
Injektionsvæske, opløsning. Æske med 3 ampuller à 1 ml.
Indlægsseddel: AIFA (Italian Medicines Agency). Indhold offentliggjort i januar 2016. De foreliggende oplysninger er muligvis ikke opdaterede.
For at få adgang til den mest opdaterede version er det tilrådeligt at få adgang til webstedet AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttige oplysninger.
01.0 LÆGEMIDLETS NAVN
KEVINDOL
02.0 KVALITATIV OG KVANTITATIV SAMMENSÆTNING
KEVINDOL 30 mg / ml injektionsvæske, opløsning
Hvert hætteglas indeholder:
Aktiv ingrediens: ketorolac trometamol 30 mg
KEVINDOL 20 mg / ml orale dråber, opløsning
1 ml opløsning indeholder:
Aktiv ingrediens: ketorolac trometamol 20 mg
Liste over hjælpestoffer findes i afsnit 6.1.
03.0 LÆGEMIDDELFORM
Injicerbar løsning.
Orale dråber, opløsning
04.0 KLINISKE OPLYSNINGER
04.1 Terapeutiske indikationer
KEVINDOL orale dråber, opløsning
KEVINDOL er kun indiceret til kortvarig (maks. 5 dage) behandling af moderate postoperative smerter.
KEVINDOL injektionsvæske, opløsning
KEVINDOL administreret intramuskulært eller intravenøst er indiceret til kortvarig (maksimalt to dage) behandling af akut moderat til svær postoperativ smerte.
I tilfælde af større operationer eller meget alvorlige smerter kan KEVINDOL administreres intravenøst bruges som et supplement til et opioid analgetikum.
KEVINDOL injektionsvæske, opløsning er også indiceret til behandling af smerter på grund af nyrekolik.
04.2 Dosering og indgivelsesmåde
KEVINDOL orale dråber, opløsning
Advarsel: behandlingens varighed må ikke overstige 5 dage.
VOKSNE
Den indgivne dosis bør være den laveste effektive dosis i forhold til smerteens sværhedsgrad og patientrespons.
Den anbefalede dosis til voksne er 10 mg (svarende til 10 dråber opløsning) efter behov hver 4-6 time op til maksimalt 40 mg / dag.
På overgangsdagen fra parenteral til oral behandling bør den samlede daglige dosis på 90 mg ikke overskrides, husk at den maksimale orale dosis ikke må overstige 40 mg.
Dosen bør reduceres tilstrækkeligt hos personer, der vejer mindre end 50 kg.
ÆLDRE (≥ 65 år)
Hos den ældre patient skal doseringen omhyggeligt fastlægges af lægen, som skal evaluere en mulig reduktion af de ovenfor angivne doser.
Oral drops formuleringen er særligt velegnet til patienter med synkebesvær.
BØRN
Sikkerhed og effekt hos børn er ikke fastslået, og brugen af lægemidlet er derfor kontraindiceret under 16 år (se pkt. 4.3).
KEVINDOL injektionsvæske, opløsning
Advarsel: injektionsvæsken, opløsning indeholder ethanol, derfor må den ikke bruges epiduralt eller intratekalt.
Parenteralt bør behandlingsvarigheden ikke overstige 2 dage ved bolusadministration og 1 dag ved kontinuerlig infusion.
Den indgivne dosis bør være den laveste effektive dosis i forhold til smerteens sværhedsgrad og patientrespons.
Opløsningen er klar og let gullig, denne farve påvirker ikke lægemidlets effekt og sikkerhed.
Intramuskulær administration
VOKSNE
Voksne rådes til at starte med en dosis på 10 mg, efterfulgt af doser på 10-30 mg, der skal gentages hver 4-6 time efter behov op til maksimalt 90 mg / dag ved hjælp af den laveste effektive dosis.
Behandlingsvarigheden må ikke overstige 2 dage.
På overgangsdagen fra parenteral til oral behandling bør den samlede daglige dosis på 90 mg ikke overskrides, husk at den maksimale orale dosis ikke må overstige 40 mg.
Dosen bør reduceres tilstrækkeligt hos personer, der vejer mindre end 50 kg.
ÆLDRE (≥65 år gammel)
Hos den ældre patient skal doseringen omhyggeligt fastlægges af lægen, som skal evaluere en mulig reduktion af de ovenfor angivne doser.
Hos ældre patienter bør den maksimale daglige dosis dog ikke overstige 60 mg / dag.
BØRN
Sikkerhed og effekt hos børn er ikke fastslået, og brugen af lægemidlet er derfor kontraindiceret under 16 år.
Intravenøs administration
INTRAVENOUS ANVENDELSE AF FORBEREDELSEN ER FORBEVARET TIL SYGEHUSER OG PLEJEHUS
VOKSNE
I situationer præget af alvorlig akut smerte (f.eks. Ved postoperativ smerteangrebsterapi) anbefales en startdosis på 10 mg efterfulgt af doser på 10-30 mg, som om nødvendigt kan gentages efter 4-6 timer ved hjælp af den laveste effektive dosis Om nødvendigt kan behandlingen fortsættes med længere intervaller, men den daglige dosis på 90 mg bør ikke overskrides.
ÆLDRE (≥ 65 år)
Hos ældre patienter bør den maksimale daglige dosis dog ikke overstige 60 mg / dag.
BØRN
Sikkerhed og effekt hos børn er ikke fastslået, og brugen af lægemidlet er derfor kontraindiceret under 16 år.
KIDNEY COLIC
Den anbefalede dosering er et 30 mg hætteglas til intramuskulær eller intravenøs administration.
04.3 Kontraindikationer
Advarsel: lægemidlet er ikke indiceret ved lette eller kroniske smerter.
Kevindol er kontraindiceret i følgende tilfælde
• Overfølsomhed over for det aktive stof eller over for et eller flere af hjælpestofferne.
• Hos patienter med allerede påvist overfølsomhed over for KEVINDOL eller andre NSAID'er og hos patienter, hvor aspirin eller andre prostaglandinsyntesehæmmere har fremkaldt allergiske reaktioner (alvorlige anafylaktiske reaktioner er observeret hos disse patienter).
• Helt eller delvist syndrom af nasal polypose, angioødem, bronkospasme.
• Astmatiske anfald, rhinitis, urticaria.
• Aktivt mavesår eller en historie med gastrointestinal blødning, sårdannelse eller perforering.
• Ligesom andre ikke-steroide antiinflammatoriske lægemidler er KEVINDOL kontraindiceret hos patienter med alvorlig hjertesvigt.
• KEVINDOL hæmmer trombocytfunktionen og er derfor kontraindiceret hos patienter med tidligere, nuværende eller formodet cerebrovaskulær blødning, hos patienter, der har gennemgået højrisiko blødningskirurgi eller ufuldstændig hæmostase og hos patienter med stor risiko for blødning.
• Moderat eller svær nyreinsufficiens (serumkreatinin> 442 μmol / L) eller hos patienter med risiko for nyreinsufficiens på grund af hypovolæmi eller dehydrering.
• Skrumpelever eller alvorligt leversvigt.
• Hæmoragisk diatese.
• Koagulationsforstyrrelser.
• Patienter, der er opereret med stor risiko for blødning eller ufuldstændig hæmostase.
• Patienter i antikoagulant terapi.
• Samtidig behandling med ASA eller andre ikke-steroide antiinflammatoriske lægemidler og med salte af lithium, probenecid eller pentoxifyllin (se afsnit 4.5).
• Patienter i intensiv vanddrivende behandling.
• KEVINDOL hæmmer trombocytfunktionen og forlænger blødningstiden, derfor er det kontraindiceret til brug ved kirurgisk smertestillende profylakse og under operationen, fordi det øger risikoen for blødning.
• Hos børn og unge under 16 år.
• Brug af KEVINDOL er kontraindiceret i tredje trimester af graviditeten, nær og under fødslen og under amning.
Advarsel: injektionsvæsken, opløsning indeholder ethanol, derfor er brug af epidural eller intratekal vej kontraindiceret.
04.4 Særlige advarsler og passende forholdsregler ved brug
Advarsel: KEVINDOL kan ikke betragtes som en simpel smertelindring og skal bruges under nøje overvågning af lægen.
KEVINDOL bør ikke bruges til behandling af milde eller kroniske smerter.
Nogle epidemiologiske beviser tyder på, at KEVINDOL kan være forbundet med en højere risiko for alvorlig gastrointestinal toksicitet sammenlignet med andre NSAID'er, især når det bruges uden for de godkendte indikationer og / eller i længere perioder (se også afsnit 4.1, 4.2 og 4.3).
Samtidig brug af KEVINDOL med andre NSAID'er bør undgås, herunder selektive cyclooxygenase-2-hæmmere.
Uønskede virkninger kan minimeres ved at bruge den laveste effektive dosis i den kortest mulige behandlingstid, der er nødvendig for at kontrollere symptomerne.
Inden behandling med KEVINDOL påbegyndes, skal det sikres, at patienten ikke tidligere har haft overfølsomhedsreaktioner over for KEVINDOL, acetylsalicylsyre og / eller andre ikke-steroide antiinflammatoriske lægemidler.
Mave -tarmblødning, sårdannelse og perforering
Gastrointestinal blødning, sårdannelse og perforering, som kan være dødelig, er blevet rapporteret når som helst under behandlingen med alle NSAID'er, inklusive KEVINDOL, med eller uden advarselssymptomer eller en tidligere historie med alvorlige gastrointestinale hændelser.
Ældre borgere
Særlig forsigtighed bør udvises hos ældre eller svækkede patienter, da forekomsten af nogle af de bivirkninger kan være højere end hos yngre patienter. Ældre patienter har en øget hyppighed af bivirkninger på NSAID, især gastrointestinal blødning og perforering, hvilket kan være dødeligt (se afsnit 4.2).
Svækkede patienter har øget risiko for sårdannelse og blødning. De fleste dødelige gastrointestinale hændelser forbundet med NSAID -brug forekommer hos ældre og / eller svækkede patienter.
Hos ældre personer kan der også være en stigning i eliminationshalveringstiden for lægemidlet og en samtidig reduktion i clearance.Foruden en reduktion i den samlede dosis kan det derfor være hensigtsmæssigt med et længere interval mellem doserne (se pkt.4.2 ).
Gastrointestinale virkninger
KEVINDOL kan forårsage gastrointestinal irritation, sår og blødning hos patienter med eller uden en tidligere gastrointestinal sygdom. Patienter med nuværende eller tidligere inflammatoriske sygdomme i mave -tarmkanalen bør kun gennemgå behandlingen under strengt lægeligt tilsyn. Forekomsten af disse effekter stiger med dosis og behandlingsvarighed.
Brug ikke KEVINDOL og andre ikke-steroide antiinflammatoriske lægemidler på samme tid.
Hos ældre og hos patienter med mavesår, især hvis det er kompliceret med blødning eller perforering (se pkt. 4.3), er risikoen for gastrointestinal blødning, ulceration eller perforering højere ved øgede doser af NSAID'er, inklusive KEVINDOL injektionsvæske, opløsning. Risikoen for alvorlig gastrointestinal blødning er dosisafhængig. Disse patienter bør starte behandlingen med den lavest tilgængelige dosis. Samtidig behandling med beskyttelsesmidler (f.eks. Misoprostol eller protonpumpehæmmere) bør overvejes for disse patienter og også for patienter, der tager lavdosis aspirin eller andre lægemidler, der kan øge risikoen for gastrointestinale hændelser (se pkt. 4.5).
NSAID bør administreres med forsigtighed til patienter med en historie med mave -tarmsygdom (ulcerøs colitis, Crohns sygdom), da disse tilstande kan forværres (se pkt. 4.8).
Patienter, der tidligere har haft gastrointestinal toksicitet, især ældre, bør rapportere eventuelle mavesymptomer (især gastrointestinal blødning), især i de indledende behandlingsstadier.
Når der opstår gastrointestinal blødning eller sårdannelse hos patienter, der tager KEVINDOL injektionsvæske, skal behandlingen seponeres.
Der skal udvises forsigtighed hos patienter, der tager samtidige lægemidler, der kan øge risikoen for sårdannelse eller blødning, såsom orale kortikosteroider, antikoagulantia såsom warfarin, selektive serotonin-genoptagelseshæmmere eller trombocytplastiske midler såsom aspirin (se pkt. 4.5).
Som med andre NSAID'er, også med KEVINDOL, kan forekomsten og sværhedsgraden af gastrointestinale komplikationer stige med stigende dosis og behandlingsvarighed. Risikoen for alvorlig gastrointestinal blødning er dosisafhængig. Dette gælder især hos ældre patienter, der får en gennemsnitlig daglig dosis på mere end 60 mg / dag KEVINDOL. En historie med mavesår øger chancen for at udvikle alvorlige gastrointestinale komplikationer under behandling med KEVINDOL.
Åndedrætsvirkninger
Til interaktion med metabolisme af arachidonsyre kan lægemidlet forårsage kriser i bronkospasme og muligvis andre pseudo-allergiske fænomener eller chok hos astmatikere og disponerede personer.
Hæmatologiske virkninger
KEVINDOL hæmmer trombocytfunktionen og kan forlænge blødningstiden.
KEVINDOL bør administreres med stor forsigtighed til patienter med koagulationsforstyrrelser, og disse bør overvåges nøje. Selvom undersøgelser ikke indikerer en signifikant interaktion mellem KEVINDOL og warfarin eller heparin, blev samtidig brug af KEVINDOL og lægemidler, der forstyrrer hæmostase, herunder terapeutiske doser af antikoagulantia, såsom warfarin, lavdosis heparin (2500-5000 IE hver 12 timer) administreret profylaktisk og dextrans, kan være forbundet med en øget risiko for blødning. KEVINDOL bør administreres med forsigtighed til disse patienter, som skal overvåges nøje (se pkt. 4.3).
Efter markedsføring er der rapporteret postoperative hæmatomer og andre tegn på sårblødning i forbindelse med den peri-operative anvendelse af KEVINDOL injektionsvæske, opløsning. Læger bør overveje den potentielle risiko for blødning, når hæmostase er kritisk, f.eks. I tilfælde af prostataresektion, tonsillektomi eller kosmetisk kirurgi (se pkt. 4.3).
Hudreaktioner
Alvorlige hudreaktioner, nogle af dem dødelige, herunder eksfoliativ dermatitis, Stevens-Johnsons syndrom og toksisk epidermal nekrolyse, er meget sjældent blevet rapporteret i forbindelse med brug af NSAID (se pkt. 4.8). I de tidlige behandlingsstadier ser det ud til, at patienter have større risiko: reaktionens begyndelse forekommer i de fleste tilfælde inden for den første behandlingsmåned.
KEVINDOL bør seponeres ved det første udseende af udslæt, slimhinderlæsioner eller andre tegn på overfølsomhed.
Natrium / væskeophobning hos patienter med hjerte -kar -sygdom og perifert ødem
Der skal udvises forsigtighed hos patienter med en historie med mild til moderat hypertension og / eller kongestivt hjertesvigt, da væskeretention og ødem er blevet rapporteret i forbindelse med NSAID -behandling.
Væskeretention, hypertension og perifert ødem er blevet observeret hos nogle patienter, der tager NSAID, herunder KEVINDOL, og bør derfor anvendes med forsigtighed til patienter med hjertesvigt, hypertension eller lignende tilstande.
Kardiovaskulære og cerebrovaskulære effekter
Da væskeretention og ødem er blevet rapporteret i forbindelse med brug af NSAID'er, bør patienter med tidligere hypertension og / eller let til moderat kongestiv hjertesvigt monitoreres og advares på passende vis.
Kliniske undersøgelser og epidemiologiske data tyder på, at brugen af selektive cyclooxygenase-2-hæmmere og nogle NSAID'er (især ved høje doser og i lang tid) kan være forbundet med en øget risiko for arterielle trombotiske hændelser (f.eks. Myokardieinfarkt eller slagtilfælde) Selvom KEVINDOL har ikke har vist sig at øge trombotiske hændelser såsom myokardieinfarkt, er der ikke tilstrækkelige data til rådighed til at udelukke denne risiko med KEVINDOL.
Patienter med ukontrolleret hypertension, kongestiv hjertesvigt, kronisk iskæmisk hjertesygdom, perifer arteriel sygdom og / eller cerebral vaskulær sygdom bør kun behandles med KEVINDOL efter grundig overvejelse. En lignende vurdering bør foretages, før behandling af patienter med risikofaktorer for hjerte -kar -sygdomme påbegyndes (f.eks. Hypertension, hyperlipidæmi, diabetes mellitus, rygning).
Nyreeffekter
KEVINDOL, ligesom andre ikke-steroide antiinflammatoriske lægemidler (NSAID'er), hæmmer prostaglandinsyntese, hvilket kan forårsage nefrotoksicitet, herunder glomerulonefritis, interstitiel nefritis, papillær nekrose, nefrotisk syndrom og akut nyresvigt.
Derfor kræver KEVINDOL særlige forholdsregler eller kræver, at det udelukkes fra brug, når følgende tilstande er til stede hos patienten: tilstander af nyrehypoperfusion, nyresygdom, levercirrhose eller alvorlig hepatitis.
Patienter med nedsat nyrefunktion
KEVINDOL bør, ligesom andre ikke-steroide antiinflammatoriske lægemidler (NSAID'er), anvendes med forsigtighed til patienter med nedsat nyrefunktion eller med en nyresygdom, da det hæmmer prostaglandinsyntese. Hos sådanne patienter kan administration af KEVINDOL og andre NSAID'er forårsage en reduktion i blodmængde og / eller nyreblodgennemstrømning, hvor prostaglandiner spiller en understøttende rolle i opretholdelsen af renal perfusion. Hos sådanne patienter kan administration af KEVINDOL eller andre NSAID'er resultere i en dosisafhængig reduktion i renal prostaglandinproduktion og kan udløse tydeligt nedsat nyrefunktion eller svigt. Patienter med større risiko for denne reaktion er patienter med kronisk nyreinsufficiens, hjertesvigt, leversvigt, patienter i diuretisk behandling og ældre. Symptomer forsvinder normalt med seponering af KEVINDOL eller andre ikke-steroide antiinflammatoriske lægemidler (NSAID'er).
Da KEVINDOL og dets metabolisme hovedsageligt udskilles af nyrerne, skal der udvises forsigtighed hos patienter med nedsat nyrefunktion under behandling med KEVINDOL. Især er brugen af KEVINDOL til patienter med serumkreatininværdier større end 442 μmol / L kontraindiceret.
Lægemidlet er kontraindiceret ved intensiv vanddrivende behandling.
Patienter med nedsat leverfunktion
Milde ændringer i leverfunktionstest er sjældent blevet observeret under behandling med KEVINDOL, dog uden klinisk relevans. Det er imidlertid tilrådeligt at overvåge leverfunktionen hos patienter, hos hvem dette tidligere var nedsat, og afbryde behandlingen med KEVINDOL, hvis der er tegn på alvorlig nedsat leverfunktion.
Anafylaktiske (anafylaktoide) reaktioner
Anafylaktiske (anafylaktoide) reaktioner (herunder, men ikke begrænset til, anafylaksi, bronkospasme, rødme, udslæt, hypotension, larynxødem og angioødem) kan forekomme hos patienter med eller uden en "historie med overfølsomhed over for aspirin, andre NSAID'er eller KEVINDOL Disse kan også forekomme hos personer med en "historie med angioødem, bronkospastisk reaktivitet (f.eks. astma), overfølsomhed og nasal polyposis." Anafylaktoide reaktioner, såsom anafylaksi, kan være dødelige. Derfor bør KEVINDOL anvendes med forsigtighed til patienter med astmahistorie og til patienter med fuldstændigt eller delvis syndrom af nasal polyposis, angioødem og bronkospasme.
Fertilitetsrelaterede forholdsregler
Anvendelse af KEVINDOL injektionsvæske, som med ethvert lægemiddel, der hæmmer prostaglandinsyntese og cyclooxygenase, kan forringe fertiliteten og anbefales ikke til kvinder, der har til hensigt at blive gravide.
KEVINDOL -administration bør seponeres hos kvinder, der har fertilitetsproblemer, eller som er under fertilitetsundersøgelser.
Natrium / væskeophobning hos patienter med hjerte -kar -sygdom og perifert ødem
Væskeretention, hypertension og ødem er blevet rapporteret ved brug af KEVINDOL og bør derfor anvendes med forsigtighed til patienter med hjertesvigt, hypertension eller lignende tilstande.
Narkotikamisbrug og afhængighed
KEVINDOL viste sig at være fri for potentiel afhængighed. Der er ikke observeret abstinenssymptomer efter pludselig seponering af KEVINDOL
KEVINDOL orale dråber, opløsning indeholder parahydroxybenzoater, der kan forårsage allergiske reaktioner (herunder forsinket).
KEVINDOL injektionsvæske, opløsning indeholder 100 mg ethylalkohol for hvert hætteglas, svarende til 10%; derfor kan produktet være skadeligt for alkoholikere og bør administreres med forsigtighed i grupper af patienter med risiko, f.eks. personer, der lider af leversygdom og epilepsi.
Injektioner skal udføres i henhold til strenge standarder for sterilisering, asepsis og antisepsis.
04.5 Interaktioner med andre lægemidler og andre former for interaktion
Samtidig brug af KEVINDOL og andre ikke-steroide antiinflammatoriske lægemidler bør undgås.
Kortikosteroider: øget risiko for gastrointestinal sårdannelse eller blødning (se pkt. 4.4).
Anti-aggregerende midler og selektive serotonin-genoptagelseshæmmere (SSRI'er): øget risiko for gastrointestinal blødning (se pkt. 4.4). Hos patienter, der behandles samtidigt med ASA eller andre NSAID'er, synes risikoen for NSAID-relaterede alvorlige bivirkninger at være øget.
KEVINDOL hæmmer blodpladeaggregering, reducerer tromboxankoncentrationer og forlænger blødningstiden.I modsætning til aspirin, hvis virkninger er forlængede, vender trombocytfunktionen tilbage til normal inden for 24-48 timer efter behandlingen er stoppet med KEVINDOL.
Antikoagulantia: NSAID'er kan forstærke virkningerne af antikoagulantia, såsom warfarin (se pkt. 4.4).
In vitro KEVINDOL forårsager ubetydelig reduktion i warfarins binding til plasmaproteiner.
Selvom undersøgelser ikke indikerer en signifikant interaktion mellem KEVINDOL og warfarin eller heparin, samtidig brug af KEVINDOL og lægemidler, der påvirker hæmostase, herunder terapeutiske doser af antikoagulanter som warfarin, lavdosis heparin (2500-5000 enheder hver 12. time) administreret profylaktisk og dextrans kan være forbundet med en øget risiko for blødning.
Pentoxifyllin: Samtidig brug af pentoxifyllin kan øge risikoen for blødning.
Probenecid: Samtidig administration af probenecid og KEVINDOL fører til nedsat clearance af sidstnævnte og til en stigning i distributionsvolumen, øgede plasmakoncentrationer og øget halveringstid for ketorolac.
Methotrexat: Nogle lægemidler, der hæmmer prostaglandinsyntese, er rapporteret at reducere syntesen af methotrexat og kan derfor øge dets toksicitet.
Lithium: Nogle lægemidler, der hæmmer prostaglandinsyntese, er rapporteret at hæmme renal clearance af lithium, hvilket fører til en stigning i lithiumplasmakoncentrationer Der har været rapporter om øgede plasmalithiumkoncentrationer under behandling med KEVINDOL.
Ketorolac tromethamin ændrer ikke proteinbinding af digoxin. In vitro-undersøgelser indikerer, at ved terapeutiske koncentrationer af salicylat (300 mcg / ml) blev bindingen af ketorolac reduceret fra ca. 99,2 til 97,5%, hvilket repræsenterer en potentiel to gange stigning i plasmakoncentrationen af ketorolac, der ikke er bundet.
Terapeutiske koncentrationer af digoxin, warfarin, ibuprofen, naproxen, piroxicam, acetaminophen, phenytoin og tolbutamid ændrer ikke proteinbindingen af ketorolac tromethamin.
Furosemid: KEVINDOL injektionsvæske, opløsning kan interagere med furosemid og reducere dets vanddrivende virkning hos raske normovolemiske forsøgspersoner med ca. 20%, derfor bør der lægges særlig vægt på patienter med hjertesvigt.
Diuretika, ACE -hæmmere og angiotensin II -antagonister: NSAID'er kan reducere virkningen af diuretika og andre antihypertensive lægemidler. Risikoen for akut nyresvigt, som normalt er reversibel, kan øges hos nogle patienter med nedsat nyrefunktion (f.eks. Dehydreret eller ældre patienter), når ACE -hæmmere og / eller angiotensin II -receptorantagonister kombineres med NSAID. Disse interaktioner bør overvejes hos patienter, der tager ketorolac samtidigt med ACE -hæmmere eller angiotensin II -antagonister. Derfor bør kombinationen administreres med forsigtighed, især til ældre patienter.
Patienterne skal være tilstrækkeligt hydreret, og overvågning af nyrefunktionen bør overvejes efter initiering af samtidig behandling og periodisk derefter.
KEVINDOL har vist sig at reducere behovet for samtidig opioid analgetika til postoperativ smertelindring.
Antacida påvirker ikke graden af absorption.
Se afsnit 6.2 for uforenelighed.
04.6 Graviditet og amning
Graviditet
KEVINDOL er kontraindiceret i graviditetens tredje trimester, under fødsel, fødsel og amning (se pkt. 4.3).
KEVINDOL bør kun bruges under graviditet, hvis den potentielle fordel for moderen begrunder den potentielle risiko for fosteret.
Inhibering af prostaglandinsyntese kan påvirke graviditet og / eller embryo / fosterudvikling negativt.
Resultater af epidemiologiske undersøgelser tyder på en øget risiko for abort, hjertemisdannelse og gastroschisis efter brug af en prostaglandinsyntesehæmmer i den tidlige graviditet Den absolutte risiko for hjertemisdannelser steg fra mindre end 1%, op til cirka 1,5%. Risikoen har været anses for at stige med dosis og behandlingsvarighed. Hos dyr har administration af prostaglandinsyntesehæmmere vist sig at forårsage øget tab af præ- og postimplantation og embryoføtal dødelighed.
Derudover er der rapporteret om en øget forekomst af forskellige misdannelser, herunder kardiovaskulære, hos dyr, der fik prostaglandinsyntesehæmmere i den organogenetiske periode.
I graviditetens første og anden trimester bør KEVINDOL kun gives, hvis det er strengt nødvendigt. Hvis KEVINDOL bruges til kvinder, der forsøger at blive gravide, eller i løbet af graviditetens første og andet trimester, bør dosis holdes lav og behandlingsvarigheden så kort som muligt.
I graviditetens tredje trimester kan alle prostaglandinsyntesehæmmere afsløre
• fosteret til:
• kardiopulmonal toksicitet (med for tidlig lukning af arteriekanalen og pulmonal hypertension);
• nedsat nyrefunktion, som kan udvikle sig til nyresvigt med oligo-hydroamnios;
• moderen og den nyfødte ved slutningen af graviditeten til:
• mulig forlængelse af blødningstiden og trombocytblæsningseffekt, der kan forekomme selv ved meget lave doser;
• inhibering af livmoderkoncentrationer, der resulterer i forsinket eller langvarig fødsel.
Derfor er KEVINDOL kontraindiceret i tredje trimester af graviditeten.
KEVINDOL bør kun administreres i de første to trimestre af graviditeten, hvis det er strengt nødvendigt.
KEVINDOL krydser placenta i et omfang på ca. 10%.
Fertilitet
Brug af KEVINDOL, som med enhver prostaglandinsyntese og cyclooxygenasehæmmer, anbefales ikke til kvinder, der planlægger at blive gravide (se pkt. 4.4).
KEVINDOL -administration bør seponeres hos kvinder, der har fertilitetsproblemer, eller som er under fertilitetsundersøgelser.
Hos kvinder i den fødedygtige alder skal enhver graviditet altid udelukkes inden behandlingens start, og der skal sikres en effektiv præventionsdækning under behandlingen.
Arbejde og fødsel
Brugen af lægemidlet tæt på fødslen kan forårsage forsinkelse af selve fødslen; Desuden kan stoffet, hvis det administreres i denne periode, forårsage ændringer i hæmodynamikken i det ufødte barns lille cirkulation med alvorlige konsekvenser for åndedrættet.
KEVINDOL er kontraindiceret under fødsel og fødsel, fordi det gennem sin virkning af hæmning af prostaglandinsyntese kan have negative virkninger på fostrets cirkulation og hæmme livmoderkontraktioner og dermed øge risikoen for livmoderblødning.
Fodringstid
KEVINDOL og dets metabolitter blev påvist hos foster og mælk fra dyr.
KEVINDOL udskilles i små mængder i modermælk, derfor er det kontraindiceret til ammende mødre.
04.7 Virkninger på evnen til at føre motorkøretøj og betjene maskiner
Nogle patienter kan opleve søvnighed, svimmelhed, svimmelhed, søvnløshed eller depression ved brug af KEVINDOL.Hvis patienter oplever disse eller andre lignende bivirkninger, skal de være forsigtige med at udføre aktiviteter, der kræver opmærksomhed.
Det er derfor tilrådeligt at være forsigtig, når du kører i biler og bruger maskiner.
04.8 Bivirkninger
Efter markedsføring erfaring
Følgende bivirkninger kan forekomme hos patienter, der får KEVINDOL; frekvenserne for de rapporterede hændelser kendes ikke, fordi de blev rapporteret frivilligt af et ikke -kvantificerbart antal mennesker.
Gastrointestinale lidelser: de mest almindeligt observerede bivirkninger er gastrointestinale. Mavesår, sår, perforering eller gastrointestinal blødning, nogle gange dødelig, kan forekomme, især hos ældre (se pkt. 4.4.
Kvalme, opkastning, diarré, flatulens, forstoppelse, dyspepsi, mavesmerter / ubehag, fylde, melaena, rektal blødning, hæmatemese, ulcerøs stomatitis, øsofagitis, rapninger, mave -tarm -ulceration, pancreatitis, mundtørhed, forværring af colitis og Crohns sygdom ( se afsnittet Forholdsregler ved brug).
Gastritis blev observeret sjældnere.
Infektioner og angreb: aseptisk meningitis.
Forstyrrelser i blod og lymfesystem: trombocytopeni, purpura, epistaxis.
Forstyrrelser i immunsystemet: anafylaksi; anafylaktoide reaktioner, såsom anafylaksi, kan være dødelige; overfølsomhedsreaktioner såsom bronkospasme, vasodilatation, rødme, udslæt, hypotension, larynxødem).
Metabolisme og ernæringsforstyrrelser: anoreksi, hyperkaliæmi, hyponatriæmi.
Psykiatriske lidelser: unormal tankegang, depression, søvnløshed, angst, irritabilitet, psykotiske reaktioner, unormal drømmeaktivitet, hallucinationer, eufori, koncentrationsbesvær, døsighed, sløvhed, forvirring.
Nervesystemet lidelser: hovedpine, svimmelhed, kramper, paræstesi, hyperkinesi, ændret smag.
Øjenlidelser: synsforstyrrelser.
Øre- og labyrintforstyrrelser: tinnitus, høretab, svimmelhed.
Hjertepatologier: hjertebanken, bradykardi, hjertesvigt.
Ødem, hypertension og hjertesvigt er blevet rapporteret i forbindelse med NSAID -behandling.
Vaskulære patologier: hypertension, vasodilatation, hypotension, blå mærker, rødme, bleghed, postoperativ blødning fra sår.
Kliniske undersøgelser og epidemiologiske data tyder på, at brug af COXIB og nogle NSAID'er (især ved høje doser og til langtidsbehandlinger) kan være forbundet med en beskeden øget risiko for arterielle trombotiske hændelser (f.eks. Myokardieinfarkt eller slagtilfælde) (se pkt.4.4) Selvom KEVINDOL ikke har vist sig at øge trombotiske hændelser, såsom myokardieinfarkt, er der utilstrækkelige data til at udelukke en lignende risiko for KEVINDOL.
Sygdomme i reproduktive system og bryst: kvindelig infertilitet.
Thorax- og mediastinale lidelser i luftvejene: lungeødem, dyspnø, astma.
Lever- og galdeforstyrrelser: hepatitis, kolestatisk gulsot, leversvigt.
Hud og subkutan væv: angioødem, eksfoliativ dermatitis, øget svedtendens, makulopapulært udslæt, urticaria, kløe, purpura, bulløse reaktioner, herunder Stevens-Johnsons syndrom og toksisk epidermal nekrolyse (meget sjældent).
Muskuloskeletale og bindevævssygdomme: myalgi.
Nyre- og urinlidelser: polyuri, pollakiuri, oliguri, akut nyresvigt, uræmisk-hæmolytisk syndrom, interstitiel nefritis, urinretention, nefrotisk syndrom, flanksmerter (med eller uden hæmaturi, +/- af azotæmi). Som med andre lægemidler, der hæmmer syntese af renal prostaglandiner efter administration af ketorolac kan der forekomme tegn på nedsat nyrefunktion, for eksempel øgede niveauer af kreatinin og kalium.
Generelle lidelser og tilstande på administrationsstedet: asteni, feber, reaktioner på injektionsstedet, ødem, brystsmerter, overdreven tørst.
Diagnostiske tests: øget blødningstid, øget serumurinstof, øget kreatinin, unormale leverfunktionstests.
Laboratorietest
Se afsnittet Erfaring efter markedsføring (bivirkninger).
Indberetning af formodede bivirkninger.
Rapportering af formodede bivirkninger, der opstår efter godkendelse af lægemidlet, er vigtig, da det muliggør løbende overvågning af lægemidlets fordel / risiko -balance. Sundhedspersonale anmodes om at rapportere alle formodede bivirkninger via det nationale rapporteringssystem. "Adresse www. agenziafarmaco.gov.it/it/responsabili.
04.9 Overdosering
Symptomer og tegn
Efter en overdosis af KEVINDOL blev følgende fundet: erosiv gastritis, mavesår, mavesmerter, kvalme, opkastning, hyperventilation og nyrefunktion, som forsvandt ved seponering af lægemidlet.
Gastrointestinal blødning kan forekomme. Sjældent kan hypertension, akut nyresvigt, respirationsdepression og koma forekomme efter indtagelse af NSAID'er.
Anafylaktoide reaktioner er blevet rapporteret ved terapeutisk indtagelse af NSAID'er; dette kan ske som følge af overdosering.
Behandling
Der er ingen specifikke modgift.
I tilfælde af overdosering af NSAID'er bør symptomatisk og understøttende behandling anvendes. I tilfælde af utilsigtet indtagelse skal normale sikkerhedsforanstaltninger tilføjes til dette (fremkaldelse af opkastning, mave -skylning, administration af aktivt kul).
Dialyse eliminerer ikke KEVINDOL væsentligt fra blodbanen.
05.0 FARMAKOLOGISKE EGENSKABER
05.1 Farmakodynamiske egenskaber
Farmakoterapeutisk gruppe: ikke-steroide antiinflammatoriske / antireumatiske; ATC -kode: M01AB15.
Den aktive ingrediens i KEVINDOL er Ketorolac trometamin, et lægemiddel tilhørende klassen af ikke-steroide antiinflammatoriske lægemidler (NSAID'er). Dens aktivitet udføres hovedsageligt ved at hæmme syntesen af prostaglandiner, især PGE2 og PGF2 alfa.
I prækliniske farmakologiske undersøgelser viste det 350 gange mere potent smertestillende aktivitet end aspirin hos mus i den phenylquinon-inducerede smerteinhiberingstest og 800 gange mere potent end rotte-aspirin ved inhibering af fleksionsmerterespons. Tarsus-tibialis af rottepote med induceret arthritis.
Ketorolac viste også antiinflammatorisk (overlegen phenylbutazon) og antipyretisk (overlegen aspirin) aktivitet.
Ketorolac var 37 gange mere aktiv end aspirin til at hæmme kollageninduceret aggregering af humane blodplader.
Ketorolac har ingen virkninger på centralnervesystemet; virkningerne på det kardiovaskulære og respiratoriske system er minimale.
Fra kliniske undersøgelser fremgik det, at den analgetiske aktivitet af ketorolac i en dosis på 10 mg var lig med eller større end aspirin 650 mg, paracetamol 600 og 1000 mg, kombinationen af paracetamol 600 mg og 1000 mg + codein 60 mg; med glafenin 400 mg, med ibuprofen 400 mg, med diclofenac 50 mg.
Ketorolac administreret i.m. ved en dosis på 30 mg blev det fundet i talrige kliniske undersøgelser, der var sammenlignelige med morfin 12 mg og meperidin 100 mg og bedre end morfin 6 mg og meperidin 50 mg.
Ketorolac administreret i.m. ved en dosis på 30 mg viste en længere virkningstid end morfin og meperidin.
Den smertestillende virkning forekommer inden for 1 time efter oral administration, 30 minutter efter i.m. administration og den maksimale smertestillende effekt vises inden for henholdsvis 2-3 timer og 1-2 timer.
For begge formuleringer er den gennemsnitlige varighed af den smertestillende effekt 4-6 timer.
Ketorolac har ingen morfinlignende virkninger, forårsager ikke respirationsdepression, og i forhold til morfin er forekomsten af bivirkninger i centralnervesystemet (døsighed) signifikant lavere.
05.2 Farmakokinetiske egenskaber
Absorption
KEVINDOL absorberes hurtigt og fuldstændigt oralt med en maksimal plasmakoncentration på 0,87 mcg / ml inden for 35 minutter efter administration af 10 mg tabletter og en top på 1,11 mcg / ml inden for 26 minutter efter administration af 10 mg i opløsning.
Tabletter og 2% oral opløsning viste sig at være bioækvivalente med hensyn til AUC og halveringstid.
Efter intramuskulær administration af 30 mg absorberes KEVINDOL på samme måde hurtigt og fuldstændigt med en gennemsnitlig maksimal plasmakoncentration på 2,2 mcg / ml.
Efter intravenøs administration af 30 mg er maksimal plasmakoncentration 5 mcg / ml.
KEVINDOLs farmakokinetik hos mennesker, både efter enkelt og gentagen administration, er lineær; plasma steady state opnås efter en dag for hver 6 timers administration.
Halveringstiden var 5,4 timer efter oral administration og 5,3 timer efter i.m. administration og 5,1 timer efter i.v.
Hos ældre er disse værdier lidt højere: for eksempel 6,2 og 7.
Indtagelse af antacida påvirker ikke absorptionen af ketorolac.
Fordeling
Plasmaproteinbindingen af ketorolac er 99%.
Terapeutiske koncentrationer af digoxin, warfarin, ibuprofen, naproxen, piroxicam, acetaminophen, phenytoin og tolbutamid ændrer ikke proteinbinding af ketorolac.
Distributionsvolumen er 0,11 l / kg.
Metabolisme
Ketorolac metaboliseres i leveren; de vigtigste metaboliske derivater er para-hydroxylerede (12%) og glucuronat (75%) derivater, alle inaktive.
Eliminering
Den vigtigste eliminationsvej for ketorolac og dets metabolitter er via urinen, og resten elimineres i fæces. Nyreclearance for ketorolac er 0,35-0,55 ml / min / kg.
05.3 Prækliniske sikkerhedsdata
Akut forgiftning
LD50 oralt i mus 529 mg / kg (M og F); hos rotter fra 100 til 400 mg / kg (M og F) og hos aber over 200 mg / kg (M og F); via i.p. hos mus 473 mg / kg (M og F), hos rotter fra 100 til 400 mg / kg (M og F).
Toksicitet ved gentagen dosis
Daglig højdosis oral administration hos mus (30 mg / kg i 6 måneder) og aber (9 mg / kg i 12 måneder) viste gastroenteropati (hos mus) og let nefrotoksicitet. I.m. forvaltninger hos kaniner (15 mg / kg i 1 måned) og aber (13,5 mg / kg i 3 måneder) viste en mild inflammatorisk reaktion på injektionsstedet.
IV administration hos kaniner og aber (2,5 mg / kg i 2 uger) tolereredes de godt.
Fostertoksicitet
Undersøgelser af: teratogenese hos rotter (10 mg / kg) og hos kanin (3,6 mg / kg), peri-postnatal (9 mg / kg) og fertilitet (16 mg / kg hun, 9 mg / kg han) hos rotte, viste ikke teratogene virkninger eller ændringer i fertilitet og reproduktionsevne.
Langvarig graviditet og / eller maternel dystoki og efterfølgende perinatal dødelighed blev observeret hos rotter ved højere doser.
Mutagenese, carcinogenese, tolerabilitet
Ketorolac viste sig at være ikke-mutagent, ikke-kræftfremkaldende, fremkaldte ikke sensibilisering hos marsvinet og manglede immunogen aktivitet.
06.0 LÆGEMIDDELOPLYSNINGER
06.1 Hjælpestoffer
KEVINDOL 30 mg injektionsvæske, opløsning: Ethylalkohol, natriumchlorid, vand til injektionsvæsker.
KEVINDOL 20 mg / ml orale dråber, opløsning:
vandfri citronsyre, natriumdihydrogenphosphatdihydrat, methylparahydroxybenzoat, propylparahydroxybenzoat, natriumhydroxid, renset vand.
06.2 Uforenelighed
KEVINDOL er kompatibelt med aminophyllin, xylocain, morfin, meperidin, dopamin, insulin og heparin administreret samtidigt i opløsning indeholdt i en dryppose til iv -administration, men kan ikke blandes med morfin, meperidin, promethazin eller hydroxyzin i en sprøjte.
06.3 Gyldighedsperiode
2 år.
Holdbarhed efter åbning af flasken med oral opløsning dråber:
Holdbarheden efter første åbning af flasken er 6 måneder.
Opbevaringstid efter rekonstituering af injektionsvæsken, opløsningen:
I overensstemmelse med reglerne for god farmaceutisk praksis skal de intravenøse opløsninger tilberedes på tidspunktet for infusionen Den rekonstituerede opløsning skal bruges straks, og eventuelle rester skal kasseres.
06.4 Særlige opbevaringsforhold
Opbevares i den originale emballage for at beskytte produktet mod lys.
06.5 Den umiddelbare emballages art og emballagens indhold
KEVINDOL 30 mg / ml injektionsvæske, opløsning: rav hætteglas af type I; pakke med 3 ampuller på 1 ml
KEVINDOL 20 mg / ml oral dråber opløsning: 10 ml rav type III glasflaske.
06.6 Brugsanvisning og håndtering
Ingen særlige instruktioner.
07.0 INDEHAVER AF MARKEDSFØRINGSTILLADELSE
Så.Se.PHARM S.r.l. Via dei Castelli Romani, 22 - 00040 Pomezia (Rom).
08.0 MARKEDSFØRINGSTILLADELSESNUMMER
KEVINDOL 30 mg / mI injektionsvæske, opløsning - 3 ampuller 1 ml A.I.C. n. 037746017
KEVINDOL 20 mg / ml oral drops opløsning - flaske 10 ml A.I.C. n. 037746029
09.0 DATO FOR FØRSTE TILLADELSE ELLER FORNYELSE AF TILLADELSEN
Første tilladelse: 29. januar 2009
Ubegrænset fornyelse: 29. januar 2014
10.0 DATO FOR REVISION AF TEKSTEN
AIFA -resolution af 18. maj 2015