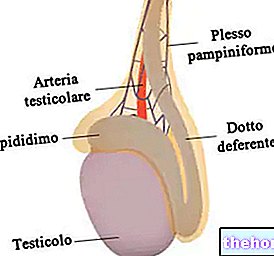
Aktive ingredienser: Oseltamivir
Tamiflu 30 mg hårde kapsler
Tamiflu indlægssedler er tilgængelige til pakningsstørrelser:- Tamiflu 30 mg hårde kapsler
- Tamiflu 45 mg hårde kapsler
- Tamiflu 75 mg hårde kapsler
- Tamiflu 6 mg / ml pulver til oral suspension
- Tamiflu 12 mg / ml pulver til oral suspension
Hvorfor bruges Tamiflu? Hvad er det for?
- Tamiflu bruges til behandling af influenza til voksne, unge, børn og spædbørn (inklusive fuldbårne babyer). Det kan bruges, når du har influenzasymptomer, og influenzavirus cirkulerer i samfundet.
- Tamiflu kan også ordineres til voksne, unge, børn og spædbørn over 1 år fra sag til sag for at forhindre influenza, for eksempel hvis du har været i kontakt med en, der har influenza.
- Tamiflu kan ordineres til voksne, unge, børn og spædbørn (inklusive spædbørn) som forebyggende behandling i særlige tilfælde, for eksempel hvis der er en "global influenzaepidemi (influenzapandemi) og sæsonbetinget influenzavaccine." For at sikre tilstrækkelig beskyttelse.
Tamiflu indeholder oseltamivir, som tilhører en gruppe lægemidler kaldet neuraminidasehæmmere. Disse lægemidler forhindrer spredning af influenzavirus i kroppen og hjælper dermed med at lindre eller forhindre symptomer på infektion forårsaget af influenzavirus.
Influenza er en infektion forårsaget af en virus. Symptomer på influenza omfatter ofte pludselig feber (over 37,8 ° C), hoste, løbende eller tilstoppet næse, hovedpine, muskelsmerter og ekstrem træthed. Disse symptomer kan også skyldes andre infektioner. Den sande infektionsinfluenza opstår kun under årlige udbrud, når influenzavirus spreder sig til lokalsamfundet. Uden for epidemiperioden skyldes influenzalignende symptomer generelt en anden type sygdom.
Kontraindikationer Når Tamiflu ikke bør bruges
Tag ikke Tamiflu
- hvis du er allergisk (overfølsom) over for oseltamivir eller et af de øvrige indholdsstoffer i Tamiflu, der er angivet i afsnit 6.
Kontakt din læge, hvis dette gælder dig. Tag ikke Tamiflu.
Forholdsregler ved brug Det, du skal vide, før du tager Tamiflu
Inden du tager Tamiflu, skal du sørge for, at din læge ved det
- hvis du er allergisk over for anden medicin
- hvis du har en nyresygdom. I dette tilfælde kan det være nødvendigt at justere dosis
- hvis du har en alvorlig sundhedstilstand, som kan kræve øjeblikkelig indlæggelse
- hvis immunsystemet ikke virker
- hvis du har hjertesygdom eller kronisk luftvejssygdom.
Fortæl det straks til din læge under behandling med Tamiflu
- hvis du har bemærket ændringer i adfærd og humør (neuropsykiatriske hændelser), især hos børn og unge.Dette kan være symptomer på sjældne, men alvorlige bivirkninger.
Tamiflu er ikke et influenzaskud
Tamiflu er ikke en vaccine: den behandler infektion eller forhindrer spredning af influenzavirus. En vaccine giver antistoffer mod virussen. Tamiflu ændrer ikke effektiviteten af en influenzavaccine, og din læge kan ordinere begge.
Interaktioner Hvilke lægemidler eller fødevarer kan ændre effekten af Tamiflu
Fortæl det til din læge eller på apoteket, hvis du tager anden medicin eller har brugt det for nylig, også uden recept.
Følgende medicin er særlig vigtig:
- chlorpropamid (bruges til behandling af diabetes)
- methotrexat (bruges til behandling af f.eks. "reumatoid arthritis)
- phenylbutazon (bruges til behandling af smerter og betændelse)
- probenecid (bruges til behandling af gigt).
Advarsler Det er vigtigt at vide, at:
Graviditet og amning
Fortæl det til din læge, hvis du er gravid, hvis du tror, du er gravid, eller hvis du prøver at blive gravid, så din læge kan beslutte, om Tamiflu er egnet til dig.
Virkninger på spædbørn, der ammes, er ukendte. Fortæl det til din læge, hvis du ammer, så han kan afgøre, om Tamiflu er egnet til dig.
Spørg din læge eller apotek til råds, før du tager denne medicin.
Kørsel og brug af maskiner
Tamiflu påvirker ikke din evne til at føre motorkøretøj eller betjene maskiner.
Dosis, metode og administrationstidspunkt Sådan bruges Tamiflu: Dosering
Tag denne medicin nøjagtigt efter lægens anvisning. Hvis du er i tvivl, skal du kontakte din læge eller apotek.
Tag Tamiflu så hurtigt som muligt, helst inden for to dage efter starten af influenzasymptomer.
Anbefalede doser
Til behandling af influenza skal du tage to doser om dagen.Det er normalt praktisk at tage en dosis om morgenen og en om aftenen. Det er vigtigt, at du gennemfører hele 5 dages cyklus, selvom du hurtigt begynder at føle dig bedre.
For at forebygge influenza eller efter kontakt med en inficeret person, tag en dosis om dagen i 10 dage.Det er bedst at tage denne dosis om morgenen med morgenmad.
I særlige situationer, såsom udbredt influenza eller for patienter med svagt immunsystem, vil behandlingen fortsætte i op til 6 eller 12 uger.
Den anbefalede dosis afhænger af patientens kropsvægt. Du bør bruge den mængde kapsler eller oral suspension, som din læge har ordineret.
Voksne og unge fra 13 år
75 mg kan bestå af en 30 mg kapsel plus en 45 mg kapsel.
Børn fra 1 til 12 år
75 mg kan bestå af en 30 mg kapsel plus en 45 mg kapsel.
Spædbørn under 1 år (0 - 12 måneder)
Administration af Tamiflu til spædbørn under 1 år til forebyggelse af influenza i tilfælde af pandemisk influenza bør baseres på lægens vurdering efter at have overvejet forholdet mellem den potentielle fordel og den potentielle risiko for barnet.
mg pr. kg = mg for hvert kilo af barnets kropsvægt. For eksempel: hvis en 6 måneder gammel baby vejer 8 kg, er dosen 8 kg x 3 mg pr. Kg = 24 mg
Indgivelsesmåde
Synk kapslerne hele med vand. Kapslerne må ikke brydes eller tygges.
Tamiflu kan tages med eller uden mad, selvom at tage det med mad kan reducere chancen for at føle eller blive syg (kvalme eller opkastning).
Folk, der har svært ved at sluge kapslerne, kan bruge det flydende præparat, Tamiflu oral suspension. Hvis du har brug for Tamiflu oral suspension, men den ikke er tilgængelig på apoteket, kan du lave Tamiflu -opløsningen fra kapslerne. For instruktioner, se siden Forberedelse af Tamiflu i flydende form derhjemme.
Overdosering Hvad skal man gøre, hvis man har taget for meget Tamiflu
Hvis du har taget for meget Tamiflu
Stop med at tage Tamiflu og kontakt straks din læge eller apoteket. I de fleste tilfælde af overdosering rapporterede folk ikke om nogen bivirkninger. Da der blev rapporteret bivirkninger, lignede de dem, der blev set med normale doser som angivet. I afsnit 4.
Tilfælde af overdosering er blevet rapporteret hyppigere, da Tamiflu blev administreret til børn end voksne og unge. Der skal udvises forsigtighed ved forberedelse af Tamiflu -opløsning til børn og ved administration af Tamiflu -kapsler eller Tamiflu -suspension til børn.
Hvis du har glemt at tage Tamiflu
Tag ikke en dobbeltdosis som erstatning for en glemt kapsel.
Hvis du holder op med at tage Tamiflu
Der er ingen bivirkninger, når Tamiflu -administrationen stoppes. Hvis Tamiflu stoppes tidligere, end din læge har fortalt dig, kan dine influenzasymptomer vende tilbage. Afslut altid den behandling, som din læge har ordineret til dig.
Spørg din læge eller apotek, hvis du har yderligere spørgsmål om brugen af dette lægemiddel.
Bivirkninger Hvad er bivirkningerne af Tamiflu
Ligesom al anden medicin kan denne medicin forårsage bivirkninger, men ikke alle får bivirkninger. Mange af de bivirkninger, der er anført nedenfor, kan også skyldes influenza.
Følgende alvorlige bivirkninger er sjældent blevet rapporteret siden oseltamivir kom på markedet:
- Anafylaktiske eller anafylaktoide reaktioner: alvorlige allergiske reaktioner med hævelse af ansigt og hud, kløende hududslæt, lavt blodtryk og åndedrætsbesvær;
- Leversygdomme (fulminant hepatitis, leverfunktionsforstyrrelser og gulsot): gulfarvning af huden og det hvide i øjet, ændring i afføringens farve, ændringer i adfærd;
- Angioneurotisk ødem: pludselig indtræder alvorlig hævelse af huden, især omkring hoved og hals, herunder øjne og tunge, med vejrtrækningsbesvær
- Stevens-Johnsons syndrom og toksisk epidermal nekrolyse: kompliceret allergisk reaktion, som kan føre til døden, manifesteret af alvorlig betændelse i huden og indre slimhinder, der i første omgang ledsages af feber, ondt i halsen, følelse af træthed og deraf følgende udslæt, blærer, skrælning af hud med store områder med dermoepidermal løsrivelse, mulig vejrtrækningsbesvær og lavt blodtryk;
- Mave -tarmblødning: langvarig blødning fra tyktarmen eller udvisning af blod fra munden;
- Neuro-psykiatriske lidelser, som beskrevet nedenfor.
Hvis du opdager nogen af disse symptomer, skal du søge øjeblikkelig lægehjælp.
De hyppigst rapporterede (meget almindelige og almindelige) bivirkninger ved Tamiflu er kvalme eller utilpashed (kvalme, opkastning), mavesmerter, mavebesvær, hovedpine og smerter. Disse bivirkninger forekommer for det meste efter den første dosis af lægemidlet og forsvinder generelt med fortsat behandling. Hyppigheden af disse virkninger reduceres, hvis lægemidlet tages sammen med mad.
Sjældne, men alvorlige virkninger: søg straks lægehjælp
(kan ramme op til 1 ud af 1.000 mennesker)
Sjældne begivenheder inklusive
- kramper og delirium inklusive ændret bevidsthedsniveau
- forvirring, unormal adfærd
- delirium, hallucinationer, uro, angst, mareridt
Disse hændelser blev hovedsageligt rapporteret blandt børn og unge og kom ofte pludseligt og blev hurtigt løst. Få tilfælde er degenereret til selvskade (instinkt til at skade sig selv), hvilket i nogle tilfælde har ført til døden. Sådanne neuropsykiatriske hændelser er også blevet rapporteret hos patienter med influenza, som ikke havde taget Tamiflu.
- Patienter, især børn og unge, bør overvåges nøje for de adfærdsmæssige ændringer, der er beskrevet ovenfor.
Hvis du bemærker nogle af disse symptomer, især hos yngre patienter, skal du søge øjeblikkelig lægehjælp.
Voksne og unge fra 13 år
Meget almindelige bivirkninger:
(kan ramme mere end 1 ud af 10 personer)
- Hovedpine
- Kvalme.
Almindelige bivirkninger
(kan ramme op til 1 ud af 10 personer)
- Bronkitis
- Forkølelsessår
- Hoste
- Svimmelhed
- Feber
- Smerte
- Smerter i lemmerne
- En løbende næse
- Søvnforstyrrelser
- Ondt i halsen
- Mavepine
- Træthed
- Følelse af fylde i den øvre del af maven
- Øvre luftvejsinfektioner (betændelse i næse, hals og næsepassager)
- Dårlig mave
- Han trak sig tilbage.
Ikke almindelige bivirkninger
(Kan ramme op til 1 ud af 100 mennesker)
- Allergiske reaktioner
- Ændret bevidsthedsniveau
- Kramper
- Hjerterytmeabnormalitet
- Milde til svære leverfunktionsabnormiteter
- Hudreaktioner (betændelse i huden, rødt og kløende udslæt, afskalning af huden).
Sjældne bivirkninger:
(kan ramme op til 1 ud af 1.000 mennesker)
- Trombocytopeni (lavt antal blodplader)
- synsforstyrrelser.
Børn mellem 1 og 12 år
Meget almindelige bivirkninger
(kan ramme mere end 1 ud af 10 personer)
- Hoste
- Næsetæthed
- Han trak sig tilbage.
Almindelige bivirkninger
(kan ramme op til 1 ud af 10 personer)
- Konjunktivitis (røde øjne og øjeudledning eller smerte)
- Ørebetændelse og andre øreforstyrrelser
- Hovedpine
- Kvalme
- En løbende næse
- Mavepine
- Følelse af fylde i den øvre del af maven
- Dårlig mave.
Ikke almindelige bivirkninger
(kan ramme op til 1 ud af 100 mennesker)
- Betændelse i huden
- Forstyrrelser i trommehinden.
Spædbørn under 1 år
De rapporterede bivirkninger hos spædbørn i alderen 0 til 12 måneder ligner for det meste bivirkningerne for ældre børn (1 år og ældre). Diarré og bleudslæt er også blevet rapporteret.
Fortæl det til din læge eller apoteket, hvis nogen af bivirkningerne bliver alvorlige, eller hvis du bemærker nogen bivirkninger, der ikke er angivet i denne indlægsseddel. Desuden,
- hvis du eller barnet ofte bliver sygt, eller
- hvis influenzasymptomerne bliver værre, eller hvis feberen vedvarer
Fortæl det til din læge så hurtigt som muligt.
Indberetning af bivirkninger
Tal med din læge, hvis du får bivirkninger, herunder mulige bivirkninger, som ikke er nævnt i denne indlægsseddel. Du kan også indberette bivirkninger direkte via det nationale rapporteringssystem anført i tillæg V. Ved at rapportere bivirkninger kan du hjælpe med at give mere information om sikkerheden ved dette lægemiddel.
Udløb og opbevaring
Opbevares utilgængeligt for børn.
Brug ikke dette lægemiddel efter den udløbsdato, der står på kartonen og blisteren efter EXP / EXP. Udløbsdatoen refererer til den sidste dag i måneden.
Må ikke opbevares over 25 ° C.
Smid ikke medicin via spildevand eller husholdningsaffald. Spørg din apotek om, hvordan du skal smide medicin, du ikke længere bruger. Dette vil hjælpe med at beskytte miljøet.
Tamiflu indeholder
- Hver hård kapsel indeholder ækvivalent med 30 mg oseltamivir.
- Hjælpestoffer er:
kapselindhold: forgelatiniseret stivelse, talkum, povidon, croscarmellosenatrium og natriumstearylfumarat
kapselskal: gelatine, gult jernoxid (E172), rødt jernoxid (E172) og titandioxid (E171)
trykfarve: shellak (E904), titandioxid (E171) og FD og C Blue 2 (indigokarmin E132).
Beskrivelse af Tamiflu udseende og pakningens indhold
Den 30 mg hårde kapsel består af en lysegul uigennemsigtig krop mærket "ROCHE" og en lysegul uigennemsigtig hætte mærket "30 mg". Inskriptionerne er i blå.
Tamiflu 30 mg hårde kapsler fås i blisterpakninger med 10 stk.
Information til brugeren
For mennesker, der har svært ved at sluge kapsler, herunder helt små børn, er det flydende præparat, Tamiflu oral suspension, tilgængeligt.
Hvis du har brug for det flydende præparat, men det ikke er tilgængeligt, kan du bruge en oral suspension fremstillet på et apotek fra Tamiflu kapsler (se Information til sundhedspersonale). Flydende apoteksforberedelse er den foretrukne mulighed.
Hvis det flydende præparat fremstillet på apoteket heller ikke er tilgængeligt, kan du tilberede Tamiflu i flydende form derhjemme fra disse kapsler.
Dosen er den samme til behandling og forebyggelse af influenza.Forskellen er i hyppigheden af administration.
Fremstilling af Tamiflu i flydende form derhjemme
- Hvis du har de korrekte kapsler til rådighed, for den krævede styrke (en dosis på 30 mg eller 60 mg), skal du åbne kapslen og blande indholdet med en teskefuld (eller mindre) af en passende sød mad. Denne procedure er normalt egnet til børn over 1 år. Se toppen af vejledningen.
- Hvis du har brug for en lavere dosis, kræver tilberedning af Tamiflu i flydende form fra kapsler yderligere trin. Denne procedure er velegnet til yngre børn og spædbørn, som normalt har brug for mindre end 30 mg Tamiflu. Se bunden af vejledningen.
Børn fra 1 til 12 år
For at forberede en dosis på 30 mg eller 60 mg skal du:
- En eller to kapsler Tamiflu på 30 mg
- Skarp saks
- En lille skål
- Teske (5 ml tsk)
- Vandfald
- En sød mad til at skjule pulverets bitre smag.
For eksempel: chokolade eller kirsebærsirup og desserter, f.eks. Karamel eller karamelsauce. Eller du kan lave lidt sukkervand ved at blande en teskefuld vand med tre fjerdedele (3/4) af en teskefuld sukker.
Trin 1: Kontroller, at dosis er korrekt
For at bestemme den korrekte mængde medicin, du skal bruge, skal du kigge efter patientens vægt i venstre kolonne i tabellen.
Se i den højre kolonne for antallet af kapsler, der skal administreres til patienten for hver dosis. Beløbet er det samme for både behandling og forebyggelse af influenza.
30 mg dosis Roche 30 mg
Dosis på 60 mg Roche 30 mg Roche 30 mg
Du bør kun bruge 30 mg kapslerne til doserne 30 mg og 60 mg. Forsøg ikke at forberede en dosis på 45 mg eller 75 mg ved hjælp af indholdet i 30 mg kapslerne. Brug i stedet kapslerne med den passende styrke.
Trin 2: Hæld alt pulveret i en skål
Hold 30 mg kapslen lodret over en skål og skær forsigtigt den afrundede ende af med en saks.
Hæld alt pulveret i skålen.
Åbn en anden kapsel til en dosis på 60 mg. Hæld alt pulveret i skålen. Vær forsigtig med støvet, da det kan irritere hud og øjne.
Trin 3: Blødgør pulveret og administrer det til patienten
Tilsæt en lille mængde - ikke mere end en teskefuld - af den sødede mad i pulverform til skålen.
Dette skjuler den bitre smag af Tamiflu pulver.
Bland blandingen godt.
Giv straks patienten hele skålens indhold.
Hvis noget af blandingen forbliver i skålen, skal du skylle skålen med en lille mængde vand og give alt indholdet til patienten at drikke.
Gentag denne procedure hver gang du skal administrere lægemidlet.
Børn under 1 år
For at forberede en mindre enkeltdosis skal du bruge:
- En 30 mg Tamiflu kapsel
- Skarp saks
- To små skåle (brug et andet par skåle til hvert barn)
- En stor oral dispenser til dosering af vand - en 5 eller 10 ml dispenser
- En lille oral dispenser, der tillader måling af 0,1 ml, for at give dosis
- Teske (5 ml tsk)
- Vandfald
- Søde fødevarer til at skjule den bitre smag af Tamiflu.
For eksempel: chokolade eller kirsebærsirup og desserter, f.eks. Karamel eller karamelsauce.
Eller du kan lave lidt sukkervand ved at blande en teskefuld vand med tre fjerdedele (3/4) af en teskefuld græskar.
Trin 1: Hæld alt pulveret i en skål
Hold en 30 mg kapsel lodret over en af skålene og skær forsigtigt den afrundede ende af med en saks Pas på for støv: det kan irritere hud og øjne.
Hæld alt pulveret i skålen, uanset hvilken dosis du forbereder.
Mængden er den samme, uanset om du behandler eller forebygger influenza.
Trin 2: Tilsæt vand for at fortynde medicinen
Brug den større dispenser til at trække 5 ml vand.
Tilsæt vandet til pulveret i skålen.
Rør blandingen med en teske i cirka 2 minutter.
Bare rolig, hvis alt støv ikke opløses. Det ikke-opløselige pulver består kun af hjælpestoffer.
Trin 3: Vælg den korrekte mængde baseret på barnets vægt
Se efter vægten i venstre side af bordet.
Kolonnen til højre i tabellen viser mængden af flydende blanding, der skal trækkes med en oral sprøjte.
Spædbørn under 1 år (inklusive fuldbårne spædbørn)
Trin 4: Aspirer den flydende blanding
Sørg for at have den rigtige størrelse dispenser (oral sprøjte)
Træk den korrekte mængde flydende blanding fra den første skål.
Aspirér opad og pas på ikke at inkludere luftbobler.
Hæld forsigtigt den korrekte dosis i den anden skål.
Trin 5: Sød og giv det til babyen
Tilsæt en lille mængde - ikke mere end en teskefuld - af den sødede mad til den anden skål.
Dette skjuler den bitre smag af Tamiflu -suspensionen.
Bland den sødede mad og Tamiflu -væsken godt.
Giv straks barnet hele indholdet i den anden skål (mad sødet med Tamiflu flydende blanding).
Hvis der er rester tilbage i den anden skål, skal du skylle skålen med en lille mængde vand og give barnet alt indholdet at drikke. For børn, der ikke kan drikke fra skålen, skal du bruge en teske eller flaske til at give barnet resterende flydende blanding.
Giv barnet noget at drikke.
Smid ubrugt væske tilbage i den første skål.
Gentag dette trin hver gang du skal administrere lægemidlet.
Indlægsseddel: AIFA (Italian Medicines Agency). Indhold offentliggjort i januar 2016. De foreliggende oplysninger er muligvis ikke opdaterede.
For at få adgang til den mest opdaterede version er det tilrådeligt at få adgang til webstedet AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttige oplysninger.
01.0 LÆGEMIDLETS NAVN
TAMIFLU 30 MG Hårde kapsler
02.0 KVALITATIV OG KVANTITATIV SAMMENSÆTNING
Hver hård kapsel indeholder oseltamivirphosphat svarende til 30 mg oseltamivir.
Den fulde liste over hjælpestoffer findes i afsnit 6.1.
03.0 LÆGEMIDDELFORM
Hård kapsel (kapsel).
Den hårde kapsel består af en lysegul uigennemsigtig krop mærket "ROCHE" og en lysegul uigennemsigtig hætte mærket "30 mg". Inskriptionerne er i blå.
04.0 KLINISKE OPLYSNINGER
04.1 Terapeutiske indikationer
Behandling af influenza
Tamiflu er indiceret til voksne og børn, herunder fuldbårne spædbørn, der udviser typiske influenzasymptomer, når influenzavirus cirkulerer i samfundet. Behandlingen var effektiv, da den startede inden for to dage efter de første symptomer viste sig.
Forebyggelse af influenza
• Forebyggelse efter eksponering hos personer 1 år eller ældre efter kontakt med et klinisk diagnosticeret tilfælde af influenza, når influenzaviruset cirkulerer i samfundet.
• Den korrekte anvendelse af Tamiflu til forebyggelse af influenza bør defineres fra sag til sag baseret på omstændighederne og befolkningen, der har behov for beskyttelse. Under ekstraordinære forhold (f.eks. I tilfælde af uoverensstemmelse mellem den cirkulerende virale stamme og den, der findes i vaccinen, og i nærvær af en pandemi), kan sæsonforebyggelse overvejes hos personer i alderen 1 år eller ældre.
• Tamiflu er indiceret til forebyggelse af influenza efter eksponering hos spædbørn under 1 år under en influenzapandemi (se afsnit 5.2).
Tamiflu er ikke en erstatning for influenzaskuddet.
Anvendelse af antivirale midler til behandling og forebyggelse af influenza bør være baseret på officielle anbefalinger. Beslutninger vedrørende brug af oseltamivir til behandling og profylakse skal tage højde for, hvad man ved om egenskaberne ved cirkulerende influenzavirus, de tilgængelige oplysninger om lægemiddelmodtagelighedsmønstre for hver sæson og sygdommens virkning i forskellige områder. Geografiske områder og i forskellige patientpopulationer (se pkt.5.1).
04.2 Dosering og indgivelsesmåde
Dosering
Tamiflu hårde kapsler og Tamiflu oral suspension er bioækvivalente formuleringer. Doser på 75 mg kan administreres på følgende måder:
• med en 75 mg kapsel eller
• med en 30 mg kapsel plus en 45 mg kapsel eller
• med en dosis på 30 mg oral suspension plus en dosis på 45 mg oral suspension.
Tamiflu pulver til oral suspension (6 mg / ml) klar til brug er den foretrukne formulering til pædiatriske og voksne patienter, der har svært ved at synke kapsler, eller hvor lavere doser er påkrævet.
Voksne og unge fra 13 år
Behandling : Den anbefalede orale dosis af oseltamivir er 75 mg to gange dagligt i 5 dage for unge (13 til 17 år) og voksne.
Behandlingen bør startes hurtigst muligt inden for de første to dage efter begyndelsen af influenzasymptomer.
Post-eksponering forebyggelse : Den anbefalede dosis til forebyggelse af influenza efter tæt kontakt med et inficeret individ er 75 mg oseltamivir én gang dagligt i 10 dage for unge (13 til 17 år) og voksne.
Behandlingen skal starte så hurtigt som muligt inden for to dage efter udsættelse for et inficeret individ.
Forebyggelse under en "samfundsinfluenzaepidemi:" Den anbefalede dosis til forebyggelse af influenza under et samfundsudbrud er 75 mg oseltamivir én gang dagligt i op til 6 uger.
Pædiatrisk population
Børn mellem 1 og 12 år
Tamiflu 30 mg, 45 mg og 75 mg kapsler og oral suspension er tilgængelige for børn i alderen 1 år og ældre.
Behandling : Følgende vægtrelaterede doseringsregimer anbefales til behandling af børn på 1 år og ældre:
Behandlingen bør startes hurtigst muligt inden for de første to dage efter begyndelsen af influenzasymptomer.
Post-eksponering forebyggelse : Den anbefalede dosis Tamiflu til forebyggelse efter eksponering er:
Forebyggelse under en "samfundsinfluenza" -epidemi: forebyggelse under influenzaudbrud er ikke undersøgt hos børn under 12 år.
Spædbørn i alderen 0 til 12 måneder
Behandling : Den anbefalede dosis til spædbørn i alderen 0 til 12 måneder er 3 mg / kg to gange dagligt. Dette er baseret på farmakokinetiske data og sikkerhedsdata, der indikerer, at denne dosis til spædbørn i alderen 0 til 12 måneder producerer plasmakoncentrationer af lægemiddel og aktiv metabolit, der forventes at være klinisk effektive, med en sikkerhedsprofil, der kan sammenlignes med den, der observeres hos ældre børn og voksne (se pkt. 5.2). Følgende doseringsregime anbefales til behandling af spædbørn i alderen 0 til 12 måneder:
* Denne tabel er ikke beregnet til at omfatte enhver mulig kropsvægt af denne population. For alle patienter under 1 år skal dosis på 3 mg / kg anvendes uanset patientens vægt.
Behandlingen bør startes hurtigst muligt inden for de første to dage efter begyndelsen af influenzasymptomer.
Denne doseringsanbefaling er ikke gældende for for tidligt fødte babyer, det vil sige dem med en post-befrugtningsalder på under 36 uger. Der er ikke tilstrækkelige data til rådighed for disse patienter, hos hvem en anden dosis kan være nødvendig på grund af umodenhed af fysiologiske funktioner.
Post-eksponering forebyggelse : Den anbefalede dosis til influenzapandemiprofylakse hos spædbørn under 1 år er halvdelen af den daglige behandlingsdosis. Dette er baseret på kliniske data fra børn på 1 år og ældre og voksne, der viser, at en profylaktisk dosis svarende til halvdelen af den daglige behandlingsdosis er klinisk effektiv til forebyggelse af influenza. Følgende anbefales: Aldersrelateret doseringsregime til profylakse af spædbørn i alderen 0-12 måneder:
Denne doseringsanbefaling er ikke gældende for for tidligt fødte babyer, det vil sige dem med en post-befrugtningsalder på under 36 uger. Der er ikke tilstrækkelige data til rådighed for disse patienter, hos hvem en anden dosis kan være nødvendig på grund af umodenhed af fysiologiske funktioner.
Forebyggelse under en "samfundsinfluenzaepidemi:" forebyggelse under et influenzaudbrud er ikke undersøgt hos børn i alderen 0 til 12 måneder.
For instruktioner om fremstilling af den ekstemporære formulering, se afsnit 6.6.
Særlige populationer
Leverinsufficiens
Ingen dosisjustering er nødvendig for patienter med nedsat leverfunktion, hverken til behandling eller forebyggelse. Der er ikke udført undersøgelser hos pædiatriske patienter med nedsat leverfunktion.
Nyresvigt
Behandling af influenza : Dosisændring anbefales til voksne og unge (13 til 17 år) med moderat eller svært nedsat nyrefunktion. Anbefalede doser er detaljeret i nedenstående tabel.
* Data fra undersøgelser hos patienter, der gennemgår kontinuerlig ambulant peritonealdialyse (CAPD); ved anvendelse af automatiseret peritonealdialyse (APD) er en højere clearance af oseltamivircarboxylat mulig. Hvis nefrologen finder det nødvendigt, kan behandlingsformen ændres fra APD til CAPD.
Forebyggelse af influenza : Dosisændring anbefales til voksne og unge (13 til 17 år) med moderat eller svært nedsat nyrefunktion som beskrevet i nedenstående tabel.
* Data fra undersøgelser hos patienter, der gennemgår kontinuerlig ambulant peritonealdialyse (CAPD); ved anvendelse af automatiseret peritonealdialyse (APD) er en højere clearance af oseltamivircarboxylat mulig. Hvis nefrologen finder det nødvendigt, kan behandlingsformen ændres fra APD til CAPD.
Der er utilstrækkelige kliniske data om spædbørn og børn (12 år og yngre) med nedsat nyrefunktion til at kunne fremsætte doseringsanbefalinger.
Ældre borgere
Ingen dosisjustering er nødvendig, medmindre der er tegn på moderat eller svær nyreinsufficiens.
Immunkompromitterede patienter
En længere varighed af sæsonprofylakse op til 12 uger hos immunkompromitterede patienter er blevet evalueret (se pkt. 4.4, 4.8 og 5.1).
Indgivelsesmåde
Oral brug.
Patienter, der ikke er i stand til at sluge kapsler, kan tage passende doser af Tamiflu oral suspension.
04.3 Kontraindikationer
Overfølsomhed over for det aktive stof eller over for et eller flere af hjælpestofferne anført i pkt.6.1.
04.4 Særlige advarsler og passende forholdsregler ved brug
Oseltamivir er kun effektivt mod sygdomme forårsaget af influenzavirus Der er ingen tegn på oseltamivirs effekt ved sygdomme forårsaget af andre midler end influenzavirus (se afsnit 5.1).
Tamiflu er ikke en erstatning for influenzaskuddet. Anvendelsen af Tamiflu bør ikke ændre individers vurdering af den årlige influenzavaccination Beskyttelse mod influenza forbliver kun, så længe Tamiflu administreres. Tamiflu bør kun bruges til behandling og forebyggelse af influenza, når pålidelige epidemiologiske data indikerer, at influenzaviruset cirkulerer i samfundet.
Modtagelighed for cirkulerende influenzavirusstammer over for oseltamivir har vist sig at være meget variabel (se afsnit 5.1). Derfor bør ordinerende læger overveje de seneste tilgængelige oplysninger om oseltamivir -modtagelighedsmønstre for cirkulerende vira på det tidspunkt. af Tamiflu.
Samtidig alvorlig medicinsk tilstand
Der foreligger ingen oplysninger om sikkerhed og virkning af oseltamivir hos patienter med en medicinsk tilstand, der er alvorlig nok eller ustabil til at anses for at have en overhængende risiko for hospitalsindlæggelse.
Immunkompromitterede patienter
Oseltamivirs effekt til både behandling og profylakse af influenza er ikke klart fastslået hos immunkompromitterede patienter (se pkt.5.1).
Hjertesygdom / lungesygdom
Oseltamivirs effekt ved behandling af personer med kronisk hjerte- og / eller lungesygdom er ikke klarlagt. Der blev ikke observeret forskel i forekomsten af komplikationer mellem behandlingsgruppen og placebogruppen i denne patientpopulation (se pkt. 5.1).
Pædiatrisk population
Der er i øjeblikket ingen data til rådighed for at tillade en dosisanbefaling til premature spædbørn (alder efter befrugtning
Alvorlig nyreinsufficiens
Dosisændring anbefales til både behandling og forebyggelse hos unge (13 til 17 år) og hos voksne med svært nedsat nyrefunktion. Utilstrækkelige kliniske data for spædbørn og børn (1 år og ældre) med nedsat nyrefunktion er tilgængelige til at fremsætte anbefalinger til dosering (se pkt. 4.2 og 5.2).
Neuropsykiatriske hændelser
Neuropsykiatriske hændelser er blevet rapporteret under behandling med Tamiflu hos patienter med influenza, især hos børn og unge. Disse hændelser forekom også hos influenzapatienter, der ikke blev behandlet med oseltamivir. Patienter bør overvåges nøje for humørsvingninger, og fordele og risici ved fortsat behandling skal vejes omhyggeligt for hver patient (se pkt. 4.8).
04.5 Interaktioner med andre lægemidler og andre former for interaktion
Oseltamivirs farmakokinetiske egenskaber, såsom lav proteinbinding og metabolisme uafhængigt af CYP450 og glucuronidasesystemer (se pkt. 5.2), indikerer, at klinisk signifikante lægemiddelinteraktioner via disse mekanismer er usandsynlige.
Probenecid
Ingen dosisjustering er nødvendig under samtidig administration af probenecid til patienter med normal nyrefunktion. Samtidig administration af probenecid, en potent hæmmer af anionvejen til renal tubulær sekretion, øger eksponeringen for den aktive metabolit af oseltamivir cirka 2 gange.
Amoxicillin
Oseltamivir har ingen kinetiske interaktioner med amoxicillin, som elimineres ad samme vej, hvilket tyder på, at oseltamivirs interaktion med denne rute er svag.
Renal eliminering
Klinisk signifikante interaktioner mellem lægemidler, der konkurrerer om renal tubulær sekretion, er usandsynlige på grund af den kendte sikkerhedsmargen for de fleste af disse stoffer på grund af elimineringskarakteristika for den aktive metabolit (glomerulær filtrering og anionisk tubulær sekretion) og evnen til at udskille. bør udøves, når oseltamivir administreres til personer, der tager molekyler med et snævert terapeutisk område udskilt ad samme vej (f.eks. chlorpropamid, methotrexat, phenylbutazon).
Yderligere Information
Der blev ikke observeret nogen farmakokinetiske interaktioner mellem oseltamivir eller dets vigtigste metabolit, når de blev administreret samtidigt med paracetamol, acetylsalicylsyre, cimetidin, antacida (magnesium og aluminiumhydroxider og calciumcarbonater), rimantadin eller warfarin (hos stabile patienter med warfarin og uden påvirkning).
04.6 Graviditet og amning
Graviditet
Selvom der ikke er udført kontrollerede kliniske undersøgelser af brugen af oseltamivir til gravide, er der data om brug under graviditet fra post-marketing og observationsstudier (se pkt. 5.1 "Behandling af influenza hos gravide"; for data om eksponering hos gravide kvinder se afsnit 5.2).
Disse data, når de kombineres med dyreforsøg, indikerer ikke direkte eller indirekte skadelige virkninger med hensyn til graviditet, embryonal / føtal eller postnatal udvikling (se pkt. 5.3). Gravide kvinder kan behandles med Tamiflu efter at have overvejet de tilgængelige sikkerhedsoplysninger, patogeniciteten af den cirkulerende influenzavirusstamme og den gravide kvindes underliggende tilstand.
Fodringstid
Hos diegivende hunrotter udskilles oseltamivir og den aktive metabolit i modermælk. Der er meget begrænset information tilgængelig om spædbørn, der ammes af mødre, der har taget oseltamivir, og om udskillelse af oseltamivir i modermælk.De begrænsede tilgængelige data viste, at oseltamivir og den aktive metabolit blev påvist i modermælk, men niveauerne var lave nok til at resultere i en subterapeutisk dosis hos spædbarnet. Under hensyntagen til disse oplysninger, patogeniciteten af den cirkulerende stamme af influenzavirus og den underliggende tilstand hos den ammende kvinde, kan administration af oseltamivir overvejes, hvis der er klare potentielle fordele for ammende mødre.
Fertilitet
Baseret på prækliniske data var der ingen tegn på effekter af Tamiflu på mandlig eller kvindelig fertilitet (se pkt. 5.3).
04.7 Virkninger på evnen til at føre motorkøretøj og betjene maskiner
Tamiflu påvirker ikke evnen til at føre motorkøretøj eller betjene maskiner.
04.8 Bivirkninger
Resumé af sikkerhedsprofilen
Den samlede sikkerhedsprofil for Tamiflu er baseret på data fra 6049 voksne / unge patienter og 1473 pædiatriske patienter behandlet med Tamiflu eller placebo for influenza, og på data fra 3990 voksne / unge patienter og 253 pædiatriske patienter. Behandlet med Tamiflu eller placebo / ingen behandling for influenzaprofylakse i kliniske forsøg. Desuden modtog 475 immunsupprimerede patienter (heraf 18 børn, af disse 10 behandlet med Tamiflu og 8 med placebo) Tamiflu eller placebo til influenzaprofylakse.
Hos voksne / unge var de hyppigst rapporterede bivirkninger kvalme og opkastning i behandlingsstudierne og kvalme i forebyggelsesundersøgelserne. De fleste af disse bivirkninger blev rapporteret ved en enkelt lejlighed på den første eller anden behandlingsdag og forsvandt spontant inden for 1 eller 2 dage. Hos børn var den hyppigst rapporterede bivirkning opkastning. For de fleste patienter førte forekomsten af disse bivirkninger ikke til afbrydelse af behandlingen med Tamiflu.
Følgende alvorlige bivirkninger er sjældent blevet rapporteret siden oseltamivir blev markedsført: anafylaktiske eller anafylaktoide reaktioner, leversygdom (fulminant hepatitis, leverfunktionsforstyrrelser og gulsot), angioneurotisk ødem, Stevens-Johnsons syndrom og toksisk epidermal nekrolyse, gastrointestinal blødning og neuropsykiatriske lidelser ( for neuropsykiatriske lidelser, se pkt. 4.4).
Tabelliste over bivirkninger
Bivirkninger anført i nedenstående tabel falder ind i følgende frekvenskategorier: meget almindelig (≥ 1/10), almindelig (fra ≥ 1/100 til), ualmindelig (fra ≥ 1/1.000 til ), sjælden (fra ≥ 1/10.000 til ) og meget sjælden (). Bivirkninger blev placeret i den relevante kategori i tabellerne baseret på den samlede dataanalyse udført på kliniske forsøg.
Behandling og forebyggelse af influenza hos voksne og unge:
I behandlings- og forebyggelsesundersøgelser hos voksne / unge er bivirkninger rapporteret hyppigst med den anbefalede dosis (75 mg to gange dagligt i 5 dages behandling og 75 mg én gang dagligt i op til 6 uger til profylakse) anført i tabel 1.
Sikkerhedsprofilen rapporteret hos forsøgspersoner, der blev behandlet med den anbefalede dosis Tamiflu til profylakse (75 mg én gang dagligt i op til 6 uger), lignede kvalitativt den, der blev observeret i behandlingsstudierne, på trods af profylakseundersøgelserne. en længere periode.
Tabel 1 Bivirkninger i studier med Tamiflu til behandling og forebyggelse af influenza hos voksne og unge eller fra rapporter efter markedsføring
Behandling og forebyggelse af influenza hos børn:
I alt 1473 børn (inklusive raske børn i alderen 1-12 år og astmatiske børn i alderen 6-12 år) blev indskrevet i kliniske forsøg med oseltamivir administreret til behandling af influenza. Heraf blev 851 børn behandlet med oseltamivir suspension. I alt af 158 børn fik den anbefalede dosis Tamiflu en gang dagligt i en familie-eftereksponeringsprofylakseundersøgelse (n = 99), i en sæsonbestemt undersøgelse af 6-ugers profylakse (n = 49) og i et 12-ugers sæsonbestemt profylakseundersøgelse i immunkompromitterede pædiatriske forsøgspersoner (n = 10).
Tabel 2 viser de hyppigst rapporterede bivirkninger i kliniske forsøg i den pædiatriske population.
Tabel 2 Bivirkninger i undersøgelser med Tamiflu til behandling og forebyggelse af influenza hos børn (dosering baseret på alder / legemsvægtforhold [30 mg til 75 mg en gang dagligt])
Beskrivelse af et udvalg af bivirkninger
Psykiatriske lidelser og patologier i nervesystemet
Influenza kan være forbundet med en række neurologiske og adfærdsmæssige symptomer, som kan omfatte hændelser som hallucinationer, delirium og unormal adfærd, i nogle tilfælde med dødelig udgang. Disse hændelser kan forekomme i forbindelse med encephalitis eller encephalopati, men uden en alvorlig sygdom tydelig.
Hos patienter med influenza, der modtog Tamiflu, har der været post-marketing rapporter om anfald og delirium (herunder symptomer som ændret bevidsthedsniveau, forvirring, unormal adfærd, delirium, hallucinationer, uro, angst, mareridt), hvilket i sjældne tilfælde resulterede i selvskade eller dødelig udgang. Disse hændelser blev hovedsageligt rapporteret blandt pædiatriske og unge patienter og havde ofte en "pludselig begyndelse og hurtig opløsning. Tamiflu's bidrag til forekomsten af disse hændelser kendes ikke. Disse neuropsykiatriske hændelser er også blevet rapporteret hos patienter med influenza, som de ikke havde taget Tamiflu.
Lever- og galdeforstyrrelser
Lidelser i det hepatobiliære system, herunder hepatitis og forhøjede leverenzymer hos patienter med influenzalignende sygdom. Disse tilfælde omfatter dødelig fulminant hepatitis / leversvigt.
Andre særlige populationer
Pædiatrisk population (spædbørn under 1 år)
I to undersøgelser for at karakterisere den farmakokinetiske, farmakodynamiske og sikkerhedsprofil af oseltamivir-baseret behandling hos 135 spædbørn under 1 år med influenzainfektion var sikkerhedsprofilen den samme mellem alderskohorter med opkastning, diarré og blæseudslæt som det mest hyppigt rapporterede bivirkninger (se afsnit 5.2). For spædbørn under 36 uger efter undfangelsesalderen er de tilgængelige data utilstrækkelige.
Tilgængelig information om oseltamivirs sikkerhed administreret til behandling af influenza hos spædbørn under 1 år, fra prospektive og retrospektive observationsstudier (samlet mere end 2.400 spædbørn i denne aldersgruppe), fra epidemiologiske databasesøgninger og fra post-marketing rapporter , tyder på, at sikkerhedsprofilen hos spædbørn under 1 år er sammenlignelig med sikkerhedsprofilen, der er fastlagt hos spædbørn i alderen 1 år eller ældre.
Ældre patienter og patienter med kronisk hjertesygdom og / eller kronisk luftvejssygdom
Befolkningen inkluderet i influenzabehandlingsundersøgelserne omfattede raske voksne / unge og patienter i risikogruppen (patienter med øget risiko for at udvikle influenzarelaterede komplikationer, f.eks. Ældre patienter og patienter med kronisk hjerte- eller luftvejssygdom). Samlet set var sikkerhedsprofilen hos "udsatte" patienter kvalitativt den, der blev observeret hos raske voksne / unge patienter.
Immunkompromitterede patienter
I en 12-ugers profylakseundersøgelse, der omfattede 475 immunkompromitterede patienter, herunder 18 børn i alderen 1 til 12 år og ældre, var sikkerhedsprofilen hos de 238 patienter, der blev behandlet med oseltamivir, den, der tidligere blev observeret i de kliniske forsøg med Tamiflu-profylakse.
Børn med allerede eksisterende bronchial astma
Generelt lignede bivirkningsprofilen hos børn med allerede eksisterende bronchial astma kvalitativt den hos raske børn.
Indberetning af formodede bivirkninger
Rapportering af formodede bivirkninger, der opstår efter godkendelse af lægemidlet, er vigtig, da det muliggør løbende overvågning af lægemidlets fordel / risiko -balance. Sundhedspersonale bedes rapportere alle formodede bivirkninger via det nationale rapporteringssystem. "Adresse http: //www.agenziafarmaco.gov.it/it/responsabili.
04.9 Overdosering
Rapporter om overdosering med Tamiflu er blevet indsamlet i kliniske forsøg og efter markedsføring. I de fleste rapporterede tilfælde af overdosering blev der ikke rapporteret om bivirkninger.
Bivirkninger, der blev rapporteret efter overdosering, var af samme art og fordeling som dem, der blev observeret ved terapeutiske doser af Tamiflu beskrevet i pkt. 4.8 "Bivirkninger".
Der kendes ingen specifik modgift.
Pædiatrisk population
Tilfælde af overdosering er blevet rapporteret hyppigere hos børn end hos voksne og unge. Der skal udvises forsigtighed ved forberedelse af Tamiflu oral suspension og ved administration af Tamiflu til børn.
05.0 FARMAKOLOGISKE EGENSKABER
05.1 Farmakodynamiske egenskaber
Farmakoterapeutisk gruppe: Antivirale midler til systemisk brug, neuraminidasehæmmere, ATC -kode: J05AH02
Oseltamivirphosphat er et pro-lægemiddel af den aktive metabolit (oseltamivir carboxylat). Den aktive metabolit er en selektiv hæmmer af influenza virus neuraminidase enzymer, som er glycoproteiner til stede på virionens overflade Aktiviteten af det virale neuraminidase enzym er vigtig både for virusindtrængning i ikke -inficerede celler og for frigivelse fra inficerede celler af nyligt dannede viruspartikler og for den efterfølgende spredning af den infektiøse virus i organismen.
Oseltamivir carboxylat hæmmer in vitro influenza A- og B -virus neuraminidaser. Oseltamivir hæmmer fosfat in vitro Infektion og replikation af influenzavirus. Oseltamivir administreret oralt hæmmer in vivo replikation og patogenicitet af influenza A- og B -vira i dyremodeller af influenzainfektion ved antivirale koncentrationer svarende til dem, der opnås hos mennesker med 75 mg to gange dagligt.
Den antivirale aktivitet af oseltamivir mod influenza A og B understøttes af eksperimentelle udfordringsstudier hos raske frivillige.
Værdierne for IC50 for neuraminidaseenzymet for oseltamivir var mellem 0,1 nM og 1,3 nM for det klinisk isolerede influenza A -virus og lig med 2,6 nM for influenza B -viruset. Højere IC50'er for influenza B -virus op til en median på 8,5 nM, blev observeret i publicerede undersøgelser.
Kliniske undersøgelser
Behandling af influenzainfektion
Indikationen er baseret på kliniske undersøgelser foretaget på naturligt overførte influenzatilfælde, hovedsageligt influenza A -infektioner.
Oseltamivir er kun effektivt mod sygdomme forårsaget af influenzavirus, statistiske analyser præsenteres derfor kun med henvisning til personer inficeret med influenzavirus. I hele den befolkning, der blev behandlet i undersøgelserne, som omfatter både influenzapositive og ITT -negative (intentioner om at behandle) forsøgspersoner, blev den primære effekt reduceret i forhold til antallet af influenza -negative individer. I den samlede behandlede befolkning blev influenzainfektion bekræftet hos 67% (interval: 46% -74%) af de rekrutterede patienter. 64% af ældre patienter var positive for influenza og 62% af dem med hjertesygdomme og / eller kronisk respiratorisk var positiv for influenza I alle fase III -behandlingsstudier blev patienter kun rekrutteret i perioder, hvor influenza cirkulerede i lokalsamfundet.
Voksne og unge i alderen 13 år eller ældre : For at være berettiget skulle patienterne præsentere sig inden for 36 timer efter symptomdebut, med feber ≥ 37,8 ° C forbundet med mindst et respiratorisk symptom (hoste, næsesymptomer eller ondt i halsen) og mindst et systemisk symptom (myalgi (kulderystelser / svedtendens, generel utilpashed, træthed eller hovedpine) .I den samlede analyse af alle influenzapositive voksne og unge (n = 2413), der var indskrevet i behandlingsstudierne, reducerede oseltamivir 75 mg to gange dagligt i 5 dage medianvarigheden af influenzasygdom på ca. en dag, fra 5,2 dage (95% CI: 4,9-5,5 dage) i placebogruppen til 4,2 dage (95% CI: 4,0 -4,4 dage; p ≤ 0,0001).
Procentdelen af forsøgspersoner, der udviklede specifikke komplikationer, der påvirker de nedre luftveje (hovedsageligt bronkitis) behandlet med antibiotika faldt fra 12,7% (135/1063) i placebogruppen til 8,6% (116/1350) i befolkningen behandlet med oseltamivir (p = 0,0012).
Behandling af influenza i højrisikopopulationer : hos ældre personer (≥ 65 år) og hos personer med kronisk hjerte- og / eller luftvejssygdom, der fik oseltamivir 75 mg to gange dagligt i 5 dage, median varighed af influenzasygdom Ikke er skrumpet betydeligt. I oseltamivir -grupperne blev den samlede febertid reduceret med en dag. Ved influenzapositiv ældre reducerede oseltamivir signifikant forekomsten af specifikke lavere luftvejskomplikationer (hovedsageligt bronkitis) behandlet med antibiotika fra 19% (52/268) i placebogruppen til 12% (29/250) i befolkningen. Behandlet med oseltamivir (p = 0,0156).
Hos influenzapositive patienter med kroniske hjerte- og/eller luftvejssygdomme var forekomsten af lavere luftvejskomplikationer (hovedsageligt bronkitis) behandlet med antibiotika 17% (22/133) i placebogruppen og 14% (16/118) i oseltamivir- behandlet population (p = 0,5976).
Behandling af influenza hos gravide : Der er ikke udført kontrollerede kliniske undersøgelser af brugen af oseltamivir hos gravide, men beviser fra post-marketing og retrospektive observationsstudier viser fordelene ved det nuværende doseringsregime i denne patientpopulation med hensyn til lavere sygelighed / dødelighed. Resultater opnået fra farmakokinetiske analyser indikerer lav eksponering for den aktive metabolit, dog anbefales ingen dosisjustering til gravide kvinder under behandling eller profylakse mod influenza (se pkt. 5.2, Farmakokinetiske egenskaber, specielle populationer).
Behandling af influenza hos børn : i en undersøgelse af ellers raske børn (65% influenza-positive) i alderen 1 til 12 år (gennemsnitsalderen 5,3 år), der havde feber (≥ 37,8 ° C) plus hoste eller nasal overbelastning, blev 67% af influenzapositive patienter smittet med influenza A -virus og 33% med influenzavirus B. Behandling med oseltamivir, der blev påbegyndt inden for 48 timer efter symptomdebut, reducerede den tid, der er nødvendig for sygdomsopløsning (defineret som samtidig tilbagevenden til normal sundhed og aktivitet og lindring af feber, hoste, og nasal overbelastning) på 1,5 dage (95% CI: 0,6-2,2 dage; gennemsnitlig akut otitis fra 26,5% (53/200) i placebogruppen til 16% (29/183) hos børn behandlet med oseltamivir (p = 0,013 ).
En anden undersøgelse blev afsluttet med 334 astmatiske børn i alderen 6 til 12 år, hvoraf 53,6% var influenza -positive. I oseltamivir -gruppen var medianvarigheden af sygdommen Ikke er skrumpet betydeligt.I denne population blev dag 6 (sidste behandlingsdag) det tvungne ekspiratoriske volumen i første sekund (FEV1) øget med 10,8% i oseltamivir -gruppen sammenlignet med 4,7% i placebogruppen (p = 0,0148).
Det Europæiske Lægemiddelagentur har udsat forpligtelsen til at indsende resultaterne af undersøgelser med Tamiflu i en eller flere undergrupper af den pædiatriske population for influenza (se afsnit 4.2 for information om pædiatrisk brug).
Indikationen hos spædbørn under 1 år er baseret på ekstrapolering af effektdata fra ældre børn, mens den anbefalede dosering er baseret på data fra den farmakokinetiske model (se afsnit 5.2).
Behandling af influenza B -infektion : Samlet set var 15% af den influenzapositive befolkning inficeret med influenza B, med procentdele fra 1 til 33% i individuelle undersøgelser. Den mediane sygdomsvarighed hos personer med influenza B -infektion viste ingen signifikante forskelle mellem behandlingsgrupperne i de enkelte undersøgelser. Data fra 504 influenza B-inficerede personer fra alle undersøgelser blev samlet til analysen. Sammenlignet med placebo reducerede oseltamivir med 0,7 dage (95% CI: 0,1-1,6 dage; p = 0,022) tiden til lindring af alle symptomer er en dag ( 95% CI: 0,4-1,7 dage; s
Forebyggelse af influenza
Oseltamivirs effekt til forebyggelse af naturligt overført influenzasygdom blev påvist i en undersøgelse om forebyggelse efter eksponering i husholdninger og i to undersøgelser om sæsonbestemt forebyggelse. I alle disse undersøgelser var det vigtigste mål for effektivitet forekomsten af laboratoriebekræftede tilfælde af influenza. Virulensen af influenzaudbrud er uforudsigelig og varierer inden for en region og fra sæson til sæson, derfor er antallet af patienter, der skal behandles (antal nødvendige til Treat, NNT) for at forhindre et tilfælde af influenzasygdom er variabel.
Post-eksponering forebyggelse : I løbet af en undersøgelse fik personer (12,6% vaccineret mod influenza) i kontakt med et individ med mistanke om influenza (index case) en 75 mg dosis oseltamivir en gang dagligt, startende inden for 2 dage efter "symptomdebut i indekset og fortsatte i syv dage. Influenza blev bekræftet i 163 af de 377 indeksstilfælde. Oseltamivir reducerede signifikant forekomsten af kliniske tilfælde af influenzasygdom, der forekom hos forsøgspersoner i kontakt med bekræftede tilfælde af influenza, fra 24/200 (12%) i placebogruppen til 2/205 ( 1%) i oseltamivir-gruppen (92% reduktion [95% CI: 6-16; p ≤ 0,0001]). NNT var 10 (95% CI: 9-12) blandt personer i kontakt med reelle tilfælde af influenza og 16 (95% CI: 15-19) over hele befolkningen (ITT), uanset status infektiøs i indekset.
Oseltamivirs effekt til forebyggelse af naturligt erhvervet influenza blev påvist i en forebyggelsesundersøgelse efter eksponering i husholdninger, der omfattede voksne, unge og børn i alderen 1 til 12 år, både som mistænkte tilfælde (indekssager) og som personer i familiekontakt. effektparameter for denne undersøgelse var forekomsten af laboratoriebekræftet klinisk influenza i husholdninger. Oseltamivir -profylakse varede i 10 dage. I den samlede befolkning var der en reduktion i forekomsten af laboratoriebekræftet klinisk influenza i husstande fra 20% (27/136), i gruppen, der ikke modtog forebyggelse, til 7% (10/135) i gruppen, der modtog forebyggelsen (62,7% reduktion [95% CI: 26,0-81,2; p = 0,0042]). I familierne til indekssagerne med influenzainfektion var der en reduktion i forekomsten af influenza fra 26% (23/89), i gruppen, der ikke modtog forebyggelse, til 11% (9/84) i gruppen, der modtaget forebyggelse (58,5% reduktion [95% CI: 15,6-79,6; p = 0,0114]).
Ifølge en analyse foretaget i en undergruppe af børn i alderen 1 til 12 år blev forekomsten af laboratoriebekræftet klinisk influenza blandt børn signifikant reduceret fra 19% (21/111) i gruppen, der ikke modtog forebyggelse, med 7% ( 7/104), i gruppen, der modtog forebyggelse (reduktion på 64,4% [95% CI: 15,8-85,0; p = 0,0188]). Blandt børn, der ved baseline ikke allerede var ved at kaste virus, forekomsten af laboratorie- bekræftet klinisk influenza faldt fra 21% (15/70) i gruppen, der ikke modtog forebyggelse, til 4% (2/47) i gruppen, der modtog forebyggelsen (reduktion på 80,1% [95% CI: 22,0- 94,9; p = 0,0206]). NNT for den samlede pædiatriske population var 9 (95% CI: 7-24) i hele befolkningen (ITT) og 8 (95% CI: 6, øvre grænse ikke estimerbar) i pædiatriske kontaktpersoner i tilfældeindekset med infektion ( ITTII).
Forebyggelse under en "samfundsinfluenzaepidemi." : I en samlet analyse af to andre undersøgelser foretaget hos ellers raske, ikke -vaccinerede voksne reducerede oseltamivir 75 mg givet en gang dagligt i 6 uger signifikant forekomsten af kliniske tilfælde af influenza fra 25/519 (4,8%) i placebogruppen til 6/520 (1,2%) i oseltamivir-gruppen (76% reduktion [95% CI: 1,6-5,7, p = 0,0006]) under en "influenzapidemi i samfundet. I denne undersøgelse var NNT 28 (95% CI: 24- 50).
I en undersøgelse af ældre patienter indlagt på plejehjem, hvoraf 80% var blevet vaccineret i studiesæsonen, reducerede dosis 75 mg oseltamivir én gang dagligt i 6 uger signifikant forekomsten af kliniske tilfælde. Influenzasygdom fra 12/272 (4,4 %) i placebogruppen til 1/276 (0,4%) i oseltamivir-gruppen (92% reduktion [95% CI: 1,5-6,6; p = 0,0015]). I denne undersøgelse var NNT 25 (95% CI: 23-62).
Influenzaprofylakse hos immunkompromitterede patienter : Der blev udført en randomiseret, placebokontrolleret, dobbeltblind undersøgelse af sæsoninfluenza-profylakse hos 475 immunsupprimerede patienter (388 patienter med solid organtransplantation [195 med placebo, 193 med oseltamivir], 87 patienter med hæmatopoietiske stamceller [43 med placebo, 44 Med oseltamivir], ingen patienter med andre immunsuppressive tilstande), herunder 18 børn i alderen 1 til 12 år. Det primære endepunkt for denne undersøgelse var forekomsten af laboratoriebekræftet klinisk influenza bestemt ved viralkultur og / eller firdobling af antistoftitren mod hæmagglutinin (Haemoagglutinin Inhibition, HAI). Incidensen af bekræftet klinisk influenzalaboratorium var 2,9% (7/238) i placebo-armen og 2,1% (5/237) i oseltamivir-eksponerede gruppe (95% CI: 2,3-4,1; p = 0,772).
Der er ikke udført specifikke undersøgelser for at evaluere reduktionen af risikoen for komplikationer.
Resistens over for oseltamivir
Kliniske undersøgelser : Risikoen for at udvikle influenzavirus med reduceret modtagelighed eller netresistens over for oseltamivir blev undersøgt i kliniske forsøg sponsoreret af Roche. Alle patienter, der viste sig at være bærere af oseltamivir-resistent virus, blev forbigående ryddet virussen normalt og viste ingen forværring af den kliniske tilstand.
* Komplet genotypebestemmelse blev ikke udført i alle undersøgelser.
Der er ingen tegn på begyndelsen af lægemiddelresistensfænomener forbundet med brugen af Tamiflu i kliniske forsøg hidtil udført i forebyggelse af influenza efter eksponering (7 dage), eftereksponering inden for familier (10 dage) og sæsonbestemt (42 dage ) hos immunkompetente patienter. Der blev ikke observeret nogen resistens under profylakseundersøgelsen op til 12 uger hos immunkompromitterede patienter.
Kliniske data og overvågningsdata : spontane mutationer forbundet med nedsat følsomhed over for oseltamivir in vitro er fundet i influenza A og influenza B virale isolater fra patienter uden forudgående eksponering for oseltamivir. Resistente stammer udvalgt under behandling med oseltamivir er blevet isoleret fra både immunkompetente og immunkompromitterede patienter. Immunkompromitterede patienter og små børn har større risiko for at udvikle resistente virale stammer under behandling med oseltamivir.
Oseltamivir-resistente vira isoleret fra oseltamivir-behandlede patienter og laboratoriestammer af oseltamivir-resistente influenzavirus har vist sig at indeholde mutationer i neuraminidaser N1 og N2. Modstandsmutationer har en tendens til at være specifikke for virale undertyper. Siden 2007 er den resistensrelaterede H275Y-mutation i sæsonbestemte H1N1-stammer blevet udbredt. Følsomhed over for oseltamivir og forekomsten af disse vira ser ud til at variere afhængigt af både sæsonen og den geografiske region. I 2008 blev H275Y fundet i> 99% af cirkulerende H1N1 -influenzavirusisolater i Europa.2009 H1N1 -influenza ("svineinfluenza") var ensartet modtagelig for oseltamivir med kun sporadiske tilfælde af resistens i forhold til både terapeutiske og profylaktiske regimer.
05.2 "Farmakokinetiske egenskaber
Generelle oplysninger
Absorption
Oseltamivir absorberes let fra mave-tarmkanalen efter oral administration af oseltamivirphosphat (pro-lægemiddel) og omdannes stort set til den aktive metabolit (oseltamivir carboxylat) hovedsageligt af leveresteraser. Mindst 75% af den oralt indgivne dosis når den systemiske cirkulation som en aktiv metabolit. Eksponeringen for pro-lægemidlet er mindre end 5% af den for den aktive metabolit Plasmakoncentrationer af pro-lægemidlet og den aktive metabolit er dosisproportionelle og påvirkes ikke af samtidig fødeindtagelse.
Fordeling
Ved steady state er middelfordelingsvolumenet for oseltamivircarboxylat hos mennesker cirka 23 liter, et volumen svarende til ekstracellulær kropsvæske.Når neuraminidaseaktivitet er ekstracellulær, distribueres oseltamivircarboxylat til alle steder, hvor influenzaviruset.
Bindingen af oseltamivircarboxylat til humane plasmaproteiner er ubetydelig (ca. 3%).
Biotransformation
Oseltamivir omdannes i vid udstrækning til oseltamivircarboxylat af esteraser, der hovedsageligt findes i leveren. Uddannelse in vitro vist, at hverken oseltamivir eller den aktive metabolit er et substrat eller en hæmmer af de vigtigste isoformer af cytochrom P450. De er ikke identificeret in vivofase 2 -konjugater for ingen af forbindelserne.
Eliminering
Absorberet oseltamivir elimineres hovedsageligt (> 90%) ved omdannelse til oseltamivircarboxylat. Det metaboliseres ikke yderligere og elimineres i urinen. Hos de fleste forsøgspersoner falder de maksimale plasmakoncentrationer af oseltamivircarboxylat med en halveringstid på mellem 6 og 10 timer. Den aktive metabolit elimineres fuldstændigt ved renal udskillelse. Renal clearance (18,8 l / t) overstiger glomerulær filtrationshastighed (7,5 l / h) hvilket indikerer, at tubulær sekretion forekommer ud over glomerulær filtrering Mindre end 20% af en radiomærket oral dosis elimineres i fæces.
Andre særlige populationer
Pædiatrisk population
Spædbørn under 1 år : Tamiflu's farmakokinetik, farmakodynamik og sikkerhed blev evalueret i to åbne ukontrollerede undersøgelser, der omfattede spædbørn under 1 år, der var inficeret med influenzavirus (n = 135). Elimineringshastigheden af den aktive metabolit korrigeret for kropsvægt, det falder hos patienter under et år.Eksponering for metabolitten er også mere variabel hos yngre børn. Tilgængelige data indikerer, at eksponering efter en dosis på 3 mg / kg hos spædbørn i alderen 0-12 måneder producerer lægemiddel- og metaboliteksponeringer, der forventes at være effektive, med en sikkerhedsprofil, der kan sammenlignes med den, der observeres. Hos ældre børn og voksne med godkendt dosis (se afsnit 4.1 og 4.2) De rapporterede bivirkninger var i overensstemmelse med sikkerhedsprofilen, der blev fastlagt for ældre børn.
Der er ingen data tilgængelige for spædbørn under 1 år til forebyggelse af influenza efter eksponering Forebyggelse under en samfundsbaseret influenzapidemi er ikke undersøgt hos børn under 12 år.
Børn i alderen 1 år eller ældre: oseltamivirs farmakokinetik blev evalueret i farmakokinetiske studier med enkeltdosis hos børn og unge i alderen 1 til 16 år. Flerdosis farmakokinetik blev undersøgt hos et lille antal børn, der var indskrevet i et klinisk effektstudie. Yngre børn rensede både pro-lægemidlet og den aktive metabolit hurtigere end voksne, hvilket resulterede i mere eksponering. Lav for en given mg / kg dosis. Doser på 2 mg / kg giver oseltamivircarboxylateksponering svarende til den, der opnås hos voksne, der tager en enkelt dosis på 75 mg (ca. 1 mg / kg). Oseltamivirs farmakokinetik hos børn og unge i alderen 12 år og ældre ligner den hos voksne.
Ældre borgere
Ved steady state var eksponeringen for den aktive metabolit hos ældre (i alderen 65 til 78 år) 25 til 35% højere end rapporteret hos voksne under 65 år givet lignende doser oseltamivir. L "halveringstid observeret hos ældre var ligner den, der observeres hos unge voksne. Baseret på lægemiddeleksponering og tolerabilitet kræves ingen dosisjustering hos ældre patienter, medmindre der er tegn på moderat eller svært nedsat nyrefunktion (kreatininclearance mindre end 60 ml / min) (se pkt. 4.2).
Nyresvigt
Administration af oseltamivirphosphat 100 mg to gange dagligt i 5 dage til patienter med forskellige grader af nedsat nyrefunktion har vist, at eksponering for oseltamivircarboxylat er omvendt proportional med faldet i nyrefunktionen. Se dosering for pkt. 4.2.
Leverinsufficiens
Uddannelse in vitro fastslog, at hverken en signifikant stigning i oseltamivir -eksponeringen eller et signifikant fald i eksponeringen for den aktive metabolit forventes hos patienter med nedsat leverfunktion (se pkt. 4.2).
Gravid kvinde
En "analyse af puljede populationsfarmakokinetiske data indikerer, at Tamiflu-doseringsregimet rapporteret i afsnit 4.2 Dosering og indgivelsesmåde resulterer i" lavere eksponering (30% som middel af alle trimestre) for den aktive metabolit hos gravide kvinder end til ikke-gravide . Den laveste forventede eksponering forbliver imidlertid over inhiberende koncentrationer (IC95 -værdier) og på et terapeutisk niveau mod en række influenzavirusstammer.Også viser observationsstudier en fordel ved det nuværende doseringsregime i denne patientpopulation. Derfor anbefales det ikke at justere dosis ved behandling eller profylakse af influenza hos gravide kvinder (se pkt. 4.6 Fertilitet, graviditet og amning).
05.3 Prækliniske sikkerhedsdata
Ikke-kliniske data afslører ingen særlig fare for mennesker baseret på konventionelle undersøgelser af sikkerhedsfarmakologi, toksicitet ved gentagen dosering og gentoksicitet. Resultaterne af konventionelle rottekarcinogenicitetsundersøgelser har vist en tendens til en dosisafhængig stigning i "forekomst af nogle typer tumorer karakteristisk af de anvendte rotterstammer. Under hensyntagen til eksponeringsmargenerne i forhold til den forventede eksponering ved brug af mennesker ændrer disse resultater ikke fordel-risiko-forholdet ved brug af Tamiflu i dets godkendte terapeutiske indikationer.
Teratogenicitetsundersøgelser blev udført hos rotter og kaniner op til doser på henholdsvis 1500 mg / kg / dag og 500 mg / kg / dag. Der blev ikke observeret nogen virkninger på fosterets udvikling. En fertilitetsundersøgelse hos rotter med en dosis på op til 1500 mg / kg / dag afslørede ingen bivirkninger på begge køn. I præ- og postnatale undersøgelser af rotter blev der observeret en forlængelse af fødselsvarigheden ved en dosis på 1500 mg / kg / dag: sikkerhedsmargen mellem menneskelig eksponering og den højeste dosis uden effekt (500 mg / dag). dag) hos rotte er 480 gange for oseltamivir og 44 gange for den aktive metabolit. Hos rotter og kaniner var fostrets eksponering cirka 15-20% af moderens.
Hos diegivende rotter udskilles oseltamivir og den aktive metabolit i modermælk. Begrænsede data indikerer, at oseltamivir og den aktive metabolit udskilles i human modermælk. Ekstrapolering fra dyredata fører til et skøn på henholdsvis 0,01 mg / dag og 0,3 mg / dag for de to forbindelser.
Muligheden for hudsensibilisering over for oseltamivir blev observeret i "maksimeringstesten" udført på marsvin. Ca. 50% af de dyr, der blev behandlet med den ikke-formulerede aktive ingrediens, viste erytem efter stimulering af de inducerede dyr. Reversibel øjenirritation blev observeret hos kaniner.
Selvom meget høje orale enkeltdoser af oseltamivirphosphatsalt op til det højeste testede dosisniveau (1310 mg / kg) ikke resulterede i bivirkninger hos voksne rotter, resulterede de samme dosisniveauer i toksicitet hos unge 7 dage gamle rotter alder, inklusive død. Disse reaktioner er blevet observeret ved doser på 657 mg / kg og derover. Ved doser på 500 mg / kg blev der ikke observeret nogen bivirkninger, selv ved kronisk behandling (500 mg / kg / dag administreret 7 til 21 dage efter levering).
06.0 LÆGEMIDDELOPLYSNINGER
06.1 Hjælpestoffer
Kapselindhold
Pregelatiniseret stivelse (afledt af majsstivelse)
Talc
Povidon
Croscarmellosenatrium
Natriumstearylfumarat.
Kapselskal
Gele
Gul jernoxid (E172)
Rødt jernoxid (E172)
Titandioxid (E171).
Blæk til udskrivning
Shellac
Titandioxid (E171)
FD og C Blue 2 (indigo karmin, E132).
06.2 Uforenelighed
Ikke relevant.
06.3 Gyldighedsperiode
7 år.
Opbevaring af suspensionen fremstillet på apoteket.
Opbevaringstid på 10 dage ved opbevaring ved temperaturer under 25 ° C.
06.4 Særlige opbevaringsforhold
Må ikke opbevares over 25 ° C.
Opbevaringsbetingelser for apotekets klargjorte suspension, se afsnit 6.3.
06.5 Den umiddelbare emballages art og emballagens indhold
Triple blister (PVC / PE / PVDC, forseglet med aluminium).
Pakke med 10 kapsler.
06.6 Brugsanvisning og håndtering
Ubrugt medicin og affald fra denne medicin skal bortskaffes i overensstemmelse med lokale regler.
Ekstemporan formulering
Når Tamiflu pulver til oral suspension ikke er tilgængeligt
Klar til brug Tamiflu til oral suspension (6 mg / ml) er den foretrukne formulering til pædiatriske og voksne patienter, der har svært ved at sluge kapsler, eller hvor der er behov for lavere doser. Hvis Tamiflu pulver til oral suspension er klar til brug, er ikke tilgængelig, kan apotekeren tilberede en suspension (6 mg / ml) fra Tamiflu kapsler, eller de samme patienter kan bruge kapslerne til at forberede suspensionen derhjemme.
Det præparat, der er tilberedt på apoteket, bør foretrækkes frem for det, der er tilberedt derhjemme. Detaljerede oplysninger om præparatet derhjemme findes i afsnittet "Tilberedning af Tamiflu i flydende form derhjemme" i indlægssedlen med Tamiflu kapsler.
Orale sprøjter med passende volumen og graduering bør tilvejebringes både til administration af den apotekfremstillede suspension og til procedurer i forbindelse med hjemmeforberedelse. I begge tilfælde skal den korrekte volumen helst markeres på sprøjterne.
Forberedelse på apoteket
6 mg / ml suspension fremstillet på et apotek ud fra kapslen
Voksne, unge, børn i alderen 1 år og derover, der ikke er i stand til at sluge kapslerne hele
Denne procedure beskriver fremstilling af en 6 mg / ml suspension, som vil give en patient en tilstrækkelig mængde medicin til en 5 dages behandling eller 10 dages profylakse.
Apotekeren kan fremstille en 6 mg / ml suspension fra Tamiflu 30 mg, 45 mg eller 75 mg kapsler ved hjælp af vand indeholdende 0,05% vægt / volumen natriumbenzoat tilsat som konserveringsmiddel.
Beregn først det samlede volumen, der skal forberedes og udleveres for at give patienten en 5-dages behandling eller 10-dages profylakse. Det krævede samlede volumen bestemmes af patientens vægt i henhold til anbefalingerne i nedenstående tabel. For at muliggøre nøjagtig tilbagetrækning af op til 10 doser (2 udtag pr. Daglig dosis i en behandling i 5 dage) skal kolonnen, der angiver tabsestimatet, overvejes i præparatet.
Volumen af 6 mg / ml suspension fremstillet på apoteket baseret på patientens vægt
* Det afhænger af doseringen af de anvendte kapsler.
For det andet bestemmes antallet af kapsler og mængden af vehikel (vand indeholdende 0,05% w / v natriumbenzoat tilsat som konserveringsmiddel), der er nødvendigt for at forberede det samlede volumen (beregnet ud fra tabellen ovenfor) på 6 mg / v suspension. Ml fremstillet i apoteket, som vist i nedenstående tabel:
Antal kapsler og mængde køretøj, der er nødvendig for at forberede det samlede volumen af en apotek-klargjort 6 mg / ml suspension
* Denne kombination af kapselstyrker kan ikke bruges til at opnå den krævede styrke, så brug forskellige styrkekapsler.
For det tredje skal du følge fremgangsmåden herunder til fremstilling af 6 mg / ml suspension fra Tamiflu kapsler:
1. Hæld den korrekte mængde vand i et glas målebæger med passende størrelse, og tilsæt 0,05% vægt / volumen natriumbenzoat som konserveringsmiddel.
2. Åbn Tamiflu -kapslerne i den angivne mængde, og hæld indholdet af hver kapsel direkte i vandet i glaset.
3. Bland med et egnet omrøringsværktøj i 2 minutter.
(Bemærk: det aktive stof, oseltamivirphosphat, opløses let i vand. Suspensionen skyldes nogle uopløselige hjælpestoffer i Tamiflu kapsler.)
4. Overfør suspensionen til en ravfarvet glas- eller polyethylenterephthalat (PET) flaske. En pipette kan bruges til at undgå lækager.
5. Luk flasken med en børnesikker lukning.
6. Læg en "hjælpemærke på flasken, der står" Ryst forsigtigt før "brug".
(Bemærk: suspensionen skal rystes forsigtigt før administration for at reducere dannelsen af luftbobler).
7. Instruer forælderen eller omsorgspersonen om, at materiale, der efterlades ubrugt efter endt behandling, skal bortskaffes korrekt. Det anbefales, at disse oplysninger gives ved at vedhæfte en hjælpemærke til flasken eller ved at tilføje en sætning til instruktionerne på apotekets etiket.
8. Påfør en etiket med den relevante udløbsdato i overensstemmelse med opbevaringsbetingelserne (se afsnit 6.3).
Læg en apoteksmærke på flasken, der indeholder patientens navn, doseringsinstruktioner, udløbsdato, medicinnavn og andre oplysninger, der er nødvendige for at overholde lokale farmaceutiske forskrifter. Se tabellen herunder for instruktioner om den korrekte dosering.
Dosering til 6 mg / ml suspension fremstillet i apotek af Tamiflu kapsler til spædbørn og børn i alderen et år eller ældre
Administrer den apotekfremstillede suspension med en gradueret oral sprøjte for at måle små mængder af suspensionen. Hvis det er muligt, markeres eller fremhæves på den orale sprøjte det niveau, der svarer til den passende dosis (i henhold til doseringstabellen ovenfor) for hver patient.
Den passende dosis skal blandes af plejepersonalet med en lige stor mængde sød flydende mad, f.eks. Sukkervand, chokoladesirup, kirsebærsirup, desserttoppe (f.eks. Karamel eller karamelsauce) for at dække den bitre smag.
Børn under 1 år
Denne procedure beskriver fremstilling af en 6 mg / ml suspension, der vil give en patient en tilstrækkelig mængde lægemiddel til en 5-dages behandling eller 10-dages profylakse.
Apotekeren kan fremstille en 6 mg / ml suspension fra Tamiflu 30 mg, 45 mg eller 75 mg kapsler ved hjælp af vand indeholdende 0,05% vægt / volumen natriumbenzoat tilsat som konserveringsmiddel.
Beregn først det samlede volumen, der skal forberedes og udleveres til hver patient. Det krævede samlede volumen bestemmes af patientens vægt i henhold til anbefalingerne i nedenstående tabel. For at muliggøre nøjagtig tilbagetrækning af op til 10 doser (2 udtag pr. Daglig behandlingsdosis i 5 dage) skal kolonnen, der angiver tabsestimatet, overvejes i præparatet.
Suspension volumen på 6 mg / ml tilberedt på apoteket baseret på patientens vægt
* Det afhænger af doseringen af de anvendte kapsler.
For det andet bestemmes antallet af kapsler og mængden af vehikel (vand indeholdende 0,05% w / v natriumbenzoat tilsat som konserveringsmiddel), der er nødvendigt for at forberede det samlede volumen (beregnet ud fra tabellen ovenfor) på 6 mg / v suspension. Ml fremstillet i apoteket, som vist i nedenstående tabel:
Antal kapsler og mængde køretøj, der er nødvendig for at forberede det samlede volumen af en apotek-klargjort 6 mg / ml suspension
* Denne kombination af kapselstyrker kan ikke bruges til at opnå den nødvendige koncentration; derfor at bruge kapsler med forskellige styrker.
For det tredje skal du følge fremgangsmåden herunder til fremstilling af 6 mg / ml suspension fra Tamiflu kapsler:
1. Hæld den korrekte mængde vand i et glas målebæger med passende størrelse, og tilsæt 0,05 vægtprocent natriumbenzoat som konserveringsmiddel.
2. Åbn Tamiflu -kapslerne i den angivne mængde, og hæld indholdet af hver kapsel direkte i vandet i glaset.
3. Bland med et egnet omrøringsværktøj i 2 minutter.
(Bemærk: Det aktive stof, oseltamivirphosphat, opløses let i vand. Suspensionen skyldes nogle uopløselige hjælpestoffer i Tamiflu kapsler.)
4. Overfør suspensionen til en ravfarvet glas- eller polyethylenterephthalat (PET) flaske. En pipette kan bruges til at undgå lækager.
5. Luk flasken med en børnesikret lukning.
6. Læg en "hjælpemærke på flasken, der står" Ryst forsigtigt før "brug".
(Bemærk: suspensionen skal rystes forsigtigt før administration for at reducere dannelsen af luftbobler).
7. Instruer forælderen eller patientens pårørende om, at materiale, der efterlades ubrugt efter endt behandling, skal bortskaffes korrekt. Det anbefales, at disse oplysninger gives ved at vedhæfte en hjælpemærke til flasken eller ved at tilføje en sætning til instruktionerne på apotekets etiket.
8. Påfør en etiket med den relevante udløbsdato i overensstemmelse med opbevaringsbetingelserne (se afsnit 6.3).
Læg en apoteksmærke på flasken, der indeholder patientens navn, doseringsinstruktioner, udløbsdato, medicinnavn og andre oplysninger, der er nødvendige for at overholde lokale farmaceutiske forskrifter. Se tabellen herunder for instruktioner om den korrekte dosering.
Dosering til 6 mg / ml suspension fremstillet på apotek af Tamiflu kapsler til spædbørn under 1 år
Administrer den apotekfremstillede suspension med en gradueret oral sprøjte for at måle små mængder af suspensionen. Hvis det er muligt, markeres eller fremhæves på den orale sprøjte det niveau, der svarer til den passende dosis (i henhold til doseringstabellen ovenfor) for hver patient.
Den passende dosis skal blandes af plejepersonalet med en lige stor mængde sød flydende mad, f.eks. Sukkervand, chokoladesirup, kirsebærsirup, desserttoppe (f.eks. Karamel eller karamelsauce) for at dække den bitre smag.
Forberedelse derhjemme
I tilfælde af at Tamiflu oral suspension klar til brug ikke er tilgængelig, bør der anvendes et apotek tilberedt suspension fra Tamiflu kapsler (for detaljerede instruktioner, se ovenfor). Hvis hverken Tamiflu oral suspension er klar til brug. Brug eller apotek-forberedt suspension, Tamiflu-suspension kan fremstilles derhjemme.
Når den passende kapselstyrke er tilgængelig ved de nødvendige doser, opnås dosen ved at åbne kapslen og blande dens indhold med højst en teskefuld (5 ml) af et egnet sødet mad. Den bitre smag kan maskeres med produkter som sukkervand, chokoladesirup, kirsebærsirup, desserttoppe (som karamel eller karamelsauce). Blandingen skal rystes og hele indholdet administreres til patienten. Blandingen skal synkes umiddelbart efter tilberedningen.
Når der kun er 75 mg kapsler til rådighed, og der kræves 30 mg eller 45 mg doser, kræver tilberedning af Tamiflu -suspensionen yderligere trin. Detaljerede instruktioner findes i afsnittet "Tilberedning af Tamiflu flydende form derhjemme" i indlægssedlen med Tamiflu kapsler.
07.0 INDEHAVER AF MARKEDSFØRINGSTILLADELSE
Roche registrering begrænset
6 Falcon Way
Shire Park
Welwyn Garden City
AL7 1TW
Storbritannien
08.0 MARKEDSFØRINGSTILLADELSESNUMMER
EU/1/02/222/003
035943036
09.0 DATO FOR FØRSTE TILLADELSE ELLER FORNYELSE AF TILLADELSEN
Dato for første godkendelse: 20. juni 2002.
Dato for sidste fornyelse: 20. juni 2012.
10.0 DATO FOR REVISION AF TEKSTEN
Maj 2015