Aktive ingredienser: Ezetimibe
ZETIA 10 mg tabletter
Hvorfor bruges Zetia? Hvad er det for?
ZETIA er en medicin til at reducere forhøjede kolesterolniveauer.
ZETIA reducerer niveauet af totalt kolesterol, det "dårlige" kolesterol (LDL -kolesterol) og de fedtstoffer, der kaldes triglycerider i blodet. ZETIA øger også niveauet af "godt" kolesterol (HDL -kolesterol).
Ezetimibe, den aktive ingrediens i ZETIA virker ved at reducere absorptionen af kolesterol fra tarmen.
Faldet i kolesterolniveauer forårsaget af ZETIA er ud over det, der skyldes statiner (en gruppe lægemidler, der virker ved at reducere kroppens egen produktion af kolesterol).
Kolesterol er et af flere fedtstoffer, der findes i blodbanen. Total kolesterol består hovedsageligt af LDL -kolesterol og HDL -kolesterol.
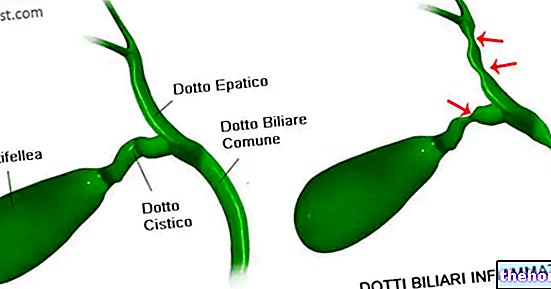
LDL -kolesterol kaldes ofte "dårligt" kolesterol, fordi det kan bygge sig op i arterievægge og danne plaketter. Over tid kan denne plakopbygning føre til indsnævring af arterierne. Denne indsnævring kan bremse eller blokere blodgennemstrømningen til vitale organer som hjerte og hjerne. Denne blokering af blodgennemstrømningen kan forårsage et hjerteanfald eller slagtilfælde.
HDL -kolesterol kaldes ofte "godt" kolesterol, fordi det hjælper med at forhindre dårligt kolesterol i at bygge sig op i arterierne og beskytter mod hjertesygdomme.
Triglycerider er en anden form for fedt i blodet, der kan øge risikoen for hjertesygdomme.
Det bruges til patienter, der ikke kan kontrollere deres kolesteroltal ved at reducere deres kolesteroltal alene med kosten. Du skal være på en kolesterolsænkende diæt, mens du tager denne medicin.
ZETIA bruges som et supplement til din kolesterolsænkende diæt, hvis du har:
- et forhøjet kolesteroltal i blodet (primær hyperkolesterolæmi [familiær og ikke-familiær heterozygot])
- sammen med en statin, når dit kolesterol ikke er tilstrækkeligt kontrolleret med et statin alene
- alene, når statinbehandling er upassende eller ikke tolereres
- en arvelig sygdom (homozygot familiær hyperkolesterolæmi), som øger niveauet af kolesterol i blodet. Du vil også blive ordineret en statin og kan blive ordineret en anden behandling
- en arvelig sygdom (homozygot sitosterolæmi, også kendt som phytosterolæmi) - som øger niveauet af plantesteroler i blodet.
ZETIA hjælper dig ikke med at tabe sig.
Kontraindikationer Når Zetia ikke bør bruges
Hvis du får ordineret ZETIA sammen med en statin, skal du læse indlægssedlen for den specifikke medicin, du ordinerer.
Tag ikke ZETIA, hvis:
- du er allergisk (overfølsom) over for ezetimibe eller et af de øvrige indholdsstoffer i dette lægemiddel (se afsnittet Pakningsstørrelser og andre oplysninger).
Tag ikke ZETIA sammen med en statin, hvis:
- du i øjeblikket har leverproblemer
- er gravid eller ammer.
Forholdsregler ved brug Det, du skal vide, før du tager Zetia
- fortæl din læge om eventuelle tilstande, herunder allergi;
- din læge bør bestille en blodprøve, inden du starter ZETIA -behandling sammen med en statin. Dette er for at kontrollere, hvordan din lever fungerer;
- Din læge kan også bede dig om at få taget blodprøver for at kontrollere, hvordan din lever fungerer, efter at du er begyndt at tage ZETIA sammen med en statin.
Hvis du har moderate eller alvorlige leverproblemer, anbefales brug af ZETIA ikke.
Sikkerheden og effekten af ZETIA administreret i kombination med visse kolesterolsænkende lægemidler, fibrater, er ikke fastslået.
Børn
ZETIA anbefales ikke til børn under 10 år.
Interaktioner Hvilke lægemidler eller fødevarer kan ændre virkningen af Zetia
Fortæl det til din læge eller apoteket, hvis du tager eller for nylig har taget anden medicin, også medicin, der er købt uden recept.
Fortæl især din læge, hvis du tager medicin med et af følgende aktive stoffer:
- cyclosporin (bruges ofte til organtransplanterede patienter)
- medicin med et aktivt stof, der forhindrer blodpropper, såsom warfarin, phenprocoumon, acenocoumarol eller fluindion (antikoagulantia)
- cholestyramin (bruges også til at sænke kolesterol), da det ændrer effektiviteten af ZETIA
- fibrater (bruges også til at sænke kolesterol).
Advarsler Det er vigtigt at vide, at:
Graviditet og amning
Tag ikke ZETIA sammen med en statin, hvis du er gravid, forsøger at blive gravid, eller hvis du tror, du kan være gravid. Hvis du bliver gravid, mens du tager ZETIA sammen med en statin, skal du stoppe begge behandlinger med det samme og kontakte din læge. Der er ingen erfaring med brug af ZETIA under graviditet uden statin. Hvis du er gravid, skal du spørge din læge om passende anbefalinger, før du bruger ZETIA.
Tag ikke ZETIA sammen med en statin, hvis du ammer, da det ikke vides, om de to lægemidler udskilles i modermælk. ZETIA, selv når det tages alene uden statin, bør ikke bruges under amning.Spørg din læge om passende anbefalinger.
Spørg din læge eller apotek til råds, før du tager medicin.
Kørsel og brug af maskiner
Der forventes ingen virkninger af ZETIA på evnen til at føre motorkøretøj eller betjene maskiner. Det skal dog tages i betragtning, at nogle mennesker kan føle sig svimmel efter at have taget ZETIA.
ZETIA indeholder lactose
ZETIA tabletter indeholder et sukker kaldet lactose. Hvis din læge har fortalt dig, at du ikke tåler nogle sukkerarter, skal du kontakte din læge, inden du tager dette lægemiddel.
Dosis, metode og administrationstidspunkt Sådan bruges Zetia: Dosering
Tag altid ZETIA nøjagtigt efter lægens anvisning. Fortsæt med at tage dine andre kolesterolsænkende lægemidler, medmindre din læge siger, at du skal stoppe med at bruge dem. Kontakt din læge eller apotek, hvis du er i tvivl.
- Inden du begynder at tage ZETIA, skal du følge en kolesterolsænkende diæt.
- Du skal fortsætte med at følge denne kolesterolsænkende diæt, mens du tager ZETIA.
Voksne, unge og børn (10 til 17 år): Dosen er en 10 mg tablet ZETIA én gang dagligt, der skal tages gennem munden.
Du kan tage ZETIA når som helst på dagen og uanset måltider.
Hvis din læge har ordineret ZETIA sammen med en statin, kan de to lægemidler tages samtidigt. I dette tilfælde henvises der også til de specifikke doseringsinstruktioner i indlægssedlen til den anden foreskrevne medicin.
Hvis din læge har ordineret ZETIA sammen med en anden kolesterolsænkende medicin, der indeholder det aktive stof cholestyramin eller anden medicin, der indeholder galdesekvestranter, skal du tage ZETIA mindst 2 timer før eller 4 timer efter indtagelse af galdesekvestranten.
Overdosering Hvad skal man gøre, hvis man har taget for meget Zetia
Hvis du har taget for meget ZETIA, end du burde
Kontakt din læge eller apotek.
Hvis du har glemt at tage ZETIA
Tag ikke en dobbeltdosis; simpelthen genoptage din sædvanlige dosis på det sædvanlige tidspunkt den næste dag.
Spørg din læge eller apotek, hvis du har yderligere spørgsmål om brugen af dette lægemiddel.
Bivirkninger Hvad er bivirkningerne af Zetia
Som al anden medicin kan ZETIA forårsage bivirkninger, men ikke alle får bivirkninger.
Følgende udtryk bruges til at beskrive, hvor ofte bivirkninger er blevet rapporteret:
- Meget almindelig (kan forekomme hos mere end 1 ud af 10 patienter)
- Almindelig (kan forekomme hos op til 1 ud af 10 patienter)
- Ikke almindelig (kan forekomme hos op til 1 ud af 100 patienter)
- Sjælden (kan forekomme hos op til 1 ud af 1.000 patienter)
- Meget sjælden (kan forekomme hos op til 1 ud af 10.000 patienter, inklusive isolerede tilfælde)
Kontakt straks din læge, hvis du oplever uforklarlige muskelsmerter, muskelsømhed eller svaghed. Dette skyldes, at muskelproblemer, herunder skader på muskelvæv, der resulterer i nyreskader, sjældent kan være alvorlige og potentielt livstruende.
Allergiske reaktioner er blevet rapporteret ved almindelig brug af medicinen, herunder hævelse af ansigt, læber, tunge og / eller hals, som kan forårsage vejrtræknings- eller synkebesvær (hvilket kræver øjeblikkelig behandling).
Når de bruges alene, er følgende bivirkninger blevet rapporteret: Almindelig: mavesmerter; diarré; flatulens; træthedsfornemmelse.
Ikke almindelig: stigninger i nogle leverlaboratorieundersøgelser (transaminaser) eller muskelfunktion (CK); hoste; dårlig fordøjelse; mavepine; kvalme; ledsmerter; muskelspasmer; nakke smerter; nedsat appetit; smerter; brystsmerter; hedeture; forhøjet blodtryk.
Derudover er følgende bivirkninger blevet rapporteret, da medicinen blev brugt sammen med en statin:
Almindelig: stigninger i nogle laboratorietests af leverfunktion (transaminaser); hovedpine; muskelsmerter; muskel ømhed eller svaghed.
Ikke almindelig: prikkende fornemmelse; tør mund; kløe; udslæt; urticaria; rygsmerte; muskelsvaghed; smerter i arme og ben; usædvanlig træthed eller svaghed hævelse især i hænder og fødder. Ved anvendelse sammen med fenofibrat er følgende almindelige bivirkning blevet rapporteret: mavesmerter.
Derudover er følgende bivirkninger blevet rapporteret ved generel brug af medicinen:
svimmelhed muskelsmerter; leverproblemer allergiske reaktioner, herunder hududslæt og nældefeber; forhøjet rødt udslæt, undertiden med målformede læsioner (erythema multiforme); muskelsmerter, muskelsømhed eller svaghed muskelvævsskade; galdeblæresten eller betændelse i galdeblæren (som kan forårsage mavesmerter, kvalme, opkastning) betændelse i bugspytkirtlen ofte ledsaget af alvorlige mavesmerter; forstoppelse; reduktion i antallet af blodlegemer, som kan forårsage blå mærker / blødninger (trombocytopeni); prikkende fornemmelse depression; usædvanlig træthed eller svaghed stakåndet. Tal med din læge eller apotek, hvis du får bivirkninger, herunder mulige bivirkninger, som ikke er nævnt i denne indlægsseddel
Udløb og opbevaring
- Opbevar denne medicin utilgængeligt for børn.
- Brug ikke dette lægemiddel efter den udløbsdato, der står på kartonen eller beholderen efter "EXP". Udløbsdatoen refererer til den sidste dag i den pågældende måned.
- Opbevar ikke ZETIA over 30 ° C.
Blister: Opbevares i den originale beholder.
Flasker: Hold flasken tæt lukket. Disse foranstaltninger hjælper med at beskytte medicinen mod fugt.
Smid ikke medicin via spildevand eller husholdningsaffald. Spørg din apotek om, hvordan du skal smide medicin, du ikke længere bruger. Dette vil hjælpe med at beskytte miljøet.
Hvad ZETIA indeholder
- Det aktive stof er ezetimibe Hver tablet indeholder 10 mg ezetimibe.
- Øvrige indholdsstoffer er: lactosemonohydrat, mikrokrystallinsk cellulose, povidon, croscarmellosenatrium, natriumlaurilsulfat, magnesiumstearat.
Beskrivelse af hvordan ZETIA ser ud og pakningens indhold
ZETIA tabletter er hvide til råhvide, kapselformede tabletter præget med "414" på den ene side.
Pakningsstørrelser: 7, 10, 14, 20, 28, 30, 50, 98, 100 eller 300 tabletter i trykblister eller enhedsdosisblister med lamina lift;
84 eller 90 tabletter i blister, der kan åbnes;
50, 100 eller 300 tabletter i push-open blister pr. Enhedsdosis; 100 tabletter på flasker.
Ikke alle pakningsstørrelser er nødvendigvis markedsført
Indlægsseddel: AIFA (Italian Medicines Agency). Indhold offentliggjort i januar 2016. De foreliggende oplysninger er muligvis ikke opdaterede.
For at få adgang til den mest opdaterede version er det tilrådeligt at få adgang til webstedet AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttige oplysninger.
01.0 LÆGEMIDLETS NAVN
ZETIA 10 MG TABLETTER
02.0 KVALITATIV OG KVANTITATIV SAMMENSÆTNING
Hver tablet indeholder 10 mg ezetimibe.
Hjælpestof (er): Hver tablet indeholder 55 mg lactosemonohydrat.
Den fulde liste over hjælpestoffer findes i afsnit 6.1.
03.0 LÆGEMIDDELFORM
Tablet.
Hvide til råhvide kapselformede tabletter med "414" præget på den ene side.
04.0 KLINISKE OPLYSNINGER
04.1 Terapeutiske indikationer
Primær hyperkolesterolæmi
ZETIA, givet med en HMG-CoA-reduktasehæmmer (statin), er angivet som supplement til diæt hos patienter med primær hyperkolesterolæmi (heterozygot familiær og ikke-familiær), som ikke er tilstrækkeligt kontrolleret på statiner alene.
Monoterapi med ZETIA er indiceret som et supplement til diæt hos patienter med primær hyperkolesterolæmi (heterozygot familiær og ikke-familiær), for hvem statiner anses for upassende eller ikke tolereres.
Homozygot familiel hyperkolesterolæmi (homozygot IF)
ZETIA administreret med et statin er indiceret som tillægsbehandling til kosten hos patienter med homozygot familiær hyperkolesterolæmi. Patienten kan også blive udsat for yderligere terapeutiske foranstaltninger (f.eks. LDL -aferese).
Familiær sitosterolæmi homozygot (Phytosterolæmi)
ZETIA er angivet som et supplement til diæt hos patienter med homozygot familiær sitosterolæmi.
En gavnlig effekt af ZETIA på kardiovaskulær morbiditet og dødelighed er endnu ikke påvist.
04.2 Dosering og indgivelsesmåde
Patienten bør følge en tilstrækkelig kolesterolsænkende diæt og fortsætte kosten under behandling med ZETIA.
Lægemidlet skal administreres oralt. Den anbefalede dosis er en ZETIA 10 mg tablet en gang dagligt. ZETIA kan administreres når som helst på dagen, uanset måltider.
Når ZETIA tilføjes til en statin, skal behandlingen fortsættes med den almindelige startdosis, der er angivet for den specifikke statin, eller den højere tidligere foreskrevne dosis skal fortsat anvendes. I denne omstændighed bør databladet for den pågældende statin konsulteres.
Samtidig administration med galdesyresekvestranter
Administration af ZETIA bør ske enten ≥2 timer før eller ≥4 timer efter administration af et galdesyresekvestreringsmiddel.
Brug til ældre
Ingen dosisjustering er nødvendig hos ældre patienter (se pkt. 5.2).
Anvendelse til pædiatriske patienter
Behandlingsstart skal udføres under tilsyn af en specialist.
Unge ≥10 år (pubertetsstatus: drenge i Tanner fase II og højere og piger, der har været postmenarche i mindst et år): ingen dosisjustering er nødvendig (se afsnit 5.2). Den kliniske erfaring hos pædiatriske og unge patienter (10 til 17 år) er imidlertid begrænset.
Når ZETIA gives sammen med simvastatin, bør doseringsinstruktioner for simvastatin konsulteres.
Børn
Anvendelse ved nedsat leverfunktion
Ingen dosisjustering er nødvendig ved let (Child-Pugh score 5 til 6) nedsat leverfunktion. Behandling med ZETIA anbefales ikke til patienter med moderat (Child-Pugh score 7 til 9) eller alvorlig (Child-Pugh score> 9), ( se afsnit 4.4 og 5.2).
Anvendes ved nedsat nyrefunktion
Ingen dosisjustering er nødvendig ved nedsat nyrefunktion (se pkt. 5.2).
04.3 Kontraindikationer
Overfølsomhed over for det aktive stof eller over for et eller flere af hjælpestofferne.
Når ZETIA gives sammen med en statin, henvises til det tekniske datablad for medicinen.
ZETIA -behandling givet sammen med en statin er kontraindiceret under graviditet og amning.
ZETIA administreret sammen med en statin er kontraindiceret hos patienter med aktiv leversygdom eller med vedvarende og ubestemt forhøjede serumtransaminaseværdier.
04.4 Særlige advarsler og passende forholdsregler ved brug
Når ZETIA gives sammen med en statin, henvises til det tekniske datablad for medicinen.
Leverenzymer
I kontrollerede kliniske forsøg, hvor patienter blev behandlet med ZETIA og et statin, blev der observeret på hinanden følgende stigninger i transaminaser (≥3 gange den øvre grænse for normal [ULN]). Hvis ZETIA administreres samtidigt med en statin, skal der udføres leverfunktionstest ved behandlingens start og som anbefalet for statinen (se pkt. 4.8).
Skelet muskel
Tilfælde af myopati og rabdomyolyse er blevet rapporteret efter markedsføring med ZETIA.De fleste patienter, der udviklede rabdomyolyse, var i samtidig behandling med ZETIA og en statin.Rhabdomyolyse er imidlertid rapporteret meget sjældent med ZETIA monoterapi og meget sjældent med tilføjelse af ZETIA til andre midler, der vides at være forbundet med en øget risiko for rabdomyolyse. Hvis der er mistanke om myopati på grund af muskelsymptomer eller bekræftes af kreatinfosfokinase (CPK) niveauer> 10 gange den øvre normale grænse, ved at tage ZETIA, ethvert statin og ethvert andet lægemiddel af denne type, som samtidig medicin bør seponeres Alle patienter, der påbegynder behandling med ZETIA, bør informeres om risikoen for myopati og rådes til straks at rapportere uforklarlige muskelsmerter, ømhed eller svaghed (se pkt. 4.8).
Leverinsufficiens
På grund af de ukendte virkninger af den øgede eksponering for ezetimibe hos patienter med moderat eller svært nedsat leverfunktion, anbefales ZETIA ikke (se pkt. 5.2).
Pædiatriske patienter (10 til 17 år)
Sikkerheden og effekten af ZETIA, som blev administreret sammen med simvastatin hos patienter i alderen 10 til 17 år med heterozygot familiær hyperkolesterolæmi, blev evalueret i et kontrolleret klinisk studie med unge drenge (Tanner-fase II og højere) og hos piger i postmenarche i mindst et år.
I denne begrænsede kontrollerede undersøgelse var der generelt ingen effekt på seksuel vækst eller modning hos unge drenge eller piger eller nogen indvirkning på menstruationscyklussens længde hos piger. Imidlertid er virkningen af ezetimib over en behandlingsperiode> 33 uger på vækst eller kønsmodning ikke undersøgt (se pkt. 4.2 og 4.8).
Sikkerheden og effekten af ZETIA, der administreres samtidig med simvastatindoser på over 40 mg dagligt, er ikke undersøgt hos pædiatriske patienter i alderen 10 til 17 år.
ZETIA er ikke undersøgt hos patienter under 10 år eller hos præmenarche-piger. (se afsnit 4.2 og 4.8).
Langtidseffekten af ZETIA-terapi til at reducere sygdom og dødelighed hos voksne er ikke undersøgt hos patienter under 17 år.
Bundler
Sikkerheden og effekten af ZETIA administreret med fibrater er ikke fastslået.
Hvis der er mistanke om cholelithiasis hos en patient, der behandles med ZETIA og fenofibrat, er galdeblæreundersøgelser indiceret, og behandlingen bør afbrydes (se pkt. 4.5 og 4.8).
Cyclosporin
Der skal udvises forsigtighed, når behandling med ZETIA påbegyndes i terapeutiske omgivelser, herunder brug af cyclosporin. Koncentrationer af cyclosporin bør monitoreres hos patienter behandlet med ZETIA og cyclosporin (se pkt. 4.5).
Antikoagulantia
Hvis ZETIA tilsættes warfarin, et andet kumarinantikoagulant eller fluindion, bør International Normalized Ratio (INR) overvåges passende (se afsnit 4.5).
Hjælpestoffer
Patienter med sjældne problemer med galactoseintolerance, Lapp-lactasemangel eller glucose-galactosemalabsorption bør ikke tage denne medicin.
04.5 Interaktioner med andre lægemidler og andre former for interaktion
Interaktionsundersøgelser er kun blevet udført hos voksne.
I prækliniske undersøgelser viste det sig, at ezetimibe ikke inducerede de cytochrom P450 -enzymer, der var involveret i stofskifte. Der blev ikke observeret klinisk signifikante farmakokinetiske interaktioner mellem ezetimibe og lægemidler, der er genstand for metabolisme af cytochromer P450 1A2, 2D6, 2C8, 2C9 og 3A4 eller N-acetyltransferase.
I kliniske interaktionsstudier havde ezetimibe ingen effekt på farmakokinetikken af dapson, dextromethorphan, digoxin, orale præventionsmidler (ethinylestradiol og levonorgestrel), glipizid, tolbutamid eller midazolam under samtidig administration. Cimetidin, administreret sammen med ezetimibe, havde ingen effekt på biotilgængeligheden af ezetimib.
Antacida : Samtidig administration af antacida nedsatte absorptionen af ezetimib, men havde ingen effekt på biotilgængeligheden af ezetimib. Dette fald i absorption anses ikke for at være klinisk signifikant.
Kolestyramin: Samtidig administration af cholestyramin reducerede middelarealet under kurven (AUC) for total ezetimib (ezetimibe + ezetimibe-glucuronid) med ca. 55%. Den yderligere reduktion i lipoproteinkolesterol med lav densitet (LDL-C) på grund af tilsætning af ZETIA til cholestyramin kan reduceres ved denne interaktion (se pkt.4.2).
Bundler : Hos patienter behandlet med fenofibrat og ZETIA bør læger overveje den mulige risiko for cholelithiasis og galdeblæresygdom (se pkt. 4.4 og 4.8).
Hvis der er mistanke om cholelithiasis hos en patient behandlet med ZETIA og fenofibrat, er galdeblæreundersøgelser indiceret, og behandlingen bør afbrydes (se pkt. 4.8).
Samtidig administration af fenofibrat eller gemfibrozil øgede moderat de samlede koncentrationer af ezetimib (henholdsvis ca. 1,5 og 1,7 gange).
Samtidig administration af ZETIA med andre fibrater er ikke undersøgt.
Fibrater kan øge udskillelsen af kolesterol i galden, hvilket kan føre til cholelithiasis.I dyreforsøg øgede ezetimibe undertiden kolesterolet i galdeblæren galde, men ikke hos alle arter (se pkt. 5.3) Risiko for litogenicitet forbundet med terapeutisk brug af ZETIA ikke kan udelukkes.
Statiner : Der blev ikke observeret klinisk signifikante farmakokinetiske interaktioner, når ezetimibe blev administreret samtidigt med atorvastatin, simvastatin, pravastatin, lovastatin, fluvastatin eller rosuvastatin.
Ciclosporin: I en undersøgelse af otte post-nyretransplanterede patienter med kreatininclearance> 50 ml / min ved stabile doser cyclosporin resulterede administration af en enkelt 10 mg dosis ZETIA i en 3,4 gange stigning (interval 2, 3-7,9 gange) af den gennemsnitlige AUC for total ezetimibe sammenlignet med en sund kontrolpopulation fra en anden undersøgelse (n = 17) behandlet med ezetimibe alene.I en anden undersøgelse viste en nyretransplanteret patient med alvorlig nyreinsufficiens, når den blev behandlet med cyclosporin og flere andre lægemidler, eksponering for total ezetimibe 12 gange højere end for relative kontroller behandlet med ezetimibe alene. I en crossover-undersøgelse med to perioder hos tolv raske individer resulterede daglig administration af 20 mg ezetimibe i 8 dage med en enkelt dosis på 100 mg cyclosporin på dag 7 i en gennemsnitlig stigning på 15% i AUC for ciclosporin (fra 10% fald til en stigning på 51%) sammenlignet med en enkelt dosis på 100 mg cyclosporin alene. Der er ikke udført en kontrolleret undersøgelse af effekten af samtidig administration af ezetimib på cyclosporin -eksponering hos nyretransplanterede patienter. Der skal udvises forsigtighed, når behandling med ZETIA påbegyndes i forbindelse med terapier, herunder brug af cyclosporin. Koncentrationer af cyclosporin bør monitoreres hos patienter behandlet med ZETIA og cyclosporin (se pkt. 4.4).
Antikoagulantia: Samtidig administration af ezetimibe (10 mg én gang dagligt) havde ingen signifikant effekt på warfarins biotilgængelighed og protrombintid i en undersøgelse af tolv raske voksne mænd. Der har imidlertid været post-marketing rapporter om stigninger i International Normalized Ratio (INR) hos patienter, der havde tilføjet ZETIA til warfarin eller fluindion. Hvis ZETIA tilsættes warfarin, et andet kumarin -antikoagulant eller fluindion, bør INR -værdien overvåges tilstrækkeligt (se pkt. 4.4).
04.6 Graviditet og amning
Samtidig administration af ZETIA og et statin er kontraindiceret under graviditet og amning (se pkt. 4.3), se det specifikke statindatablad.
Graviditet :
ZETIA bør kun administreres til gravide, når det er klart nødvendigt. Der foreligger ingen kliniske data om brug af ZETIA under graviditet. Dyrestudier om brugen af ezetimibe alene har ikke vist tegn på direkte eller indirekte skadelige virkninger på graviditet, embryoføtal udvikling, fødsel eller postnatal udvikling (se afsnit 5.3).
Fodringstid :
ZETIA bør ikke anvendes under amning. Undersøgelser med rotter har vist, at ezetimibe udskilles i mælk. Det vides ikke, om ezetimibe udskilles i modermælk.
04.7 Virkninger på evnen til at føre motorkøretøj og betjene maskiner
Der er ikke udført undersøgelser af evnen til at føre motorkøretøj eller betjene maskiner, men ved kørsel med biler eller brug af maskiner skal det tages i betragtning, at der er rapporteret om svimmelhed.
04.8 Bivirkninger
Kliniske undersøgelser
I kliniske forsøg med op til 112 ugers varighed blev ZETIA 10 mg / dag administreret til 2.396 patienter alene, med en statin til 11.308 patienter eller med fenofibrat til 185 patienter. Bivirkninger var normalt milde og forbigående. Den samlede forekomst af bivirkninger mellem ZETIA og placebo var ens. På samme måde var afbrydelsesgraden på grund af bivirkninger sammenlignelig mellem ZETIA og placebo.
ZETIA givet alene eller i kombination med en statin:
Følgende bivirkninger blev observeret hos patienter behandlet med ZETIA (N = 2.396) og med en højere forekomst end placebo (N = 1.159) eller hos patienter behandlet med ZETIA i kombination med et statin (N = 11.308) og med en forekomst højere end med statinen alene givet (N = 9.361):
Frekvenser defineres som: meget almindelige (≥1 / 10); almindelig (≥1 / 100 til
ZETIA administreres samtidig med fenofibrat:
Mave -tarmlidelser: mavesmerter (almindelige).
I et multicenter, dobbeltblindet, placebokontrolleret klinisk studie med patienter med blandet hyperlipidæmi blev 625 patienter behandlet i op til 12 uger og 576 patienter i op til 1 år. I denne undersøgelse gennemførte 172 patienter behandlet med ZETIA og fenofibrat 12 ugers behandling og 230 patienter behandlet med ZETIA og fenofibrat (inklusive 109 behandlet med ZETIA alene i de første 12 uger) gennemførte 1 års behandling. Undersøgelsen var ikke designet til at sammenligne behandlingsgrupper for sjældne hændelser. Incidensen (95% CI) for klinisk relevante stigninger i serumtransaminaser (> 3 X ULN, på hinanden følgende) var 4,5% og 2,7% for fenofibrat alene og for ZETIA administreret sammen med fenofibrat, justeret til henholdsvis eksponering for behandling. satser for cholecystektomi var henholdsvis 0,6% og 1,7% for fenofibratmonoterapi og for ZETIA samtidig administreret med fenofibrat (se pkt. 4.4 og 4.5).
Pædiatriske patienter (10 til 17 år)
I en undersøgelse af unge patienter (10 til 17 år) med heterozygot familiær hyperkolesterolæmi (n = 248) blev stigninger i ALAT og / eller ASAT (≥ 3 X ULN, på hinanden følgende) observeret hos 3% af patienterne (4 patienter) i gruppen ezetimibe / simvastatin mod 2% af patienterne (2 patienter) i gruppen simvastatin som monoterapi; procentdelene af CPK -stigninger (≥10 X ULN) var henholdsvis 2% (2 patienter) og 0%. Der er ikke rapporteret tilfælde af myopati.
Denne undersøgelse var ikke egnet til at sammenligne sjældne lægemiddelbivirkninger.
Diagnostiske undersøgelser
I monoterapikontrollerede kliniske forsøg var forekomsten af klinisk vigtige stigninger i serumtransaminaser (ALAT og / eller ASAT ≥ 3 X ULN, på hinanden følgende værdier) ens mellem ZETIA (0,5%) og placebo (0 I samtidig administrationsstudier var forekomsten 1,3% for patienter behandlet med ZETIA i kombination med et statin og 0,4% for patienter behandlet med et statin alene. Forhøjelser var generelt asymptomatiske, ikke forbundet med kolestase og vendte tilbage til baseline efter afbrydelse af behandlingen eller med fortsat behandling (se pkt.4.4) .
I kliniske forsøg blev CPK -værdier> 10 X ULN rapporteret for 4 af 1.674 (0,2%) patienter behandlet med ZETIA alene sammenlignet med 1 af 786 (0,1%) patienter, der fik placebo og for 1 af 917 patienter (0,1%) co -administreret med ZETIA og et statin sammenlignet med 4 ud af 929 patienter (0,4%) behandlet med et statin alene. Der var ingen overdreven myopati eller rabdomyolyse forbundet med ZETIA sammenlignet med dets kontrolarm (placebo eller statin alene). (se afsnit 4.4.)
Efter markedsføring erfaring
Følgende yderligere bivirkninger er blevet rapporteret efter markedsføringen: Da disse bivirkninger er blevet identificeret ud fra spontane rapporter, kendes deres sande frekvenser ikke og kan ikke estimeres.
Blod- og lymfesystem: trombocytopeni
Nervesystemet: svimmelhed; paræstesi
Åndedrætsorganer, thorax og mediastinum: dyspnø
Gastrointestinale lidelser: pancreatitis; forstoppelse
Hud og subkutan væv: erythema multiforme
Muskuloskeletale og bindevævssygdomme: myalgi; myopati / rabdomyolyse (se pkt.4.4)
Generelle lidelser og tilstande på administrationsstedet: asteni
Immunsystemet: overfølsomhed, herunder udslæt, nældefeber, anafylaksi og angioødem
Lever og galdeveje: hepatitis; cholelithiasis; cholecystitis
Psykiatriske lidelser: Depression
04.9 Overdosering
I kliniske undersøgelser blev administration af ezetimibe 50 mg / dag til 15 raske personer i op til 14 dage eller 40 mg / dag til 18 patienter med primær hyperkolesterolæmi i op til 56 dage generelt godt tolereret. Hos dyr blev der ikke observeret toksicitet efter enkelt orale doser på 5.000 mg / kg ezetimibe hos rotter og mus og 3.000 mg / kg hos hunde.
Et par tilfælde af overdosering med ZETIA er blevet rapporteret; de fleste af dem var ikke forbundet med negative oplevelser. De rapporterede negative oplevelser var ikke alvorlige. I tilfælde af overdosering bør symptomatiske og støttende foranstaltninger anvendes.
05.0 FARMAKOLOGISKE EGENSKABER
05.1 Farmakodynamiske egenskaber
Farmakoterapeutisk gruppe: andre lipidmodificerende stoffer. ATC -kode: C10AX09
ZETIA er en del af en ny klasse af lipidsænkende stoffer, der selektivt hæmmer tarmoptagelsen af kolesterol og beslægtede plantesteroler.ZETIA er aktivt oralt og har en specifik virkningsmekanisme, der adskiller sig fra andre klasser af kolesterolsænkende stoffer (f.eks. : statiner, galdesyresekvestranter [harpikser], fibrinsyrederivater og plantestanoler). ezetimibens molekylære mål er steroltransportøren, Niemann-Pick C1-Like 1 (NPC1L1), der er ansvarlig for tarmoptagelseskolesterol og phytosteroler.
Ezetimibe er lokaliseret på børstekanten af tyndtarmen og hæmmer absorptionen af kolesterol, hvilket forårsager et fald i passage af tarmkolesterol til leveren.
Statiner reducerer syntesen af kolesterol i leveren, og disse to forskellige mekanismer producerer tilsammen en komplementær reduktion i kolesterol. I et 2-ugers klinisk studie med 18 hyperkolesterolæmiske patienter hæmmede ezetimibe tarmkolesterolabsorptionen med 54% sammenlignet med placebo.
En række prækliniske undersøgelser blev udført for at bestemme selektiviteten af ezetimib til at hæmme absorptionen af kolesterol. Ezetimibe hæmmede absorptionen af [14C] -kolesterol uden effekt på absorptionen af triglycerider, fedtsyrer, galdesyrer, progesteron, ethinylestradiol eller de fedtopløselige vitamin A og D.
Epidemiologiske undersøgelser har fastslået, at kardiovaskulær morbiditet og dødelighed varierer direkte med totalt kolesterol- og LDL -kolesteroltal og omvendt med HDL -kolesterolniveauer. En gavnlig effekt af ZETIA på kardiovaskulær morbiditet og dødelighed er endnu ikke påvist.
KLINISKE STUDIER
I kontrollerede kliniske forsøg, ZETIA givet både alene og i kombination med et statin reducerede signifikant totalt (C-total) kolesterol, lavdensitets lipoprotein (LDL-C) kolesterol, apolipoprotein B (Apo B) og triglycerider (TG) og øget high-density lipoprotein (HDL-C) kolesterol hos patienter med hyperkolesterolæmi.
Primær hyperkolesterolæmi
I et 8-ugers dobbeltblindet, placebokontrolleret studie, 769 patienter med hyperkolesterolæmi, der allerede var på statinmonoterapi, og som ikke lykkedes at nå LDL-C-mål ifølge National Cholesterol Education Program (NCEP) (siden 2, 6 til 4,1 mmol / L [100 til 160 mg / dL afhængigt af baseline-karakteristika) blev randomiseret til at modtage enten ZETIA 10 mg eller placebo ud over deres eksisterende statinbehandling.
Blandt statinbehandlede patienter, der ikke nåede LDL-C-mål ved baseline (≈82%), opnåede signifikant flere patienter randomiseret til ZETIA undersøgelsens endepunkt LDL-C-mål sammenlignet med patienter randomiseret til placebo, henholdsvis 72%og 19%. Tilsvarende reduktioner i LDL-C var signifikant forskellige (25% og 4% for ZETIA vs. placebo, henholdsvis). Desuden reducerede ZETIA, tilføjet til statinbehandling, signifikant total-C, Apo B, TG og øget HDL-C sammenlignet med placebo.
ZETIA eller placebo tilføjet til statinbehandling reducerede median C-reaktivt protein med henholdsvis 10% eller 0% fra baseline.
I to 12 ugers placebokontrollerede, randomiserede, dobbeltblinde 1719 patienter med primær hyperkolesterolæmi reducerede ZETIA 10 mg signifikant total-C (13%), LDL-C (19%), l "Apo B (14% ) og TG (8%) og øget HDL-C (3%) sammenlignet med placebo. ZETIA havde heller ingen effekt på plasmakoncentrationer af fedtopløselige vitamin A, D og E over tid med protrombin og, ligesom andre lipidsænkende lægemidler , ændrede ikke produktionen af adrenokortikosteroider.
I et multicenter, dobbeltblindet, kontrolleret klinisk forsøg (ENHANCE) blev 720 patienter med heterozygot familiær hyperkolesterolæmi randomiseret til at modtage ezetimibe 10 mg i kombination med simvastatin 80 mg (n = 357) eller simvastatin 80 mg (n = 363) til 2 flere år. Undersøgelsens primære formål var at undersøge effekten af kombinationsbehandlingen ezetimibe / simvastatin på tykkelsen af tunica intima og medier (IMT) af halspulsåren sammenlignet med simvastatin alene. Virkningen af denne markør er endnu ikke påvist. Surrogat for kardiovaskulær morbiditet og dødelighed.
Det primære endepunkt, den gennemsnitlige IMT-ændring af alle seks halspulsegmenter, var ikke signifikant forskellig (p = 0,29) mellem de to behandlingsgrupper baseret på B-mode ultralydsmålinger. Med ezetimibe 10 mg i kombination med simvastatin 80 mg eller simvastatin 80 mg alene steg tykkelsen af intima og medial tunika med henholdsvis 0,0111 mm og 0,0058 mm i løbet af den 2-årige undersøgelsesvarighed (ved baseline var den gennemsnitlige carotis-IMT-måling henholdsvis Henholdsvis 0,68 mm og 0,69 mm).
Ezetimibe 10 mg i kombination med simvastatin 80 mg reducerede LDL-C, total-C, Apo B og TG betydeligt mere end simvastatin 80 mg. For de to behandlingsgrupper var stigningen i procent i C -HDL ens. Bivirkninger rapporteret med ezetimibe 10 mg i kombination med simvastatin 80 mg var i overensstemmelse med dets kendte sikkerhedsprofil.
Kliniske undersøgelser af pædiatriske patienter (10 til 17 år)
I et multicenter, dobbeltblindet, kontrolleret studie, 142 drenge (Tanner fase II og højere) og 106 postmenarche piger, 10 til 17 år (gennemsnitsalder 14,2 år) med heterozygot familiær hyperkolesterolæmi (IF heterozygot) med baseline LDL-C værdier mellem 4,1 og 10,4 mmol / L blev randomiseret til ZETIA 10 mg samtidig administreret med simvastatin (10, 20 eller 40 mg) eller simvastatin (10, 20 eller 40 mg) alene i 6 uger, ZETIA og simvastatin 40 mg co -administreret eller simvastatin 40 mg alene i de næste 27 uger, og derefter administreret ZETIA og simvastatin (10 mg, 20 mg eller 40 mg) åben etiket i 20 uger.
I uge 6 reducerede ZETIA samtidig med simvastatin (alle doser) signifikant total C (38% vs 26%), LDL-C (49% vs 34%), Apo B (39% vs 27%) og ikke- HDL-C (47% vs 33%) versus simvastatin alene (alle doser). Resultaterne var ens mellem de to behandlingsgrupper for henholdsvis TG og HDL-C (-17% vs -12% og +7% vs +6% .) I uge 33 var resultaterne i overensstemmelse med dem i uge 6, og signifikant flere patienter på ZETIA og simvastatin 40 mg (62%) opnåede et ideelt terapeutisk mål ifølge NCEP AAP (
Sikkerheden og effekten af ZETIA, der administreres samtidigt med simvastatindoser større end 40 mg dagligt, er ikke undersøgt hos pædiatriske patienter i alderen 10 til 17 år. Effekt er ikke undersøgt hos patienter under 17 år. Langtidsbehandling med ZETIA at reducere sygelighed og dødelighed i voksenalderen.
Homozygot familiel hyperkolesterolæmi (homozygot IF)
Et 12-ugers, dobbeltblindet, randomiseret studie inkluderede 50 patienter med en klinisk og / eller genotypisk diagnose af homozygot IF, der blev behandlet med atorvastatin eller simvastatin (40 mg) med eller uden samtidig LDL-aferese. ZETIA givet med atorvastatin (40 eller 80 mg) eller simvastatin (40 eller 80 mg) reducerede LDL-C betydeligt med 15% sammenlignet med at øge dosis af simvastatin eller atorvastatin som monoterapi fra 40 til 80 mg.
Homozygot sitosterolæmi (phytosterolæmi)
I et 8 ugers dobbeltblindet, placebokontrolleret studie blev 37 patienter med homozygot sitosterolæmi randomiseret til at modtage ZETIA 10 mg (n = 30) eller placebo (n = 7). Nogle patienter blev behandlet med andre lægemidler (f.eks. Statiner, harpikser). ZETIA reducerede signifikant de to vigtigste plantesteroler, sitosterol og campesterol, med henholdsvis 21% og 24% fra baseline. Virkningerne af faldende sitosterolniveauer på sygelighed og dødelighed i denne population er ukendte.
Aortastenose
Simvastatin og Ezetimibe til behandling af aortastenose (SEAS) var et multicenter, dobbeltblindet, placebokontrolleret studie med en medianvarighed på 4,4 år hos 1.873 patienter med asymptomatisk aortastenose (AS), dokumenteret af en maksimal aortastrømningshastighed målt af Doppler mellem 2,5 og 4,0 m / s. Kun patienter blev registreret, for hvem statinbehandling ikke blev anset for nødvendig for at reducere risikoen for aterosklerotisk hjerte -kar -sygdom. Patienter blev randomiseret i forholdet 1: 1 til at modtage placebo eller ezetimibe 10 mg og simvastatin 40 mg dagligt i samtidig administration.
Det primære endepunkt var sammensætningen af større kardiovaskulære hændelser (MCE) bestående af kardiovaskulær død, kirurgisk aortaklappeskift (AVR), kongestiv hjertesvigt. (CHF) som følge af progression af AS, ikke-dødeligt myokardieinfarkt, koronar bypass-transplantat (CABG), perkutan koronar intervention (PCI), hospitalsindlæggelse for ustabil angina og ikke-hæmoragisk slagtilfælde. De vigtigste sekundære endepunkter var sammensat af undersæt af hændelseskategorierne for det primære endepunkt.
Sammenlignet med placebo reducerede ezetimibe / simvastatin 10/40 mg ikke signifikant risikoen for MCE. Det primære resultat forekom hos 333 patienter (35,3%) i ezetimibe / simvastatin -gruppen og hos 355 patienter (38,2%) i placebogruppen (hazard ratio i ezetimibe / simvastatin -gruppen, 0,96; konfidensinterval 95%, 0,83 til 1,12; p = 0,59) Aortaklappeskift blev udført hos 267 patienter (28,3%) i ezetimibe / simvastatin -gruppen og hos 278 patienter (29,9%) i placebogruppen (hazard ratio, 1,00; 95%CI, 0,84 til 1,18; p = 0,97) Færre patienter havde iskæmiske kardiovaskulære hændelser i ezetimibe / simvastatin -gruppen (n = 148) sammenlignet med placebogruppen (n = 187) (hazard ratio, 0,78; 95% CI, 0,63 til 0,97; p = 0,02), hovedsageligt pga. til det mindre antal patienter, de havde gennemgået koronar bypass -podning.
Kræft forekom hyppigere i gruppen ezetimibe / simvastatin (105 versus 70, p = 0,01). Den kliniske relevans af denne observation er usikker. I en metaanalyse, der omfattede foreløbige resultater fra to store, langsigtede, igangværende undersøgelser med ezetimibe / simvastatin (n = 10.319 aktivt behandlet, 10.298 behandlet med kontrol; patientår = 18.246 aktivt behandlet, 18.255 behandlet med kontrol) var der ingen stigning i kræftforekomsten (313 aktiv behandling, 326 kontrol); risikoforhold, 0,96; 95% konfidensinterval, 0,82 til 1,12; p = 0,61).
05.2 "Farmakokinetiske egenskaber
Absorption : Efter oral administration absorberes ezetimibe hurtigt og konjugeres i vid udstrækning til det farmakologisk aktive phenoliske glucuronid (ezetimibe-glucuronid). Gennemsnitlig maksimal plasmakoncentration (Cmax) observeres inden for 1-2 timer for ezetimibe-glucuronid og 4-12 timer for ezetimibe absolut biotilgængelighed af ezetimib kan ikke bestemmes, da forbindelsen er praktisk talt uopløselig i et vandigt medium, der er egnet til injektion.
Samtidig madindgift (måltider med højt fedtindhold eller fedtfattig mad) havde ingen indvirkning på den orale biotilgængelighed af ezetimib ved administration som ZETIA 10 mg tabletter. ZETIA kan gives med eller uden måltider.
Fordeling : Ezetimibe og ezetimibe-glucuronid er henholdsvis 99,7% og 88-92% bundet til humane plasmaproteiner.
Biotransformation : Ezetimibe metaboliseres primært i tyndtarmen og leveren via glucuronidkonjugering (en fase II -reaktion) med efterfølgende galdeudskillelse. Minimal oxidativ metabolisme (en fase I-reaktion) blev observeret i alle evaluerede arter. Ezetimibe og ezetimib-glucuronid er de vigtigste lægemiddelderivatforbindelser, der findes i plasma, hvilket tegner sig for cirka 10-20% og 80-90% af det samlede antal af det tilstedeværende lægemiddel. i henholdsvis plasmaet. Både ezetimibe og ezetimibe-glucuronid fjernes langsomt fra plasma med tegn på signifikant enterohepatisk cykling. Halveringstiden for ezetimib og ezetimibe-glucuronid er cirka 22 timer.
Eliminering : Efter oral administration af 14C ezetimibe (20 mg) til mennesker var total ezetimibe cirka 93% af den samlede plasma radioaktivitet. Ca. 78% og 11% af den administrerede radioaktivitet blev genfundet i henholdsvis fæces og urin over en 10-dages prøveopsamlingsperiode. Efter 48 timer var der ingen påviselige niveauer af radioaktivitet i plasmaet.
Særlige populationer:
Pædiatriske patienter
Ezetimibs absorption og metabolisme er ens hos børn og unge (10 til 18 år) og voksne Der er ingen farmakokinetiske forskelle mellem unge og voksne baseret på total ezetimibe. Farmakokinetiske data i den pædiatriske population
Geriatriske patienter
Plasmakoncentrationer af total ezetimib er cirka dobbelt så høje hos ældre (≥ 65 år) som hos unge (18-45 år). LDL-C-reduktion og sikkerhedsprofil er sammenlignelige mellem ældre og yngre personer behandlet med ZETIA Derfor er der ingen dosering justering er nødvendig hos ældre.
Leverinsufficiens
Efter administration af en enkelt 10 mg dosis ezetimibe steg den gennemsnitlige AUC for total ezetimibe cirka 1,7 gange hos patienter med let nedsat leverfunktion (Child Pugh score 5 eller 6) sammenlignet med raske forsøgspersoner. I en 14-dages multiple dosis (10 mg / dag) undersøgelse hos patienter med moderat nedsat leverfunktion (Child Pugh-score 7 til 9) steg middelværdien af AUC for total ezetimibe cirka 4 gange om dagen 1 og på dag 14 sammenlignet med raske forsøgspersoner. Ingen dosisjustering er nødvendig hos patienter med let nedsat leverfunktion. På grund af de ukendte virkninger af øget eksponering for ezetimibe hos patienter med moderat eller svært nedsat leverfunktion (Child Pugh score> 9), anbefales ZETIA ikke til disse patienter (se pkt. 4.4).
Nyresvigt
Efter en enkelt dosis på 10 mg ezetimibe til patienter med alvorlig nyresygdom (n = 8; gennemsnitlig CrCl ≤30 ml / min / 1,73 m2) steg den gennemsnitlige AUC for total ezetimibe med cirka 1,5 gange sammenlignet med raske forsøgspersoner (n = 9). Dette resultat anses ikke for klinisk signifikant. Ingen dosisjustering er nødvendig for patienter med nedsat nyrefunktion.
En yderligere patient i denne undersøgelse (efter nyretransplantation og behandlet med multipel lægemiddelbehandling inklusive cyclosporin) havde en 12 gange "eksponering for" total ezetimibe.
Køn
Plasmakoncentrationer af total ezetimibe er lidt højere (ca. 20%) hos kvinder end hos mænd LDL-C-reduktion og sikkerhedsprofil er sammenlignelige mellem mænd og kvinder behandlet med ZETIA. Det er derfor ikke nødvendigt at justere dosis baseret på køn.
05.3 Prækliniske sikkerhedsdata
Kroniske toksicitetsundersøgelser af ezetimib hos dyr identificerede ikke målorganer for toksiske virkninger. Hos hunde behandlet i fire uger med ezetimibe (≥0,03 mg / kg / dag) steg kolesterolkoncentrationen i den cystiske galde med en faktor 2,5 til 3,5. I et etårigt studie med hunde, der blev behandlet med doser på op til 300 mg / kg / dag, blev der imidlertid ikke observeret nogen stigninger i forekomsten af cholelithiasis eller andre hepatobiliære virkninger. Disse dataers betydning for mennesker er ukendt. En risiko for litogen effekt forbundet med den terapeutiske anvendelse af ZETIA kan ikke udelukkes.
I samtidige administrationsundersøgelser med ezetimibe og statiner var de toksiske virkninger hovedsageligt dem, der typisk er forbundet med statiner. Nogle af de toksiske virkninger var mere udtalte end dem, der blev set ved statinbehandling alene. Dette tilskrives farmakokinetiske og farmakodynamiske interaktioner ved samtidig administration. Interaktioner af denne art forekom ikke i kliniske forsøg. Episoder af myopati forekom kun hos rotter efter eksponering for doser, der var flere gange højere end den terapeutiske dosis hos mennesker (ca. 20 gange AUC -niveauet for statiner og 500 til 2000 gange AUC -niveauet for aktive metabolitter).
I en række essays in vivo og in vitro Ezetimibe, givet alene eller sammen med statiner, viste ingen genotoksisk potentiale. Langsigtede kræftfremkaldende test på ezetimibe var negative.
Ezetimibe havde ingen effekt på fertiliteten hos han- eller hunrotter, var ikke teratogent hos rotter eller kaniner, og det påvirkede heller ikke prænatal eller postnatal udvikling. Ezetimibe krydsede placentabarrieren hos drægtige rotter og behandlede kaniner. / dag. Samtidig administration af ezetimibe og statiner var ikke teratogent hos rotter. Hos drægtige kaniner blev der observeret et lille antal skeletdeformiteter (sammensmeltning af thorax- og caudalhvirvler, reduceret antal caudalhvirvler). Administration af ezetimibe i kombination med lovastatin har vist sig at have dødelige virkninger på embryoet.
06.0 LÆGEMIDDELOPLYSNINGER
06.1 Hjælpestoffer
Croscarmellosenatrium
Lactosemonohydrat
Magnesiumstearat
Mikrokrystallinsk cellulose
Povidon (K29-32)
Natriumlaurylsulfat
06.2 Uforenelighed
Ikke relevant.
06.3 Gyldighedsperiode
3 år.
06.4 Særlige opbevaringsforhold
Må ikke opbevares over 30 ° C.
Blister: Opbevares i den originale emballage for at beskytte medicinen mod fugt.
Flasker: Hold flasken tæt lukket for at beskytte medicinen mod fugt.
06.5 Den umiddelbare emballages art og emballagens indhold
Enkeltdosis gennemsigtig blister i polychlortrifluorethylen / PVC svejset til en aluminium / papir / polyester belægning ved hjælp af vinylharpiks. Tabletterne kan ekstraheres ved at løfte aluminium / papir / polyesterfolien
Pakninger med 7, 10, 14, 20, 28, 30, 50, 98, 100 eller 300 tabletter.
Gennemsigtig polychlortrifluorethylen / PVC -blister svejset til en aluminiumsbelægning ved hjælp af vinylharpiks. Tabletterne kan ekstraheres ved at trykke på plastiklommen.
Pakninger med 7, 10, 14, 20, 28, 30, 50, 84, 90, 98, 100 eller 300 tabletter.
Gennemsigtig enkeltdosisblister i polychlortrifluorethylen / PVC belagt med aluminium. Tabletterne kan ekstraheres ved at trykke på plastiklommen.
Pakninger med 50, 100 eller 300 tabletter.
HDPE -flaske med polypropylenhætte, indeholdende 100 tabletter.
Ikke alle pakningsstørrelser er nødvendigvis markedsført.
06.6 Brugsanvisning og håndtering
Ingen særlige instruktioner.
07.0 INDEHAVER AF MARKEDSFØRINGSTILLADELSE
Neopharmed Gentili S.r.l.
Via San Giuseppe Cottolengo, 15 - 20143 Milano
Italien
08.0 MARKEDSFØRINGSTILLADELSESNUMMER
7 tabletter i enkeltdosis blisterpakninger PCTFE / PVC / AL / PAPIR AIC n.036017010 / M
10 tabletter i enkeltdosis blisterpakninger PCTFE / PVC / AL / PAPIR AIC n.036017022 / M
14 tabletter i enkeltdosis blisterpakninger PCTFE / PVC / AL / PAPIR AIC n.036017034 / M
20 tabletter i enkeltdosis blisterpakninger PCTFE / PVC / AL / PAPIR AIC n.036017251 / M
28 tabletter i enkeltdosis blisterpakninger PCTFE / PVC / AL / PAPIR AIC n.036017046 / M
30 tabletter i enkeltdosis blisterpakninger PCTFE / PVC / AL / PAPIR AIC n.036017059 / M
50 tabletter i enkeltdosis blisterpakninger PCTFE / PVC / AL / PAPIR AIC n.036017061 / M
98 tabletter i enkeltdosis blisterpakninger PCTFE / PVC / AL / PAPIR AIC n.036017073 / M
100 tabletter i enkeltdosis blisterpakninger PCTFE / PVC / AL / PAPIR AIC n.036017085 / M
300 tabletter i enkeltdosis blisterpakninger PCTFE / PVC / AL / PAPIR AIC n.036017097 / M
7 tabletter i PCTFE / PVC / AL AIC -blister n.036017109 / M
10 tabletter i PCTFE / PVC / AL AIC -blister n.036017111 / M
14 tabletter i PCTFE / PVC / AL AIC -blister n.036017123 / M
20 tabletter i blisterpakninger PCTFE / PVC / AL AIC n.036017263 / M
28 tabletter i PCTFE / PVC / AL AIC blister n.036017135 / M
30 tabletter i PCTFE / PVC / AL AIC blister n.036017147 / M
50 tabletter i PCTFE / PVC / AL AIC -blister n.036017150 / M
84 tabletter i PCTFE / PVC / AL AIC -blister n.036017236 / M
90 tabletter i PCTFE / PVC / AL AIC -blister n.036017224 / M
98 tabletter i PCTFE / PVC / AL AIC -blister n.036017162 / M
100 tabletter i PCTFE / PVC / AL AIC -blister n.036017174 / M
300 tabletter i PCTFE / PVC / AL AIC blister n.036017186 / M
50 tabletter i enkeltdosisblister PCTFE / PVC / AL AIC n.036017198 / M
100 tabletter i enkeltdosis blisterpakninger PCTFE / PVC / AL AIC n.036017200 / M
300 tabletter i enkeltdosis blisterpakninger PCTFE / PVC / AL AIC n.036017212 / M
100 tabletter i HDPE -flaske AIC n.036017248 / M
09.0 DATO FOR FØRSTE TILLADELSE ELLER FORNYELSE AF TILLADELSEN
Februar 2007
10.0 DATO FOR REVISION AF TEKSTEN
Juni 2011