Almindelighed
Amyloidose er udtrykket, der bruges til at definere en gruppe sygdomme, der er karakteriseret ved akkumulering, ofte i det ekstracellulære område, af et fibrillært proteinmateriale, defineret som amyloid. Uopløselige amyloidfibriller danner særligt stabile aflejringer i talrige organer.

Andre fotos Amyloidosis - Gallery 2
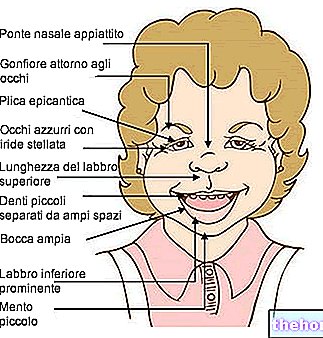
Symptomer og sværhedsgrad af sygdommen afhænger af det organ, der overvejende påvirkes af amyloidakkumulering og typen af amyloidose. De fleste tilfælde er imidlertid systemiske. Med andre ord er fibrillære aflejringer udbredt og kan potentielt forringe funktionen. . Diagnose er defineret ved biopsi, ved at undersøge en lille prøve af væv under et mikroskop. Potentielle etiologiske faktorer varierer alt efter varianten af amyloidose. Tilgængelige behandlinger kan hjælpe med at håndtere symptomer og begrænse amyloidproduktion.
Karakteristika for amyloidaflejringer
Amyloidose stammer fra forstyrrelser i den sekundære struktur af proteiner (med β-foldet arkkonfiguration). Under normale forhold syntetiseres proteiner faktisk i en lineær streng af aminosyrer, som, når de foldes, får en specifik rumlig konformation (proteinfoldning). Takket være sin struktur, derfor med den korrekte proteinfoldning, er proteinet i stand til at udføre de fysiologiske funktioner, som det er ansvarlig for. Amyloidproteinerne stammer fra en forløber, der behandles af cellerne forkert (på grund af "fejlfoldning) "). Proteinerne, der danner fibriller, er diversificerede efter størrelse, aminosyresekvens og nativ struktur, men bliver til uopløselige aggregater, der er ens i struktur og egenskaber. Forstadierne til fibriller repræsenteres af primære molekyler (eksempel: let kæde af immunglobuliner, β2-mikroglobulin, apolipoprotein A1 osv.) eller fra produkter, der afspejler en ændring i aminosyre -ligning. Den afvigende sekundære struktur disponerer for dannelse af fibriller, som kan deponeres lokalt i væv og organer og føre til forringelse af deres normale fysiologiske funktion. Mere end 20 forskellige proteinforstadier er blevet identificeret, der kan antage en amyloidformation, hvilket er hvorfor de findes mange forskellige former for amyloidose.
Baseret på placeringen af amyloidaflejringerne kan sygdommen opdeles i:
- Lokaliseret form: Begrænset til et bestemt organ eller væv (hjerte, nyrer, mave -tarmkanal, nervesystem og dermis) og er normalt mindre alvorlig end systemiske (diffuse) former. For eksempel kan amyloidose kun påvirke huden og forårsage misfarvning og / eller kløe. En bestemt type amyloidprotein er også fundet i hjernen hos patienter med Alzheimers sygdom. Lokaliseret amyloidose er typisk for ældning og påvirkede patienter. Fra type 2 -diabetes. (hvor protein ophobes i bugspytkirtlen).
- Systemisk form: amyloidaflejringer er til stede i forskellige organer og genkender generelt neoplastisk, inflammatorisk, genetisk eller iatrogen oprindelse. Systemisk amyloidose er ofte meget alvorlig: det skader normalt hjerte, nyrer, tarm og nerver, hvilket forårsager progressiv insufficiens af organet.
Klassifikation
Der er mange former for amyloidose, klassificeret efter arten af de proteiner, der udgør de fibrillære aflejringer.
De mest almindelige varianter er:
- Primær amyloidose (også kaldet let kæde amyloidose, AL);
- Sekundær amyloidose (også kaldet erhvervet amyloidose, AA);
- Arvelig amyloidose;
- Aldringsassocieret amyloidose (eller senil systemisk amyloidose).