Aktive ingredienser: Capecitabin
Xeloda 150 mg filmovertrukne tabletter
Xeloda indlægssedler er tilgængelige til pakningsstørrelser:- Xeloda 150 mg filmovertrukne tabletter
- Xeloda 500 mg filmovertrukne tabletter
Hvorfor bruges Xeloda? Hvad er det for?
Xeloda tilhører en gruppe af lægemidler kaldet 'cytostatika', som stopper væksten af kræftceller. Xeloda indeholder 150 mg capecitabin, som i sig selv ikke er en cytostatisk medicin. Kun en gang absorberet af kroppen omdannes det til en aktiv kræftmedicin (i større omfang i tumorvæv end i normale væv).
Xeloda er ordineret af læger til behandling af tyktarm, endetarm, mave eller brystkræft. Xeloda er også ordineret til at forhindre ny tyktarmskræft i at dukke op efter fuldstændig kirurgisk fjernelse af tumoren.
Xeloda kan bruges alene eller i kombination med anden medicin.
Kontraindikationer Når Xeloda ikke bør bruges
Tag ikke Xeloda:
- hvis du er allergisk over for capecitabin eller et af de øvrige indholdsstoffer i dette lægemiddel (angivet i afsnit 6). Du skal fortælle det til din læge, hvis du ved, at du er allergisk eller har en overreaktion over for denne medicin,
- hvis du tidligere har haft en alvorlig reaktion på fluoropyrimidinbehandling (en gruppe kræftlægemidler som f.eks. fluorouracil),
- hvis du er gravid eller ammer,
- hvis du har for lave niveauer af hvide blodlegemer og blodplader i blodet (leukopeni, neutropeni eller trombocytopeni),
- hvis du har alvorlige lever- eller nyreproblemer,
- hvis du har en kendt mangel på enzymet dihydropyrimidin dehydrogenase (DPD) involveret i metabolismen af uracil og thymin eller
- hvis du i øjeblikket er i behandling eller er blevet behandlet inden for de sidste 4 uger med brivudin, sorivudin eller stoffer af lignende klasser som en del af behandlingen for herpes zoster (skoldkopper eller St. Anthony's brand).
Forholdsregler ved brug Hvad du skal vide, før du tager Xeloda
Tal med din læge eller apotek, før du tager Xeloda:
- hvis du har en nyre- eller leversygdom
- hvis du har haft eller har hjerteproblemer (for eksempel uregelmæssig puls eller smerter, der stråler fra brystet til kæben og omvendt forårsaget af fysisk anstrengelse og på grund af problemer med blodgennemstrømningen til hjertet),
- hvis du har hjernesygdom (f.eks. en tumor, der har spredt sig til hjernen) eller nerveskader (neuropati),
- hvis du har ubalancer i calciumniveauer (detekteres ved blodprøver),
- hvis du har diabetes
- hvis du ikke kan holde mad eller vand i din krop på grund af alvorlig kvalme og opkastning,
- hvis du lider af diarré,
- hvis du er eller kan blive dehydreret,
- hvis du har ion -ubalancer i dit blod (elektrolyt -ubalancer, som kan findes i blodprøver),
- hvis du har lidt af øjenproblemer, da du muligvis har brug for yderligere øjenovervågning.
- hvis du har en alvorlig hudreaktion.
Dihydropyrimidine dehydrogenase (DPD) -mangel: DPD -mangel er en sjælden sygdom, der er til stede ved fødslen, og som generelt ikke er forbundet med sundhedsproblemer, medmindre der tages visse lægemidler. Hvis du har en ukendt DPD -mangel og tager Xeloda, kan bivirkningerne anført i afsnit 4 "Mulige bivirkninger" forekomme i alvorlig form. Fortæl det til din læge, hvis nogen af bivirkningerne bekymrer dig, eller hvis du bemærker nogen bivirkninger, der ikke er angivet i denne indlægsseddel (se afsnit 4 "Mulige bivirkninger").
Børn og unge
Xeloda er ikke indiceret til behandling af børn og unge. Giv ikke Xeloda til børn og unge.
Interaktioner Hvilke lægemidler eller fødevarer kan ændre virkningen af Xeloda
Brug af anden medicin sammen med Xeloda
Inden behandlingen påbegyndes, skal du fortælle det til din læge eller apotek, hvis du tager anden medicin eller har brugt det for nylig. Dette er af grundlæggende betydning, da samtidig indtagelse af flere lægemidler kan styrke eller reducere deres virkning. Der bør lægges særlig vægt på i tilfælde af samtidig indtagelse af:
- gigtmedicin (allopurinol),
- medicin, der fortynder blodet (coumarin, warfarin),
- visse antivirale lægemidler (sorivudin og brivudin),
- medicin til behandling af anfald eller rysten (phenytoin),
- interferon alfa,
- strålebehandling og nogle lægemidler, der bruges til behandling af kræft (folinsyre, oxaliplatin, bevacizumab, cisplatin, irinotecan),
- medicin, der bruges til at behandle folsyremangel.
Brug af Xeloda sammen med mad og drikke
Du skal tage Xeloda inden for 30 minutter efter måltidets afslutning.
Advarsler Det er vigtigt at vide, at:
Graviditet og amning
Inden behandlingen påbegyndes, skal du fortælle det til din læge, hvis du er gravid, har mistanke om eller planlægger at blive gravid. Du bør ikke tage Xeloda, hvis du er gravid eller mistænkes for at være gravid. Du må ikke amme, mens du tager Xeloda. Spørg din læge eller apotek til råds, før du tager denne medicin.
Kørsel og brug af maskiner
Xeloda kan få dig til at føle dig svimmel, syg eller træt. Det er derfor muligt, at Xeloda kan påvirke evnen til at føre motorkøretøj eller betjene maskiner.
Xeloda indeholder vandfri lactose
Hvis din læge har fortalt dig, at du ikke tåler visse sukkerarter, skal du kontakte din læge, inden du tager dette lægemiddel.
Dosis, metode og administrationstidspunkt Sådan bruges Xeloda: Dosering
Tag altid dette lægemiddel altid nøjagtigt som din læge eller apotek har fortalt dig. Kontakt din læge eller apotek, hvis du er i tvivl.
Xeloda bør kun ordineres af en læge, der har specialiseret sig i brug af antineoplastiske lægemidler.
Xeloda tabletter skal synkes hele med vand inden for 30 minutter efter måltidets afslutning.
Din læge vil ordinere den dosis og behandlingsregime, der passer til dig. Doseringen af Xeloda er baseret på kropsoverfladearealet. Dette beregnes ud fra højde og vægt. Den sædvanlige dosis for voksne er 1250 mg / m2 kropsoverflade to gange om dagen (morgen og aften). Der foreslås to eksempler: en person, hvis vægt er 64 kg og med en højde på 1,64 m, har en kropsoverflade på 1,7 m2 og skal tage 4 tabletter på 500 mg og 1 tablet på 150 mg to gange dagligt. En person, hvis vægt er 80 kg og højden på 1,80 m, har et kropsoverfladeareal på 2,00 m2 og skal tage 5 tabletter à 500 mg to gange dagligt.
Xeloda tabletter tages normalt i 14 dage efterfulgt af en hviledag på 7 dage (hvor der ikke tages tabletter). Disse 21 dage svarer til en behandlingscyklus.
I kombination med andre lægemidler kan den sædvanlige voksen dosis være mindre end 1250 mg / m2 kropsoverflade, og tabletterne skal muligvis tages i en anden tidsperiode (f.eks. Hver dag, uden hvileperiode).
Din læge vil fortælle dig, hvilken dosis du skal tage, hvornår du skal tage den, og hvor lang tid du skal tage den.
Din læge kan ordinere en kombination af 150 mg og 500 mg tabletter for hver styrke.
- Tag tabletterne morgen og aften som foreskrevet af din læge.
- Tag tabletterne inden for 30 minutter efter et måltid (morgenmad og aftensmad).
- Det er vigtigt at tage al medicin som foreskrevet af din læge.
Overdosering Hvad skal jeg gøre, hvis du har taget for meget Xeloda
Hvis du har taget for mange Xeloda
Hvis du har taget for mange Xeloda, skal du kontakte din læge hurtigst muligt, inden du tager din næste dosis.
Hvis du tager mere Xeloda end du burde, kan du opleve følgende bivirkninger: kvalme eller opkastning, diarré, betændelse eller sårdannelse i tarmen eller munden, smerter eller blødninger fra tarmen eller maven eller knoglemarvsdepression (reduktion af en vis type blodlegemer). Hvis du får nogle af disse symptomer, skal du straks kontakte din læge.
Hvis du har glemt at tage Xeloda:
Tag ikke den glemte dosis, og dobbelt ikke den næste. Fortsæt i stedet med din normale dosis og kontakt din læge.
Hvis du holder op med at tage Xeloda:
Stop med capecitabin -behandling forårsager ikke bivirkninger Standsning af capecitabin, hvis du tager coumarin -antikoagulantia (indeholdende f.eks. Phenprocoumon), kan kræve, at din læge ændrer dosis af antikoagulantia.
Spørg din læge eller apotek, hvis du har yderligere spørgsmål om brugen af dette produkt.
Bivirkninger Hvad er bivirkningerne af Xeloda
Ligesom al anden medicin kan denne medicin forårsage bivirkninger, men ikke alle får bivirkninger.
STOP med at tage Xeloda med det samme, og kontakt din læge, hvis et af følgende symptomer udvikler sig:
- Diarré: hvis du har en stigning på 4 eller flere afføring om dagen i forhold til din normale afføring eller natlig diarré.
- Opkastning: hvis du kaster op mere end én gang i løbet af en 24 -timers periode.
- Kvalme: hvis du mister din appetit, og mængden af mad, der indtages på en dag, er meget mindre end normalt.
- Stomatitis: hvis du har smerter, rødme, hævelse eller sår i munden eller halsen.
- Hånd-fod hudreaktion: hvis du har smerter, hævelse og rødme eller prikken i dine hænder og / eller fødder.
- Feber: hvis du har en kropstemperatur på 38 ° C eller højere.
- Infektion: hvis du har tegn på infektion med bakterier eller vira eller andre organismer.
- Brystsmerter: hvis du oplever smerter lokaliseret til midten af brystet, især hvis de opstår under træning.
- Steven-Johnsons syndrom: hvis du oplever et smertefuldt rødt eller lilla udslæt, der spreder sig og blærer og / eller andre læsioner, der begynder at dukke op i slimhinden (f.eks. Mund og læber), især hvis du tidligere har haft lysfølsomhed, infektioner i luftvejene (f.eks. bronkitis) og / eller feber.
Hvis de fanges tidligt, forbedres disse bivirkninger normalt inden for 2-3 dage efter, at medicinen er stoppet. Hvis symptomerne vedvarer, skal du straks kontakte din læge. Din læge kan råde dig til at genoptage medicinen i en lavere dosis.
Ud over dem, der er anført ovenfor, er andre meget almindelige bivirkninger rapporteret ved brug af Xeloda alene, som kan påvirke mere end 1 ud af 10 personer,:
- mavesmerter
- udslæt, tør eller kløende hud
- træthed
- appetitløshed (anoreksi).
Disse bivirkninger kan blive alvorlige. Kontakt derfor altid din læge med det samme, når du bemærker en bivirkning. Din læge vil fortælle dig at reducere dosis og / eller midlertidigt stoppe behandlingen med Xeloda. Dette vil hjælpe med at reducere sandsynligheden for, at bivirkningen vedvarer eller gøre den til en alvorlig bivirkning.
Andre bivirkninger er:
Almindelige bivirkninger (kan forekomme hos op til 1 ud af 10 personer) omfatter:
- fald i antallet af hvide eller røde blodlegemer i blodet (ses ved test)
- dehydrering, vægttab,
- søvnmangel (søvnløshed), depression,
- hovedpine, søvnighed, svimmelhed, unormal hudfornemmelse (følelsesløshed eller prikken), ændring i smag,
- øjenirritation, øget tåreflåd, røde øjne (konjunktivitis),
- betændelse i venerne (tromboflebitis),
- åndenød, næseblod, hoste, løbende næse,
- forkølelsessår eller andre herpesinfektioner,
- infektioner i lungerne eller luftvejene (f.eks. lungebetændelse eller bronkitis),
- tarmblødning, forstoppelse, smerter i øvre del af maven, fordøjelsesbesvær, overdreven luft, mundtørhed,
- hududslæt, hårtab (alopeci), rødme i huden, tør hud, kløe, misfarvning af huden, hudtab, hudbetændelse, negleændringer,
- smerter i led eller lemmer (ekstremiteter), bryst eller ryg,
- feber, hævelse af lemmerne, utilpashed
- problemer med leverfunktionen (ses ved blodprøver) og forhøjet bilirubin i blodet (udskilles af leveren).
Ikke almindelige bivirkninger (kan forekomme hos færre end 1 ud af 100 personer) omfatter:
- blodinfektion, urinvejsinfektion, hudinfektion, næse- og halsinfektion, svampeinfektioner (herunder i munden), influenza, gastroenteritis, byld,
- bløde hævelser under huden (lipoma),
- fald i blodlegemer inklusive blodplader, udtynding af blodet (ses ved test)
- allergi,
- diabetes, nedsat kalium i blodet, fejlernæring, øgede triglycerider i blodet,
- forvirringstilstand, panikanfald, stemningsdepression, nedsat libido,
- problemer med at tale, hukommelsesbesvær, tab af bevægelseskoordination, balanceforstyrrelser, besvimelse, nerveskader (neuropati) og problemer med sanserne,
- sløret eller dobbeltsyn,
- svimmelhed, ørepine,
- uregelmæssig hjerterytme og hjertebanken (arytmi), brystsmerter og hjerteanfald (hjerteanfald),
- blodpropper i dybe vener, højt eller lavt blodtryk, rødme, kulde i lemmerne (ekstremiteter), lilla pletter på huden,
- blodpropper i lungeårerne (lungeemboli), lungekollaps, blodtab ved hoste, astma, åndenød ved anstrengelse,
- tarmobstruktion, opsamling af væske i maven, betændelse i tynd- eller tyktarmen, mave eller spiserør, smerter i underlivet, ubehag i maven, halsbrand (tilbagesvaling af mad fra maven), blod i afføringen,
- gulsot (gulfarvning af hud og øjne),
- hudsår og blærer, hudreaktioner på sollys, rødme i håndfladerne, hævelse eller smerter i ansigtet,
- fælles hævelse eller stivhed, knoglesmerter, muskelsvaghed eller stivhed,
- væskeopsamling i nyrerne, øget urinfrekvens om natten, inkontinens, blod i urinen, øget kreatinin i blodet (tegn på nedsat nyrefunktion),
- usædvanlig blødning fra skeden,
- hævelse (ødem), kuldegysninger og stivhed.
Nogle af disse bivirkninger er almindelige, når capecitabin bruges sammen med andre lægemidler til behandling af kræft. Andre bivirkninger observeret i denne sammenhæng er:
Almindelige bivirkninger (kan forekomme hos op til 1 ud af 10 personer) omfatter:
- fald i natrium, magnesium og calcium i blodet, stigning i blodsukker,
- nervesmerter,
- ring i ørerne (tinnitus), høretab,
- betændelse i venerne,
- hikke, ændret stemme,
- smerter eller ændret / unormal fornemmelse i munden, smerter i kæben,
- svedtendens, nattesved,
- muskelspasme,
- vandladningsbesvær, blod eller protein i urinen,
- blå mærker eller reaktioner på injektionsstedet (forårsaget af medicin givet ved injektion på samme tid).
Sjældne bivirkninger (kan forekomme hos op til 1 ud af 1.000 mennesker) omfatter:
- indsnævring eller blokering af tårekanalen (tårekanalstenose),
- leversvigt,
- betændelse, der fører til dysfunktion eller blokering af galdesekretion (kolestatisk hepatitis),
- specifikke ændringer i elektrokardiogrammet (QT -forlængelse),
- visse typer arytmier (herunder ventrikelflimren, torsades de pointes og bradykardi)
- øjenbetændelse forårsager smerter og potentielle synsproblemer,
- betændelse i huden, der fører til røde pletter og afskalning på grund af en sygdom i immunsystemet.
Meget sjældne bivirkninger (kan forekomme hos op til 1 ud af 10.000 mennesker) omfatter:
- alvorlige hudreaktioner, såsom udslæt, sårdannelse og blærer, som kan involvere sår i mund, næse, kønsorganer, hænder, fødder og øjne (røde og hævede øjne).
Indberetning af bivirkninger
Tal med din læge, apotek eller sygeplejerske, hvis du får bivirkninger. Dette inkluderer eventuelle bivirkninger, der ikke er anført i denne indlægsseddel. Du kan også rapportere bivirkninger direkte via det nationale rapporteringssystem anført i tillæg V. Bivirkninger kan hjælpe give mere information om sikkerheden ved dette lægemiddel.
Udløb og opbevaring
Opbevares utilgængeligt for børn.
Må ikke opbevares ved temperaturer over 30 ° C.
Brug ikke dette lægemiddel efter den udløbsdato, der står på den ydre karton og etiketten efter "EXP". Udløbsdatoen refererer til den sidste dag i måneden.
Lægemidler bør ikke bortskaffes via spildevand eller husholdningsaffald. Spørg din apotek om, hvordan du skal bortskaffe medicin, du ikke længere bruger. Dette vil hjælpe med at beskytte miljøet.
Sammensætning og farmaceutisk form
Xeloda indeholder
Det aktive stof er capecitabin (150 mg for hver filmovertrukket tablet).
De andre hjælpestoffer er:
- Tabletkerne: vandfri lactose, croscarmellosenatrium, hypromellose, mikrokrystallinsk cellulose, magnesiumstearat.
- Tabletovertræk: hypromellose, titandioxid (E171), gul og rød jernoxid (E172), talkum.
Hvordan Xeloda ser ud og pakningens indhold
Lys fersken, bikonveks, aflang filmovertrukket tablet, præget med "150" på den ene side og "Xeloda" på den anden side.
Pakningen med Xeloda 150 mg filmovertrukket tablet indeholder 60 filmovertrukne tabletter (6 blisterpakninger med 10 tabletter).
Indlægsseddel: AIFA (Italian Medicines Agency). Indhold offentliggjort i januar 2016. De foreliggende oplysninger er muligvis ikke opdaterede.
For at få adgang til den mest opdaterede version er det tilrådeligt at få adgang til webstedet AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttige oplysninger.
01.0 LÆGEMIDLETS NAVN
XELODA 150 mg tabletter belagt med film
02.0 KVALITATIV OG KVANTITATIV SAMMENSÆTNING
Hver filmovertrukket tablet indeholder 150 mg capecitabin.
Hjælpestof (er) med kendt virkning:
hver filmovertrukket tablet indeholder 15,6 mg vandfri lactose.
Den fulde liste over hjælpestoffer findes i afsnit 6.1.
03.0 LÆGEMIDDELFORM
Filmovertrukket tablet.
Xeloda 150 mg filmovertrukne tabletter er lyse fersken, bikonvekse, aflange tabletter præget med "150" på den ene side og "Xeloda" på den anden side.
04.0 KLINISKE OPLYSNINGER
04.1 Terapeutiske indikationer
Xeloda er indiceret til adjuverende behandling hos patienter, der opereres for tyktarmskræft i fase III (Dukes C) (se pkt. 5.1).
Xeloda er indiceret til behandling af metastatisk kolorektal cancer (se pkt.5.1).
Xeloda er indiceret til førstelinjebehandling af fremskreden mavekræft i kombination med et platinbaseret regime (se pkt.5.1).
Xeloda i kombination med docetaxel (se pkt. 5.1) er indiceret til behandling af patienter med lokalt fremskreden eller metastatisk brystkræft efter svigt i cytotoksisk kemoterapi. Tidligere behandling skal have inkluderet en "antracyklin. Desuden er Xeloda indiceret som monoterapi til behandling af patienter med lokalt fremskreden eller metastatisk brystkræft efter svigt i et taxan og et antracyklinholdigt kemoterapiregime, eller for hvem et antracyklin ikke er indiceret." yderligere antracyklinbehandling.
04.2 Dosering og indgivelsesmåde
Xeloda bør kun ordineres af en læge, der har specialiseret sig i brug af antineoplastiske lægemidler.Nær overvågning anbefales for alle patienter under det første behandlingsforløb.
Behandlingen bør afbrydes, hvis der opstår alvorlig toksicitet eller sygdomsprogression. Standard- og reducerede dosisberegninger baseret på kropsoverfladeareal til start Xeloda -doser på 1250 mg / m2 og 1000 mg / m2 er detaljeret i henholdsvis tabel 1 og 2.
Dosering
Anbefalet dosering (se afsnit 5.1):
Monoterapi
Tyktarm, tyktarm og brystkræft
Ved monoterapibehandling er den anbefalede startdosis capecitabin til adjuvant behandling af tyktarm, metastatisk kolorektal eller lokalt fremskreden eller metastatisk brystkræft 1250 mg / m2, administreret to gange dagligt (morgen og aften; samlet dagligt på 2500 mg / m2) til 14 dage, efterfulgt af en 7-dages hviletid. Adjuverende behandling til patienter med stadium III tyktarmskræft anbefales i alt 6 måneder.
Foreningsterapi
Tyktarm, tyktarm og mavekræft
I kombinationsbehandling bør den anbefalede startdosis capecitabin reduceres til 800 - 1000 mg / m2, når det administreres to gange dagligt i 14 dage efterfulgt af en 7 -dages hviletid eller til 625 mg / m2 to gange dagligt. Ved kontinuerlig administration (se pkt. 5.1). I kombination med irinotecan er den anbefalede startdosis 800 mg / m2, når det administreres to gange dagligt i 14 dage, efterfulgt af en 7-dages hvileperiode i kombination med irinotecan 200 mg / m2 på dag 1. Introduktion af bevacizumab i kombinationsregimet har ingen effekt på startdosis af capecitabin.Patienter behandlet med kombinationen capecitabin plus cisplatin, bør præmedicinering for at opretholde tilstrækkelig hydrering og antiemetisk behandling påbegyndes før cisplatinadministration, ifølge produktresuméet af cisplatin. anbefales til patienter behandlet med kombinationen capecitabin plus oxaliplatin i henhold til produktresuméet af oxaliplatin. En 6 måneders adjuverende behandling anbefales til patienter med tyktarmskræft i fase III.
Brystkræft
I kombination med docetaxel er den anbefalede startdosis capecitabin til behandling af metastatisk brystkræft 1250 mg / m2 to gange dagligt i 14 dage efterfulgt af en 7-dages hvileperiode i kombination med docetaxel 75 mg / m2 efter 1 time intravenøst infusion hver 3. uge. Hos patienter, der får kombinationen capecitabin og docetaxel, bør præmedicinering med et oralt kortikosteroid, såsom dexamethason, startes inden administration af docetaxel i henhold til docetaxels resumé af produktkarakteristika.
Beregning af dosis af Xeloda
Tabel 1 Standard- og reducerede dosisberegninger af capecitabin baseret på kropsoverfladeareal, startdosis på 1250 mg / m2
Tabel 2 Standard- og reducerede dosisberegninger af capecitabin baseret på kropsoverfladeareal, startdosis på 1000 mg / m2
Dosisjusteringer under behandlingen:
Generel
Toksicitet forårsaget af capecitabin -administration kan håndteres med symptomatisk behandling og / eller dosisændring (behandlingsafbrydelse eller dosisreduktion). Når dosis er reduceret, bør den ikke øges derefter. I tilfælde af toksiciteter, som efter den behandlende læges mening sandsynligvis ikke bliver alvorlige eller dødelige, såsom alopeci, ændret smag, negleændringer, kan behandlingen fortsættes med den samme dosis uden reduktion eller afbrydelse. Patienter, der tager capecitabin, skal informeres om behovet for øjeblikkeligt at afbryde behandlingen, hvis der opstår moderat eller alvorlig toksicitet. Doser af capecitabin udelukket på grund af toksicitet kan ikke erstattes. Følgende er anbefalede dosisændringer i tilfælde af toksicitet:
Tabel 3 Capecitabin dosisreduktionsplan (3-ugers cyklus eller kontinuerlig behandling)
* Ifølge Common Toxicity Criteria (version 1) fra National Cancer Institute of Canada Clinical Trial Group (NCIC CGT) eller Common Terminology Criteria for Adverse Events (CTCAE) fra Cancer Therapy Evaluation Program, US National Cancer Institute, version 4.0 . For hånd-fod syndrom og hyperbilirubinæmi, se pkt.4.4.
Hæmatologi
Patienter med baseline neutrofiltal
Dosisændringer for toksicitet, når capecitabin bruges som en 3-ugers cyklus i kombination med andre lægemidler
Når capecitabin anvendes i 3-ugers cyklusser i kombination med andre lægemidler, bør dosisændringer for toksicitet udføres i henhold til tabel 3 ovenfor for capecitabin og i henhold til den relevante produktresumé for de andre lægemidler. .
I begyndelsen af behandlingsforløbet, hvis der er angivet udsættelse af behandlingen for enten capecitabin eller det eller de andre lægemidler, bør administrationen af alle lægemidler udskydes, indtil kravene for genoptagelse af administrationen af alle lægemidler er nødvendige.
I løbet af behandlingsforløbet bør behandlingen med capecitabin fortsættes, og dosis af det andet lægemiddel skal justeres i henhold til de relevante forskrivningsoplysninger for de toksiciteter, som den behandlende læge anser for ikke at være relateret til capecitabin.
Hvis det eller de andre lægemidler skal seponeres permanent, kan behandlingen med capecitabin genoptages, når kravene til genindførelse af capecitabin er opfyldt.
Denne tilgang gælder for alle indikationer og alle særlige patientpopulationer.
Dosisændringer for toksicitet, når capecitabin anvendes som kontinuerlig behandling i kombination med andre lægemidler
Dosisændringer for toksicitet, når capecitabin bruges som kontinuerlig behandling i kombination med andre lægemidler, bør udføres i henhold til tabel 3 ovenfor for capecitabin og i overensstemmelse med den relevante produktresumé for de andre lægemidler.
Dosisjusteringer i især patientpopulationer:
Nedsat leverfunktion
Der er utilstrækkelige sikkerheds- og effektdata til at vejlede om dosisjusteringer til patienter med nedsat leverfunktion. Der er ingen data om leversvigt på grund af skrumpelever eller hepatitis.
Nedsat nyrefunktion
Capecitabin er kontraindiceret hos patienter med alvorlig nyreinsufficiens (kreatininclearance mindre end 30 ml / min [Cockcroft og Gault] ved baseline). Forekomsten af grad 3 eller 4 bivirkninger hos patienter med moderat nedsat nyrefunktion (kreatininclearance 30-50 ml / min ved baseline) er højere end i den samlede population. En reduktion på 75% anbefales til en startdosis på 1250 mg / m2 hos patienter med moderat nedsat nyrefunktion ved baseline Ingen dosisreduktion er påkrævet for en startdosis på 1000 mg / m2 hos patienter med moderat nedsat nyrefunktion ved baseline. startdosis hos patienter med let nedsat nyrefunktion (kreatininclearance 51-80 ml / min ved baseline). Hvis patienten udvikler en grad 2, 3 eller 4 bivirkning under behandlingen, skal omhyggelig overvågning og "Umiddelbar seponering af behandlingen, og den næste dosis justeres som angivet i tabel 3 ovenfor. Hvis den beregnede kreatininclearance falder under behandlingen nde under 30 ml / min, bør Xeloda seponeres. Disse anbefalinger om dosisjusteringer ved nedsat nyrefunktion gælder for både monoterapi og kombinationsbrug (se også afsnittet "Ældre" nedenfor).
Ældre borgere
Ingen startdosisjustering er nødvendig ved brug af capecitabin alene.Patienter ≥ 60 år sammenlignet med yngre forsøgspersoner rapporterede imidlertid hyppigere behandlingsrelaterede bivirkninger af grad 3 eller 4.
Da capecitabin blev brugt i kombination med andre midler, oplevede ældre patienter (≥ 65 år) flere bivirkninger af grad 3 og 4, herunder dem, der førte til afbrydelse af behandlingen, end yngre patienter. Tæt overvågning af patienter ≥ 60 år er tilrådeligt.
- I kombination med docetaxel: En øget forekomst af grad 3 eller 4 behandlingsrelaterede bivirkninger og behandlingsrelaterede alvorlige bivirkninger blev observeret hos patienter 60 år og ældre (se pkt.5.1) En initial dosis capecitabin reduceret til 75% (950 mg / m2 to gange dagligt) hos patienter 60 år og ældre Hvis der ikke opstår toksicitet hos patienter ≥ 60 år behandlet med en reduceret startdosis capecitabin i kombination med docetaxel, kan capecitabin -dosis forsigtigt øges til 1250 mg / m2 to gange daglige.
Pædiatrisk population
Der er ingen relevant brug af capecitabin i den pædiatriske population ved indikationer af tyktarm, kolorektal, mave- og brystkræft.
Indgivelsesmåde
Xeloda -tabletter skal synkes med vand inden for 30 minutter efter måltidets afslutning.
04.3 Kontraindikationer
• Tidligere alvorlige eller uventede reaktioner på fluoropyrimidinbehandling.
• Overfølsomhed over for capecitabin eller over for et eller flere af hjælpestofferne anført i pkt. 6.1 eller over for fluorouracil.
• Hos patienter med kendt fuldstændig fravær af dihydropyrimidin dehydrogenase (DPD) aktivitet (se pkt. 4.4).
• Under graviditet og amning.
• Hos patienter med alvorlige former for leukopeni, neutropeni eller trombocytopeni.
• Hos patienter med svært nedsat leverfunktion.
• Hos patienter med svært nedsat nyrefunktion (kreatininclearance mindre end 30 ml / min).
• Under behandling med sorivudin eller dets kemisk relaterede analoger, såsom brivudin (se afsnit 4.5).
• Hvis der er kontraindikationer for nogen af lægemidlerne i kombinationsprogrammet, bør denne medicin ikke bruges.
04.4 Særlige advarsler og passende forholdsregler ved brug
Det dosisbegrænsende toksicitet omfatter diarré, mavesmerter, kvalme, stomatitis og hånd-fod syndrom (hånd-fod hudreaktion, palmar-plantar erythrodysæstesi). De fleste bivirkninger er reversible og kræver ikke permanent seponering af behandlingen, selvom dosisafbrydelse eller reduktion kan være nødvendig.
Diarré. Patienter med alvorlig diarré bør overvåges nøje og i tilfælde af dehydrering gives væske og elektrolytter. Standard antidiarrheal behandlinger (f.eks. Loperamid) kan gives. Grad 2 -diarré i henhold til NCIC's Common Toxicity Criteria betyder en stigning fra 4 til 6 udledninger pr. Dag eller natlig udledning, for grad 3 -diarré en stigning på 7 til 9 udledninger pr. Dag eller inkontinens og malabsorption og for diarré grad 4 og stigning på ≥10 udledninger om dagen eller kraftigt blødende diarré eller behov for parenteral støtte. Om nødvendigt bør en dosisreduktion foretages (se pkt.4.2).
Dehydrering. Dehydrering skal forebygges eller korrigeres, når det sker. Patienter med anoreksi, asteni, kvalme, opkastning eller diarré kan hurtigt blive dehydreret. Dehydrering kan forårsage akut nyresvigt, især hos patienter med allerede nedsat nyrefunktion eller når capecitabin gives i kombination med kendte nefrotoksiske lægemidler. Akut nyresvigt sekundært til dehydrering kan være potentielt dødelig. Hvis der opstår dehydrering af grad 2 (eller højere), skal behandlingen med capecitabin straks stoppes og dehydrering korrigeres. Behandlingen bør ikke genoptages, før patienten er blevet rehydreret, og enhver udløsende årsag skal rettes eller kontrolleres. Dosisændringer bør foretages for den udløsende bivirkning efter behov (se afsnit 4.2).
Hånd-fod syndrom (også kendt som hånd-fod hudreaktion eller palmar-plantar erythrodysæstesi eller kemoterapi-induceret erytem i ekstremiteterne). Grad 1 hånd-fod syndrom er defineret som følelsesløshed, dysestesi / paræstesi, prikken, smertefrit ødem eller erytem i hænder og / eller fødder og / eller ubehag, der ikke hæmmer patientens normale aktiviteter.
Grad 2 hånd-fod syndrom er defineret som smertefuld erytem og ødem i hænder og / eller fødder og / eller ubehag, der påvirker patientens daglige aktiviteter.
Grad 3 hånd-fod syndrom er defineret som våd skalering, sårdannelse, blærer og alvorlige smerter i hænder og / eller fødder og / eller alvorligt ubehag, der gør det umuligt for patienten at arbejde eller udføre daglige aktiviteter. Hvis grad 2 eller 3 hånd -fodssyndrom opstår, tilbagehold administration af capecitabin, indtil symptomintensiteten er løst eller reduceret til grad 1. Efter begyndelsen af grad 3 hånd-fod-syndrom bør efterfølgende doser capecitabin reduceres. Når capecitabin og cisplatin bruges i kombination, anbefales brug af vitamin B6 (pyridoxin) til symptomatisk eller sekundær profylakse behandling af hånd-fod-syndrom ikke, da publicerede tilfælde har vist, at det kan reducere cisplatins effekt. Der er nogle tegn på, at dexpanthenol er effektivt til forebyggelse af hånd-fod-syndrom hos patienter behandlet med Xeloda.
Kardiotoksicitet. Fluoropyrimidinbehandling har været forbundet med kardiotoksicitet, herunder myokardieinfarkt, angina, arytmi, kardiogent shock, pludselig død og elektrokardiografiske ændringer (herunder meget sjældne tilfælde af forlængelse af QT -intervallet). Disse bivirkninger kan forekomme mere almindeligt hos patienter med tidligere koronararterie Hjertearytmi (herunder ventrikelflimren, torsades de pointes og bradykardi), angina pectoris, myokardieinfarkt, hjertesvigt og kardiomyopati er blevet rapporteret hos patienter, der tager capecitabin. betydelig angina pectoris bør udvises særlig forsigtighed (se pkt. 4.8).
Hypo- eller hypercalcæmi. Tilfælde af hypo- eller hypercalcæmi er blevet rapporteret under behandling med capecitabin. Særlig forsigtighed bør udvises hos patienter med en allerede eksisterende hypo- eller hypercalcæmi (se pkt. 4.8).
Sygdomme i central- eller perifert nervesystem. Patienter med central- eller perifert nervesystem, f.eks. Hjernemetastaser eller neuropati, bør betragtes med forsigtighed (se pkt.4.8).
Diabetes mellitus eller elektrolytforstyrrelser. Patienter med diabetes mellitus eller elektrolytforstyrrelser i betragtning af muligheden for forværring under behandling med capecitabin bør overvejes med forsigtighed.
Coumarin-afledte antikoagulantia. I et interaktionsstudie med administration af en enkelt dosis warfarin var der en signifikant stigning i den gennemsnitlige AUC (+ 57%) for S-warfarin. Disse data tyder på en "interaktion, sandsynligvis på grund af" inhibering af cytochrom P450 isoenzym 2C9 med capecitabin. Patienter, der tager coumarin-afledte orale antikoagulantia sammen med capecitabin, bør regelmæssigt overvåges for mulig forekomst af ændringer i koagulationsparametrene (INR eller protrombin tid) og dosis af antikoagulantia bør justeres i overensstemmelse hermed (se pkt.4.5).
Nedsat leverfunktion. Da der ikke foreligger data om sikkerhed og effekt hos patienter med nedsat leverfunktion, bør brugen af capecitabin overvåges nøje hos patienter med let til moderat nedsat leverfunktion, uanset tilstedeværelse eller fravær af levermetastaser. Administration af capecitabin bør afbrydes, hvis behandlingsrelaterede forhøjelser i bilirubin større end 3,0 x ULN eller behandlingsrelaterede forhøjelser i hepatiske aminotransferaser (ALAT, ASAT) større end 2,5 x ULN. monoterapi kan genoptages, når bilirubin falder til ≤3,0 x ULN eller hepatiske aminotransferaser falder til ≤2,5 x ULN.
Nedsat nyrefunktion. Forekomsten af bivirkninger af grad 3 eller 4 hos patienter med moderat nedsat nyrefunktion (kreatininclearance 30-50 ml / min) er højere end i den samlede population (se pkt. 4.2 og 4.3).
Dihydropyrimidine dehydrogenase (DPD) -mangel: Sjælden, uventet og alvorlig toksicitet (f.eks. Stomatitis, diarré, mucositis, neutropeni og neurotoksicitet) forbundet med 5-FU har været relateret til et underskud i DPD-aktivitet.
Patienter med lav eller ingen aktivitet af DPD, et enzym involveret i nedbrydning af fluorouracil, har en øget risiko for alvorlige, livstruende eller dødelige bivirkninger forårsaget af fluorouracil. Selvom DPD -mangel ikke kan identificeres præcist, vides det, at patienter med visse homozygote eller sammensatte heterozygote mutationer af genlokus DPYD, som forårsager fuldstændig eller næsten fuldstændig fravær af DPD-enzymatisk aktivitet (bestemt ved laboratorieanalyse), har størst risiko for livstruende eller dødelig toksicitet og bør ikke behandles med Xeloda (se afsnit 4.3). Ingen dosis viste sig at være sikker for patienter med et totalt fravær af DPD -aktivitet.
Patienter med delvis DPD -mangel (f.eks. Patienter med heterozygote mutationer i DPYD), og for hvilke fordelene ved Xeloda anses for at opveje dets risici (under hensyntagen til hensigtsmæssigheden af et alternativt ikke-fluopyrimidin kemoterapiregime) bør behandles med ekstrem forsigtighed og overvåges ofte med dosisjustering i henhold til toksicitet. Der er utilstrækkelige data til anbefaler en specifik dosis til patienter med delvis DPD -aktivitet målt ved en specifik test.
Livstruende toksiciteter såsom akutte overdosepisoder kan forekomme hos patienter med uidentificeret DPD-mangel, der behandles med capecitabin (se pkt. 4.9). I tilfælde af akut grad 2-4 toksicitet skal behandlingen straks stoppes. Permanent seponering af behandlingen bør overvejes baseret på den kliniske vurdering af begyndelsen, varigheden og sværhedsgraden af de observerede toksiciteter.
Oftalmologiske komplikationer: Patienter bør overvåges nøje for oftalmologiske komplikationer såsom keratitis og hornhindeforstyrrelser, især hvis de tidligere har haft øjensygdomme. Behandling af øjensygdomme bør indledes på en klinisk hensigtsmæssig måde.
Alvorlige hudreaktioner: Xeloda kan forårsage alvorlige hudreaktioner, såsom Stevens-Johnsons syndrom og toksisk epidermal nekrolyse. Hos patienter, der oplever en alvorlig hudreaktion under behandling med Xeloda, skal denne medicin seponeres permanent.
Da dette lægemiddel indeholder vandfri lactose som hjælpestof, bør patienter med sjældne arvelige former for galactoseintolerance, Lapp lactase-enzymmangel og glucose-galactosemalabsorption ikke tage denne medicin.
04.5 Interaktioner med andre lægemidler og andre former for interaktion
Interaktionsundersøgelser er kun blevet udført hos voksne.
Interaktioner med anden medicin:
Substrater af cytokrom P-450 2C9: Ud over warfarin-undersøgelserne er der ikke blevet udført formelle lægemiddel-lægemiddelinteraktionsundersøgelser mellem capecitabin og andre CYP2C9-substrater. Der skal udvises forsigtighed ved administration af capecitabin sammen med 2C9 -substrater (f.eks. Phenytoin). Se også interaktion med andre coumarin-afledte antikoagulantia og pkt.4.4.
Coumarin-afledte antikoagulantiaÆndringer i koagulationsparametre og / eller blødninger er blevet rapporteret hos patienter behandlet samtidigt med capecitabin og coumarin-afledte antikoagulantia, såsom warfarin og phenprocoumon. Disse reaktioner forekom i løbet af et par dage til flere måneder efter initiering af capecitabinbehandling og i nogle tilfælde inden for en måned efter afslutning af capecitabinbehandling. I en klinisk farmakokinetisk interaktionsundersøgelse, efter administration af en enkelt 20 mg dosis warfarin, øgede behandling med capecitabin S-warfarin AUC med 57% med en stigning på 91% i INR. Da metabolismen af R-warfarin ikke blev ændret, tyder disse data på, at capecitabin reducerer isoenzym 2C9, men ikke har nogen effekt på isoenzymer 1A2 og 3A4. Patienter, der tager coumarin-afledte antikoagulantia samtidig med capecitabin, bør monitoreres regelmæssigt for mulig forekomst af ændringer i koagulationsparametre (PT eller INR) og doseringen af antikoagulantia skal justeres i overensstemmelse hermed.
Phenytoin: Stigninger i plasma -phenytoin -koncentrationer er registreret under samtidig brug af capecitabin og phenytoin, hvilket resulterer i symptomer på phenytoinforgiftning i individuelle tilfælde Patienter, der tager phenytoin samtidigt med capecitabin, bør monitoreres regelmæssigt for forekomst af øgede plasmakoncentrationer af phenytoin.
Folinsyre / folsyre: En undersøgelse, der involverede kombinationen af capecitabin og folinsyre, viste, at folinsyre ikke har nogen signifikant effekt på farmacokinetikken af capecitabin og dets metabolitter. Folinsyre har imidlertid virkninger på capecitabins farmakodynamik, hvis toksicitet kan øges med folinsyre: den maksimalt tolererede dosis (MTD) af capecitabin monoterapi ved intermitterende behandlinger er 3000 mg / m2 pr. Dag, hvorimod når capecitabin var forbundet med folinsyre ( 30 mg po to gange dagligt) faldt den maksimalt tolererede dosis til kun 2000 mg / m2 pr. Dag. Stigningen i toksicitet kan være relevant, når man skifter fra 5-FU / LV til et capecitabinbaseret regime.På grund af ligheden mellem folinsyre og folsyre kan den øgede toksicitet også være relevant med tilskud af folsyre ved behandling af folatmangel .
Sorivudin og analoger: Der er rapporteret en klinisk signifikant lægemiddel-lægemiddelinteraktion mellem sorivudin og 5-FU som følge af sorivudin-inhibering af dihydropyrimidin dehydrogenase. Denne interaktion, som fører til øget fluoropyrimidintoksicitet, er potentielt dødelig. Af denne grund bør capecitabin ikke administreres samtidigt med sorivudin eller dets kemisk relaterede analoger, såsom brivudin (se pkt. 4.3). Der bør observeres en hviletid på mindst 4 uger mellem afslutningen af behandlingen med sorivudin eller dets kemisk relaterede analoger, såsom brivudin, og initiering af capecitabinbehandling.
Antacida: Virkningen af en antacida indeholdende aluminiumhydroxid og magnesiumhydroxid på capecitabins farmakokinetik blev undersøgt. Der var en lille stigning i plasmakoncentrationer af capecitabin og en metabolit (5 "-DFCR); der var ingen effekt på de 3 hovedmetabolitter (5 "-DFUR, 5-FU og FBAL).
Allopurinol: Interaktioner mellem 5-FU og allopurinol er blevet observeret med mulig nedsat effekt af 5-FU. Samtidig brug af allopurinol og capecitabin bør undgås.
Interferon alfa: den maksimalt tolererede dosis (MTD) af capecitabin var 2000 mg / m2 pr. dag, når det blev taget i kombination med interferon alfa-2a (3 MIU / m2 pr. dag) sammenlignet med 3000 mg / m2 pr. dag, når capecitabin blev administreret alene.
Strålebehandling: Den maksimalt tolererede dosis (MTD) af capecitabin monoterapi ved hjælp af den intermitterende behandling er 3000 mg / m2 pr. Dag, mens den maksimalt tolererede dosis (MTD) af capecitabin er 2000 mg / m2 pr. Dag, når den kombineres med strålebehandling mod rektal cancer. enten en kontinuerlig dosering eller en daglig dosering fra mandag til fredag i forbindelse med den 6-ugers strålebehandlingscyklus.
Oxaliplatin: Der var ingen klinisk signifikant forskel i eksponering for capecitabin eller dets metabolitter, fri platin eller total platin, når capecitabin blev administreret i kombination med oxaliplatin eller i kombination med oxaliplatin og bevacizumab.
Bevacizumab: Der var ingen klinisk signifikant effekt af bevacizumab på de farmakokinetiske parametre for capecitabin eller dets metabolitter i nærvær af oxaliplatin.
Interaktion med mad
I alle kliniske undersøgelser blev patienterne rådet til at tage capecitabin inden for 30 minutter efter et måltid. Da de nuværende sikkerheds- og effektdata er baseret på administration af lægemidlet sammen med mad, anbefales det, at capecitabin administreres sammen med mad. Administration med mad reducerer absorptionshastigheden af capecitabin (se pkt. 5.2).
04.6 Graviditet og amning
Kvinder i den fertile alder / prævention hos mænd og kvinder
Kvinder i den fertile alder bør rådes til at undgå risiko for graviditet under behandling med capecitabin. Hvis der opstår graviditet under behandling med capecitabin, skal patienten informeres om den potentielle risiko for fosteret. En effektiv præventionsmetode bør anvendes under behandlingen.
Graviditet
Der er ikke udført undersøgelser med capecitabin hos gravide; det kan dog antages, at capecitabin, når det administreres til gravide, kan forårsage skade på fosteret. I reproduktionstoksicitetsundersøgelser hos dyr resulterede administration af capecitabin i embryonal dødelighed og teratogenicitet. Disse resultater er de forventede virkninger af fluoropyrimidinderivater. Capecitabin er kontraindiceret under graviditet.
Fodringstid
Det vides ikke, om capecitabin udskilles i modermælk. Der blev fundet betydelige mængder capecitabin og dets metabolitter i ammende musemælk. Amning bør afbrydes i løbet af capecitabinbehandlingsperioden.
Fertilitet
Der er ingen data om Xeloda og dets indvirkning på fertiliteten. De centrale undersøgelser af Xeloda omfattede kun kvinder i den fertile alder og mænd, hvis de var villige til at bruge passende prævention for at undgå graviditet under hele undersøgelsen og i en rimelig periode derefter.
Effekter på fertiliteten blev observeret i dyreforsøg (se pkt. 5.3).
04.7 Virkninger på evnen til at føre motorkøretøj og betjene maskiner
Capecitabin har en mild eller moderat indflydelse på evnen til at føre motorkøretøj eller betjene maskiner. Capecitabin kan forårsage svimmelhed, træthed og kvalme.
04.8 Bivirkninger
Resumé af sikkerhedsprofilen
Den overordnede sikkerhedsprofil for capecitabin er baseret på data fra mere end 3000 patienter behandlet med capecitabin alene eller med capecitabin i kombination med forskellige kemoterapiregimer ved flere indikationer. Sikkerhedsprofilerne for capecitabin monoterapi i patientpopulationer med metastatisk brystkræft, metastatisk kolorektal cancer og adjuverende tyktarmskræft er ens. Se afsnit 5.1 for detaljer om hovedundersøgelser, herunder undersøgelsesdesign og vigtige effektresultater.
De mest almindeligt rapporterede og / eller klinisk relevante behandlingsrelaterede bivirkninger (ADR'er) var gastrointestinale forstyrrelser (især diarré, kvalme, opkastning, mavesmerter, stomatitis), hånd-fod-syndrom (palmar-plantar erythrodysæstesi), træthed, asteni, anoreksi, kardiotoksicitet, forværring af nyrefunktionen, hvor funktionen tidligere var nedsat og trombose / emboli.
Resumé af bivirkninger i tabelform
De bivirkninger, som efterforskeren anser for muligvis, sandsynligvis eller eksternt relateret til administration af capecitabin, er angivet i tabel 4 for at tage capecitabin alene og i tabel 5 for at tage capecitabin i kombination med forskellige kemoterapiregimer ved flere indikationer. Følgende udtryk bruges til at klassificere bivirkninger efter deres hyppighed: meget almindelig (≥ 1/10), almindelig (≥ 1/100,
Capecitabin monoterapi:
Tabel 4 viser de bivirkninger, der er forbundet med brugen af capecitabin monoterapi baseret på en samlet analyse af sikkerhedsdata fra tre hovedundersøgelser, herunder over 1900 patienter (undersøgelser M66001, SO14695 og SO14796). Bivirkningerne blev inkluderet i den specifikke frekvensgruppe i henhold til den "samlede forekomst, der stammer fra den samlede analyse".
Tabel 4 Resumé af relaterede bivirkninger rapporteret hos patienter behandlet med capecitabin monoterapi.
Capecitabin i kombinationsbehandling:
Tabel 5 viser bivirkninger relateret til brug af capecitabin i kombination med forskellige kemoterapiregimer ved flere indikationer baseret på sikkerhedsdata fra over 3000 patienter. observeret i de afgørende kliniske undersøgelser og kun hvis de er suppleret med dem, der er observeret med capecitabin monoterapi eller hvis de tilhører en højere frekvensgruppe end capecitabin monoterapi (se tabel 4). De usædvanlige bivirkninger, der er rapporteret for capecitabin i kombinationsbehandling, er i overensstemmelse med de bivirkninger, der er rapporteret for capecitabin monoterapi eller monoterapi med kombinationslægemidler (i litteraturen og / eller deres respektive resumé af produktkarakteristika).
Nogle af bivirkningerne er reaktioner, der hyppigt observeres med kombinationslægemidlet (f.eks. Perifer sensorisk neuropati med docetaxel eller oxaliplatin, hypertension med bevacizumab); forværring forårsaget af capecitabinbehandling kan dog ikke udelukkes.
Tabel 5 Oversigt over bivirkninger rapporteret hos patienter behandlet med capecitabin i kombinationsbehandling ud over dem, der blev observeret med capecitabin alene eller observeret i en højere frekvensgruppe end capecitabin alene.
+ For hvert udtryk blev frekvensen beregnet på grundlag af bivirkningerne for alle kvaliteter. For udtryk markeret med et "+" blev frekvensen beregnet på grundlag af grad 3-4 ADR'er. ADR'er blev inkluderet baseret på den højeste forekomst, der er observeret i de kliniske forsøg med kombinationsbehandling.
Beskrivelse af et udvalg af bivirkninger
Hånd-fod syndrom (se pkt.4.4):
I undersøgelser af capecitabin monoterapi (herunder adjuverende terapistudier i tyktarmskræft, behandling af metastatisk kolorektal cancer og behandling af brystkræft), med 1250 mg / m2 capecitabin to gange dagligt i dag 1 til 14 hver tredje uge, hånd-fod-syndrom i enhver grad blev observeret med en frekvens fra 53% til 60%; i capecitabin / docetaxel -armen til behandling af metastatisk brystkræft var frekvensen 63%. I kombinationsbehandling med capecitabin, med capecitabin 1000 mg / m2 to gange dagligt på dag 1 til 14 hver tredje uge, blev enhver grad af hånd-fod-syndrom observeret med en frekvens på 22% og 30%.
Som en del af en metaanalyse af 14 kliniske forsøg med data fra mere end 4.700 patienter behandlet med capecitabin monoterapi eller capecitabin i kombination med forskellige kemoterapiregimer ved flere indikationer (tyktarm, kolorektal, mave- og brystkræft), hånd-fod-syndrom af enhver grad forekom hos 2066 patienter (43%) efter en median på 239 dage (95% CI: 201, 288) fra initiering af capecitabinbehandling. I alle undersøgelser tilsammen var der en "statistisk signifikant sammenhæng mellem følgende kovariater og en øget risiko for at udvikle hånd-fod-syndrom: stigning i startdosis capecitabin (gram), fald i kumulativ dosis capecitabin (0,1 * kg), øget relativ dosisintensitet i de første 6 uger, øget varighed af studiebehandling (uger), stigende alder (trin på 10 år), kvindelig køn og god ECOG-præstationsstatus ved baseline (0 vs ≥1).
Diarré (se pkt.4.4):
Capecitabin kan forårsage diarre, som er observeret hos op til 50% af patienterne.
Resultaterne af en metaanalyse af 14 kliniske undersøgelser med data fra mere end 4.700 patienter behandlet med capecitabin viste, at der i alle undersøgelser tilsammen var en "statistisk signifikant sammenhæng mellem følgende kovariater og en øget risiko for at udvikle diarré: øget startdosis af capecitabin (gram), øget varighed af studiebehandling (uger), stigende alder (trin på 10 år) og kvindeligt køn. Der blev observeret en statistisk signifikant sammenhæng mellem følgende kovariater og en reduktion i risikoen for at udvikle diarré: stigning i den kumulative dosis capecitabin (0,1 * kg) og stigning i relativ dosisintensitet i de første 6 uger.
Kardiotoksicitet (se pkt. 4.4):
Ud over de bivirkninger, der er beskrevet i tabel 4 og 5, baseret på en "samlet analyse af kliniske sikkerhedsdata fra 7 kliniske undersøgelser, herunder 949 patienter (2 fase III og 5 fase II -undersøgelser med metastatisk kolorektal cancer) og i metastatisk brystkræft), Følgende bivirkninger med en forekomst på mindre end 0,1% er blevet observeret i forbindelse med brug af capecitabin alene: kardiomyopati, hjertesvigt, pludselig død og ventrikulære ekstrasystoler.
Encefalopati:
Ud over de bivirkninger, der er beskrevet i tabel 4 og 5, var brugen af capecitabin alene også forbundet med encefalopati med en forekomst på mindre end 0,1% på grundlag af den førnævnte poolede analyse af kliniske sikkerhedsdata fra 7 kliniske undersøgelser.
Særlige populationer
Ældre patienter (se pkt.4.2):
En "analyse af sikkerhedsdata hos patienter ≥ 60 år behandlet med capecitabin monoterapi og en" analyse af patienter behandlet med den terapeutiske kombination af capecitabin og docetaxel viste en øget forekomst af grad 3 og 4 bivirkninger behandlingsrelaterede og behandlingsrelaterede alvorlige bivirkninger sammenlignet med patienter under 60 år. Desuden afbrød patienter ≥60 år, der blev behandlet med capecitabin og docetaxel, behandlingen for tidligt på grund af hyppigere bivirkninger end patienter under 60 år.
Resultaterne af en metaanalyse af 14 kliniske undersøgelser med data fra mere end 4.700 patienter behandlet med capecitabin viste, at der i alle undersøgelser tilsammen var en "statistisk signifikant sammenhæng mellem" fremgang i alder (trin på 10 år) og en øget risiko. at udvikle hånd-fod-syndrom og diarré, og en reduceret risiko for at udvikle neutropeni.
Køn
Resultaterne af en metaanalyse af 14 kliniske forsøg med data fra mere end 4.700 patienter behandlet med capecitabin viste, at der i alle undersøgelser tilsammen var en "statistisk signifikant sammenhæng mellem kvindekøn og en øget risiko for at udvikle syndromet. Hånd-fod og diarré og en reduceret risiko for at udvikle neutropeni.
Patienter med nedsat nyrefunktion (se pkt. 4.2, 4.4 og 5.2):
En analyse af sikkerhedsdata hos patienter behandlet med capecitabin monoterapi (kolorektal cancer) med nedsat nyrefunktion ved baseline viste en øget forekomst af grad 3 og 4 behandlingsrelaterede bivirkninger sammenlignet med patienter med normalt nyre (36% hos patienter uden nedsat nyrefunktion n = 268 vs 41% ved let svækkelse n = 257 og 54% i moderat n = 59) (se afsnit 5.2). En stigning i dosisreduktionshastigheden (44%) blev observeret hos patienter med moderat nedsat nyrefunktion vs 33% og 32% hos patienter med let eller ingen nedsat nyrefunktion og en stigning i for tidlig afbrydelse af behandlingen (21% afbrydelser i løbet af de to første cyklusser) mod 5% og 8% hos patienter med lidt eller ingen nedsat nyrefunktion.
Indberetning af formodede bivirkninger
Rapportering af formodede bivirkninger, der opstår efter godkendelse af lægemidlet, er vigtig, da det muliggør løbende overvågning af lægemidlets fordel / risiko -balance.Professionelle sundhedspersoner anmodes om at rapportere alle formodede bivirkninger via det nationale rapporteringssystem www .agenziafarmaco.gov .it / it / ansvarlig.
04.9 Overdosering
Manifestationer af akut overdosis omfatter kvalme, opkastning, diarré, mucositis, gastrointestinal irritation og blødning samt knoglemarvsdepression. Klinisk behandling af overdosering bør finde sted gennem konventionel terapi og understøttende medicinsk intervention for at korrigere de tilstedeværende kliniske manifestationer og forhindre eventuelle komplikationer deraf.
05.0 FARMAKOLOGISKE EGENSKABER
05.1 Farmakodynamiske egenskaber
Farmakoterapeutisk gruppe: cytostatisk (antimetabolit).
ATC -kode: L01BC06.
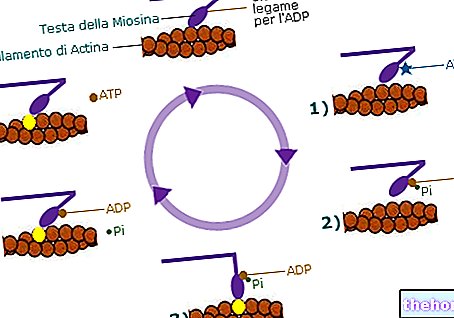
Capecitabin er et ikke-cytotoksisk fluoropyrimidinkarbamat, der fungerer som en oralt administrerbar forløber for den cytotoksiske form 5-fluorouracil (5-FU). Capecitabin aktiveres via flere enzymatiske trin (se afsnit 5.2). Enzymet, der er involveret i den endelige omdannelse til 5-FU, thymidinfosforylase (ThyPase), findes i tumorvæv, men også i normale væv, selvom det generelt er i en lavere koncentration.I humane xenograft-tumormodeller har capecitabin vist sig at have en synergistisk effekt i kombination med docetaxel, som kan være relateret til hyperegulering af thymidinfosforylase af docetaxel.
Metabolismen af 5-FU i den anabolske vej er blevet observeret for at blokere methyleringsreaktionen af deoxyuridylsyre til thymidylsyre og således interferere i syntesen af deoxyribonukleinsyre (DNA). Inkorporering af 5-FU fører også til inhibering af RNA og proteinsyntese. Da DNA og RNA er afgørende for celledeling og vækst, kan 5-FU resultere i thymidinmangel, der forårsager ubalanceret vækst og celledød. Virkningerne af DNA- og RNA-afsavn er særligt markante i celler, der vokser hurtigere og metaboliserer 5-FU hurtigere.
Tyktarm og tyktarmskræft:
Capecitabin monoterapi i adjuverende behandling af tyktarmskræft
Data fra et multicenter, randomiseret, kontrolleret fase III klinisk forsøg med patienter med stadium III (Dukes C) tyktarmskræft understøtter brugen af capecitabin til adjuvant behandling hos patienter med tyktarmskræft (X-ACT Study, M66001) .I denne undersøgelse, 1987 patienter blev randomiseret til behandling med capecitabin (1250 mg / m2 to gange dagligt i 2 uger, efterfulgt af 1 uge fri, som 3-ugers cyklusser i 24 uger) eller 5-FU og leucovorin (Mayo Clinic tidsplan: 20 mg / m2 IV leucovorin efterfulgt af 425 mg / m2 IV 5-FU bolus, på dag 1 til 5, hver 28. dag i 24 uger). Capecitabin svarede mindst til 5-FU / LV IV i sygdomsfri overlevelse i pr. protokolpopulation (HR 0,92; 95% CI: 0,80-1,06). Sygdomsfri overlevelse og samlet overlevelse viste en HR på 0,88 (95% CI: 0,77-1,01; p = 0,068) og 0,86 (95% CI: 0,74-1,01; p = 0,060). Medianopfølgningen på tidspunktet for analysen var 6,9 år.I en tidligere planlagt multivariat Cox-analyse blev capecitabin overlegenhed over 5-FU / LV bolus påvist. Følgende faktorer var foruddefineret i den statistiske analyse for inkludering i modellen: alder, tid fra operation til randomisering, køn, baseline CEA -niveauer, baseline lymfeknuder og land. På tværs af den randomiserede befolkning viste capecitabin sig at være overlegen i forhold til 5-FU / LV både hvad angår sygdomsfri overlevelse (HR: 0,849; 95% CI: 0,739-0,976; p = 0,0212) og med hensyn til samlet overlevelse (HR 0,828; 95% CI: 0,705-0,971; p = 0,0203).
Kombinationsterapi i adjuverende behandling af tyktarmskræft
Data fra et multicenter, randomiseret, kontrolleret, fase III klinisk forsøg med patienter med tyktarmskræft i fase III (Dukes C) understøtter brugen af capecitabin i kombination med oxaliplatin (XELOX) til adjuvant behandling hos patienter med tyktarmskræft (undersøgelse NO16968).I denne undersøgelse blev 944 patienter randomiseret til behandling med capecitabin (1000 mg / m2 to gange dagligt i 2 uger efterfulgt af 1 uges fri som 3-ugers kurser i 24 uger) i kombination med oxaliplatin (130 mg / m2 ved intravenøs infusion i 2 timer på dag 1 hver 3. uge); 942 patienter blev randomiseret til bolus 5-FU og leucovorin. I den primære analyse for DFS i ITT-befolkningen viste det sig, at XELOX var signifikant bedre end 5-FU / LV (HR = 0,80, 95% CI = [0,69; 0,93]; p = 0, 0045). DFS-hastigheden var 71% i XELOX-armen sammenlignet med 67% i 5-FU / LV-armen. Analysen udført for det sekundære endepunkt for RFS understøtter disse resultater med en HR på 0,78 (95% CI = [0,67; 0,92]; p = 0,0024) i XELOX-armen sammenlignet med 5-FU / LV-armen. XELOX viste en tendens til overlegenhed med hensyn til OS med en HR på 0,87 (95% CI = [0,72; 1,05]; p = 0,1486), hvilket oversætter til en 13% reduktion i dødsrisikoen. 5-årigt OS var 78% for XELOX mod 74% for 5-FU / LV. Effektdata er baseret på en median observationstid på 59 måneder for OS og 57 måneder for DFS. Undersøgelsens tilbagetrækningshastighed for bivirkninger var højere i XELOX-armen (21%) end i 5-FU / LV-monoterapi-armen (9%) i ITT-populationen.
Capecitabin monoterapi ved metastatisk kolorektal cancer
Data fra to lignende designede, multicenter, randomiserede, kontrollerede fase III kliniske forsøg (SO14695: SO14796) understøtter brugen af capecitabin til førstelinjebehandling af metastatisk kolorektal cancer. I disse undersøgelser blev 603 patienter randomiseret til behandling med capecitabin (1250 mg / m2 to gange dagligt i 2 uger efterfulgt af en 1-ugers hvile og administreret i 3-ugers cyklusser). 604 patienter blev randomiseret til behandling med 5-FU og leucovorin (regime Mayo: 20 mg / m2 iv leucovorin efterfulgt af 425 mg / m2 intravenøs bolus 5-FU, på dag 1 til 5, hver 28. dag). efterforsker) var: 25,7% (capecitabin) versus 16,7% (Mayo-regime); s. s
Kombinationsterapi i førstelinjebehandling af metastatisk kolorektal cancer
Data fra et multicenter, randomiseret, kontrolleret fase III klinisk forsøg (NO16966) understøtter brugen af capecitabin i kombination med oxaliplatin eller i kombination med oxaliplatin og bevacizumab til førstelinjebehandling af metastatisk kolorektal cancer. Undersøgelsen omfattede to dele: en første to -arm del, hvor 634 patienter blev randomiseret til to forskellige behandlingsregimer, dvs. XELOX eller FOLFOX-4, og en efterfølgende 2x2 faktoriel del, hvor 1401 patienter blev randomiseret til fire forskellige behandlingsregimer. behandling, dvs. XELOX plus placebo, FOLFOX-4 plus placebo, XELOX plus bevacizumab og FOLFOX-4 plus bevacizumab Se tabel 6 for behandlingsregimer.
Tabel 6 Behandlingsregimer i studie NO16966 (mCRC)
I den samlede sammenligning blev non-inferioritet af de XELOX-holdige arme sammenlignet med dem, der indeholdt FOLFOX-4, påvist med hensyn til progressionsfri overlevelse i den berettigede patientpopulation og populationen, der var til hensigt at behandle (se tabel 7). Resultaterne indikerer, at XELOX er ækvivalent med FOLFOX-4 med hensyn til den samlede overlevelse (se tabel 7). Sammenligning af XELOX plus bevacizumab versus FOLFOX-4 plus bevacizumab bestod af en "forud planlagt sonderende analyse. Ved sammenligning af disse behandlingsundergrupper lignede XELOX plus bevacizumab FOLFOX-4 plus bevacizumab med hensyn til progressionsfri overlevelse (fareforhold 1.01; 97,5% CI: 0,84-1,22). Medianopfølgning på tidspunktet for de primære analyser i hensigtsbehandlingspopulationen var 1,5 år; data afledt af udført efter et yderligere års opfølgning er også inkluderet i tabel 7 .. Analysen af PFS under behandlingen bekræftede imidlertid ikke resultaterne af analysen af generel PFS og OS: hazard ratio for XELOX versus FOLFOX -4 var 1,24 med 97,5% CI: 1,07 - 1,44. Selvom følsomhedsanalyser viser, at forskelle i planlægningsplanlægning og tumorvurderingstid påvirker den igangværende PFS -analyse af behandlingen, der blev ikke fundet en endelig forklaring på dette resultat.
Tabel 7 Vigtige effektresultater for non-inferioritetsanalysen af undersøgelse NO16966
* PPE = population af kvalificerede patienter; ** ITT = intention-to-treat population.
I et fase III, randomiseret, kontrolleret studie (CAIRO) blev effekten af at bruge capecitabin i en startdosis på 1000 mg / m2 i 2 uger hver 3. uge undersøgt i kombination med irinotecan til førstelinjebehandling undersøgt. Af patienter med metastatisk kolorektal Kræft. 820 patienter blev randomiseret til at modtage sekventiel (n = 410) eller kombinationsbehandling (n = 410). Sekventiel behandling bestod af en førstelinjebehandling med capecitabin (1250 mg / m2 to gange dagligt i 14 dage), en anden linje med irinotecan (350 mg / m2 på dag 1) og en tredje linje med kombinationen af capecitabin. (1000 mg / m2 to gange dagligt i 14 dage) og oxaliplatin (130 mg / m2 på dag 1). Kombinationsbehandling bestod af førstelinjes capecitabinbehandling (1000 mg / m2 to gange dagligt i 14 dage) kombineret med irinotecan (250 mg / m2 på dag 1 ) (XELIRI) og en anden linje med capecitabin (1000 mg / m2 to gange dagligt i 14 dage) plus oxaliplatin (130 mg / m2 på dag 1). Blev givet med 3 ugers mellemrum. Ved førstelinjebehandling blev den mediane progression -fri overlevelse i hensigtsbehandlingspopulationen var 5,8 måneder (95% CI; 5,1 -6,2 måneder) for capecitabin monoterapi og 7,8 måneder (95% CI: 7,0 -8,3 måneder; p = 0,0002) for XELIRI. dette var forbundet med en øget forekomst af gastrointestinal toksicitet og neutropeni under førstelinjebehandling med XELIRI (henholdsvis 26% og 11% for XELIRI og første-linies capecitabin).
I tre randomiserede undersøgelser af patienter med metastatisk kolorektal cancer blev XELIRI-regimet sammenlignet med 5-FU + irinotecan (FOLFIRI). XELIRI-regimerne omfattede capecitabin 1000 mg / m2 to gange dagligt på dag 1 til 14 i en tre-ugers cyklus kombineret med irinotecan 250 mg / m2 på dag 1. I det større studie (BICC-C) blev patienterne randomiseret til open-label behandling med FOLFIRI (n = 144), bolus 5-FU (mIFL) (n = 145) eller XELIRI (n = 141) og yderligere randomiseret til dobbeltblind celecoxib eller placebo. Median PFS var 7,6 måneder for FOLFIRI, 5,9 måneder for mIFL (p = 0,004 til sammenligning med FOLFIRI) og 5,8 måneder for XELIRI (p = 0,015). Median OS var 23,1 måneder for FOLFIRI, 17,6 måneder for mIFL (p = 0,09) og 18,9 måneder for XELIRI (p = 0,27). Patienter behandlet med XELIRI oplevede overdreven gastronintestinal toksicitet sammenlignet med dem, der blev behandlet med FOLFIRI (48% og 14% diarré for XELIRI og FOLFIRI).
I EORTC-undersøgelsen blev patienterne randomiseret til åben behandling med FOLFIRI (n = 41) eller XELIRI (n = 44) og yderligere randomiseret til dobbeltblind celecoxib eller placebo. Median PFS og total overlevelse (OS) var lavere for XELIRI sammenlignet med FOLFIRI (PFS 5,9 versus 9,6 måneder og OS 14,8 versus 19,9 måneder); derudover er der rapporteret for høje diarrehyppigheder hos patienter, der får XELIRI -behandling (41% XELIRI; 5,1% FOLFIRI).
I undersøgelsen udgivet af Skof et al.blev patienter randomiseret til at modtage enten FOLFIRI eller XELIRI. Den samlede responsrate var 49% i XELIRI -armen og 48% i FOLFIRI -armen (p = 0,76). Ved afslutningen af behandlingen havde 37% af patienterne i XELIRI -armen og 26% af patienterne i FOLFIRI -armen ingen tegn på sygdom (p = 0,56). Toksicitet var ens mellem behandlinger, med undtagelse af neutropeni, som oftest blev rapporteret hos patienter behandlet med FOLFIRI.
Montagnani et al. de brugte resultaterne fra de tre førnævnte undersøgelser til at levere en "global analyse af de randomiserede forsøg, der sammenlignede FOLFIRI- og XELIRI -terapeutiske behandlinger i behandlingen af mCRC." En signifikant reduktion i risikoen for sygdomsprogression var forbundet med FOLFIRI-behandling (HR 0,76; 95% CI: 0,62-0,95; p
Data fra et randomiseret klinisk forsøg (Souglakos et al., 2012) sammenligninger mellem FOLFIRI + bevacizumab og XELIRI + bevacizumab viste ingen signifikante forskelle med hensyn til PFS og OS mellem behandlingerne. Patienter blev randomiseret til behandling med FOLFIRI plus bevacizumab (Arm A, n = 167) eller XELIRI plus bevacizumab (Arm B, n = 166). For arm B brugte XELIRI-regimet capecitabin 1000 mg / m2 to gange dagligt i 14 dage + irinotecan 250 mg / m2 på dag 1. Til behandling med FOLFIRI-Bev og behandling med henholdsvis XELIRI-Bev var den mediane progressionsfri overlevelse ( PFS), samlet overlevelse og responsrate var som følger: 10,0 måneder og 8,9 måneder (p = 0,64); 25,7 måneder og 27,5 måneder (p = 0,55); 45,5% og 39,8% (p = 0,32). Patienter behandlet med XELIRI + bevacizumab rapporterede en signifikant højere forekomst af diarré, febril neutropeni og hånd-fod hudreaktioner sammenlignet med patienter behandlet med FOLFIRI + bevacizumab med signifikant øgede behandlingsforsinkelser, dosisreduktioner og behandlingsafbrydelser.
Data fra et fase II, multicenter, randomiseret, kontrolleret studie (AIO KRK 0604) understøtter brugen af capecitabin i en startdosis på 800 mg / m2 i 2 uger hver 3. uge i kombination med irinotecan og bevacizumab til behandling. patienter med metastatisk kolorektal cancer.
120 patienter blev randomiseret til et modificeret XELIRI-regime med capecitabin 800 mg / m2 to gange dagligt i to uger efterfulgt af 7 dages hvile), irinotecan (200 mg / m2 som en 30 minutters infusion på dag 1 hver 3. uge) og bevacizumab (7,5 mg / kg infunderet i 30 til 90 minutter på dag 1 hver 3. uge); 127 patienter blev randomiseret til behandling med capecitabin (1000 mg / m2 to gange dagligt i to uger efterfulgt af 7 dages hvile), oxaliplatin (130 mg / m2 som en 2-timers infusion på dag 1 hver 3. uge) og bevacizumab (7,5 mg / kg infunderet i 30 til 90 minutter på dag 1 hver 3. uge). Efter en gennemsnitlig opfølgningsvarighed for undersøgelsespopulationen på 26,2 måneder var svarene på behandlingen som følger:
Tabel 8 Effektresultater for AIO KRK -undersøgelsen
Kombinationsterapi i andenlinjebehandling af metastatisk kolorektal cancer
Data fra et fase III, multicenter, randomiseret, kontrolleret klinisk forsøg (NO16967) understøtter brugen af capecitabin i kombination med oxaliplatin til andenlinjebehandling af metastatisk kolorektal cancer. I dette studie 627 patienter med metastatisk kolorektal cancer, som havde modtaget tidligere behandling med irinotecan i kombination med et fluoropyrimidin-baseret regime som førstelinjebehandling blev randomiseret til behandling med XELOX eller FOLFOX-4. For doseringsregime af XELOX og FOLFOX-4 (uden tilføjelse af placebo eller bevacizumab), se tabel 6. XELOX viste sig at være ikke ringere end FOLFOX-4 med hensyn til progressionsfri overlevelse i protokollen og hensigtsbehandlingspopulation (se tabel 9). Resultaterne indikerer, at XELOX er ækvivalent med FOLFOX -4 med hensyn til total overlevelse (se tabel 9). Median opfølgning på tidspunktet for primære analyser i populationen, der var til hensigt at behandle, var på 2,1 år; data fra analyser udført efter yderligere 6 måneders opfølgning er også inkluderet i tabel 9.
Tabel 9 Vigtige effektresultater for non-inferioritetsanalysen af undersøgelse NO16967
* OPP = befolkning pr. Protokol; ** ITT = intention-to-treat-befolkning.
Avanceret mavekræft:
Data fra et multicenter, randomiseret, kontrolleret klinisk fase III-forsøg med patienter med fremskreden mavekræft understøtter brugen af capecitabin ved førstelinjebehandling af fremskreden mavekræft (ML17032). I denne undersøgelse blev 160 patienter randomiseret. Behandling med capecitabin ( 1000 mg / m2 to gange dagligt i 2 uger efterfulgt af 7 dages hvile) og cisplatin (80 mg / m2 som en 2-timers infusion hver 3. uge). I alt 156 patienter blev randomiseret til behandling med 5-FU (800 mg / m2 pr. dag, som en kontinuerlig infusion fra dag 1 til dag 5 hver 3. uge) og cisplatin (80 mg / m2 som en 2-timers infusion på dag 1 hver 3. uge). Capecitabin i kombination med cisplatin har vist non-mindreværd til 5-FU i kombination med cisplatin med hensyn til progressionsfri overlevelse i pr-protokol-analysen (HR 0,81; 95% CI: 0,63-1,04). Median progressionsfri overlevelse var 5,6 måneder (capecitabin + cisplatin) sammenlignet med 5,0 måneder (5-FU + cisplatin). Hazardforholdet for overlevelsesvarighed (samlet overlevelse) svarede til hazard ratio for progressionsfri overlevelse (HR 0,85; 95% CI: 0,64 - 1,13). Median overlevelsesvarighed var 10,5 måneder (capecitabin + cisplatin) sammenlignet med 9,3 måneder (5-FU + cisplatin).
Data fra et fase III, multicenter, randomiseret, klinisk forsøg, der sammenlignede capecitabin med 5-FU og oxaliplatin og cisplatin hos patienter med fremskreden mavekræft, understøtter brugen af capecitabin til førstelinjebehandling af fremskreden mavekræft (REAL-2) I denne undersøgelse blev 1002 patienter randomiseret med et 2x2 faktorielt design til en af følgende 4 arme:
-ECF: epirubicin (50 mg / m2 som bolus på dag 1 hver 3. uge), cisplatin (60 mg / m2 som en 2-timers infusion på dag 1 hver 3. uge) og 5-FU (200 mg / m2 administreret dagligt som en infusion fortsætter via det centrale kateter).
- ECX: epirubicin (50 mg / m2 som bolus på dag 1 hver 3. uge), cisplatin (60 mg / m2 som en 2-timers infusion på dag 1 hver 3. uge) og capecitabin (625 mg / m2 to gange dagligt som behandling sammenhængende).
-EOF: epirubicin (50 mg / m2 som bolus på dag 1 hver 3. uge), oxaliplatin (130 mg / m2 som en 2-timers infusion på dag 1 hver 3. uge) og 5-FU (200 mg / m2 administreret dagligt som en infusion fortsætter via det centrale kateter).
- EOX: epirubicin (50 mg / m2 som bolus på dag 1 hver 3. uge), oxaliplatin (130 mg / m2 som en 2-timers infusion på dag 1 hver 3. uge) og capecitabin (625 mg / m2 to gange dagligt som behandling sammenhængende).
Primære effektanalyser i befolkningen pr. Protokol viste ikke-mindreværd i den samlede overlevelse for capecitabinholdige regimer sammenlignet med 5-FU-baserede regimer (HR 0,86; 95% CI: 0,8-0,0, 99) og for oxaliplatinholdige regimer sammenlignet til cisplatin -baserede regimer (HR 0,92; 95% CI: 0,80 - 1,1). Median samlet overlevelse var 10,9 måneder i capecitabinbaserede regimer og 9,6 måneder hos dem, der indeholdt 5-FU. Median samlet overlevelse var 10,0 måneder i de cisplatin-baserede regimer og 10,4 måneder i de oxaliplatin-baserede regimer.
Capecitabin er også blevet brugt i kombination med oxaliplatin til behandling af fremskreden mavekræft. Undersøgelser med capecitabin monoterapi indikerer, at capecitabin udviser aktivitet ved fremskreden mavekræft.
Avanceret mave-, tyktarms- og tyktarmskræft: metaanalyse
En metaanalyse af seks kliniske undersøgelser (undersøgelser SO14695, SO14796, M66001, NO16966, NO16967, M17032) understøtter brugen af capecitabin som erstatning for 5-FU alene og i kombinationsbehandling af mave-tarmkræft. Den samlede analyse omfatter 3097 patienter behandlet med capecitabinholdige regimer og 3074 patienter behandlet med 5-FU-holdige regimer. Median samlet overlevelse var 703 dage (95% CI: 671; 745) hos patienter behandlet med capecitabinholdige regimer og 683 dage (95% CI: 646; 715) hos patienter behandlet med 5-FU-holdige regimer. Hazardforholdet for total overlevelse var 0,94 (95% CI: 0,89; 1,00, p = 0,0489), hvilket indikerer, at regimer indeholdende capecitabin er ikke ringere end dem, der indeholder 5- FU.
Brystkræft
Kombinationsterapi med capecitabin og docetaxel ved lokalt fremskreden eller metastatisk brystkræft
Data fra et fase III, multicenter, randomiseret, kontrolleret klinisk forsøg understøtter brugen af capecitabin i kombination med docetaxel til behandling af patienter med fremskridt lokalt fremskreden eller metastatisk brystkræft efter svigt i cytotoksisk kemoterapi, der omfattede en "antracyklin. I denne undersøgelse blev 255 patienter randomiseret til behandling med capecitabin (1250 mg / m2 to gange dagligt i 2 uger efterfulgt af en uges hviletid og docetaxel 75 mg / m2 som en 1 times intravenøs infusion hver 3. uge). 256 patienter blev randomiseret til behandling med docetaxel alene (100 mg / m2 som en 1 times intravenøs infusion hver 3. uge). Overlevelse var overlegen i kombinationsarmen capecitabin + docetaxel (p = 0,0126). Median overlevelse var 442 dage (capecitabin + docetaxel) sammenlignet med 352 dage (docetaxel alene). De samlede objektive responsrater i hele den randomiserede population (undersøgelsesvurdering) var: 41,6% (capecitabin + docetaxel) versus 29,7% (docetaxel alene); p = 0,0058. Tid til progression sygdom var overlegen i capecitabin + docetaxel kombinationsarm ( s
Capecitabin monoterapi efter svigt af taxan og en antracyklinholdig kemoterapi, og hvor antracyklinbehandling ikke er indiceret
Data fra to multicenter fase II -studier understøtter brugen af capecitabin monoterapi til behandling af patienter, der skrider frem efter svigt i kemoterapi, der omfattede taxaner og en antracyklin, eller for hvem der ikke er angivet yderligere behandling. Antracykliner. af 236 patienter blev behandlet med capecitabin (1250 mg / m2 to gange dagligt i 2 uger efterfulgt af 1 uges hvileperiode). Samlet objektiv responsrate (undersøgelsesvurdering) var 20 % (første undersøgelse) og 25 % (andet studie) Mediantid til progression var 93 og 98 dage Median overlevelse var 384 og 373 dage.
Alle indikationer:
En metaanalyse af 14 kliniske forsøg med data om mere end 4.700 patienter, der blev behandlet med capecitabin alene eller i kombination med forskellige kemoterapiregimer ved flere indikationer (tyktarm, kolorektal, mave og brystkræft) viste en samlet overlevelse mere langvarig hos capecitabin-behandlede patienter, der udviklet hånd-fod-syndrom end hos patienter, der ikke gjorde: median samlet overlevelse 1100 dage (95% CI: 1007, 1200) vs 691 dage (95% CI: 638; 754) med et hazard ratio på 0,61 (95% CI: 0,56 0,66).
Pædiatrisk population:
Det Europæiske Lægemiddelagentur har frafaldet forpligtelsen til at foretage undersøgelser med Xeloda i alle underklasser af den pædiatriske population i tyktarms- og rektal adenocarcinom, gastrisk adenocarcinom og brystkræft (se afsnit 4.2 for information om "pædiatrisk brug").
05.2 Farmakokinetiske egenskaber
Farmakokinetikken af capecitabin blev evalueret over et dosisinterval på 502-3514 mg / m2 / dag. Parametrene for capecitabin, 5 "-deoxy-5-fluorocytidin (5" -DFCR) og 5 "-deoxy-5-fluorouridin (5" DFUR) målt på dag 1 og 14 var ens. AUC for 5-FU på dag 14 var 30-35% højere. Capecitabin-dosisreduktion reducerer systemisk eksponering for 5-FU på en mere dosisproportionel måde på grund af den ikke-lineære farmakokinetik af den aktive metabolit.
Absorption
Efter oral administration absorberes capecitabin fuldstændigt og hurtigt; efterfølgende omdannes det fuldstændigt til 5 "-DFCR og 5" -DFUR metabolitterne. Administration med mad nedsætter absorptionen af capecitabin, men forårsager kun en mindre effekt på AUC for 5 "-DFUR og AUC for den efterfølgende metabolit 5-FU. I en dosis på 1250 mg / m2 på dag 14 administreret efter måltider, de maksimale plasmakoncentrationer (Cmax i mcg / ml) af capecitabin, 5 "-DFCR, 5" -DFUR, 5 -FU og FBAL var henholdsvis 4,67 - 3,05 - 12,1 - 0,95 og 5,46. Tiden til at nå maksimale plasmakoncentrationer (Tmax i timer) var 1,50 - 2,00 - 2,00 - 2,00 og 3,34. AUC0- ∞ værdierne i mcg • h / ml var 7,75 - 7,24 - 24,6 - 2,03 og 36,3.
Fordeling
Human plasma undersøgelser udført in vitro viste, at capecitabin, 5 "DFCR, 5" -DFUR og 5 -FU er bundet til proteiner, hovedsageligt albumin, i procent på henholdsvis 54%, 10%, 62% og 10%.
Biotransformation
Capecitabin metaboliseres først af hepatisk carboxylesterase til 5 "-DFCR, som efterfølgende omdannes til 5" -DFUR af cytidindeaminase, hovedsageligt lokaliseret i lever- og tumorvæv. Der er derefter en "yderligere katalytisk aktivering af 5" -DFUR af thymidinfosforylase (ThyPase). De enzymer, der er involveret i katalytisk aktivering, er til stede i tumorvæv, men også i raske væv, skønt generelt i lavere mængder. Den sekventielle enzymatiske biotransformation af capecitabin til 5-FU fører til højere koncentrationer i de neoplastiske væv. Ved kolorektal kræft synes 5-FU-generationen stort set at være lokaliseret i tumorstromaceller. Efter oral administration af capecitabin til patienter med tyktarmskræft var forholdet mellem 5-FU koncentration i kolorektal cancer og tilstødende væv 3,2 (fra 0,9 til 8,0). Forholdet mellem 5-FU-koncentration i tumor og plasma var 21,4 (spænder fra 3,9 til 59,9, n = 8), mens forholdet i sundt væv til plasma var 8,9 (med variation fra 3,0 til 25,8, n = 8). Thymidinphosphorylase -aktivitet blev målt og fundet at være 4 gange højere ved primær kolorektal cancer end rapporterede værdier i tilstødende normalt væv Baseret på immunhistokemiske undersøgelser synes thymidinphosphorylase stort set at være lokaliseret i tumorstromalceller.
5-FU kataboliseres efterfølgende af enzymet dihydropyrimidine dehydrogenase (DPD) til dihydro-5-fluorouracil (FUH2), som er meget mindre toksisk. -ureido-propionase omdanner FUPA til a-fluor-b-alanin (FBAL), der elimineres i urinen Aktiviteten af dihydropyrimidin dehydrogenase (DPD) er den kritiske begrænsende faktor. DPD -mangel kan forårsage "øget toksicitet af capecitabin (se afsnit 4.3 og 4.4).
Eliminering
Eliminationshalveringstiden (t½ i timer) for capecitabin, 5 "-DFCR, 5" -DFUR, 5 -FU og FBAL var henholdsvis 0,85 -1,11 -0,66 -0,76 og 3, 23. Capecitabin og dets metabolitter elimineres primært i urinen; 95,5% af den administrerede dosis capecitabin blev genfundet i urinen. Fækal udskillelse er minimal (2,6%). Den største metabolit, der udskilles i urinen, er FBLA, der tegner sig for 57% af den administrerede dosis. Ca. 3% af den administrerede dosis udskilles i urinen som uændret lægemiddel.
Foreningsterapi
Fase I -undersøgelser, der evaluerede effekten af capecitabin på docetaxels eller paclitaxels farmakokinetik og omvendt har vist, at capecitabin ikke har nogen effekt på docetaxels eller paclitaxels farmakokinetik (Cmax og AUC), og at der ikke er nogen effekt af docetaxel eller paclitaxel på farmakokinetikken for 5 "-DFUR.
Farmakokinetik, især patientpopulationer
Der blev udført en populationsfarmakokinetisk analyse efter behandling med capecitabin administreret i en dosis på 1250 mg / m2 to gange dagligt hos 505 patienter med kolorektal cancer. ASAT og ALAT påvirkede ikke statistisk signifikant farmakokinetikken for 5 "-DFUR, 5-FU og FBAL.
Patienter med nedsat leverfunktion på grund af levermetastaser: En farmakokinetisk undersøgelse har vist, at capecitabinens biotilgængelighed og eksponering for 5-FU kan øges hos kræftpatienter med let til moderat nedsat leverfunktion på grund af levermetastaser sammenlignet med patienter uden nedsat leverfunktion. Tilgængelighed af farmakokinetiske data hos patienter med svært nedsat leverfunktion .
Patienter med nedsat nyrefunktionBaseret på resultaterne af en farmakokinetisk undersøgelse foretaget hos kræftpatienter med let til svært nedsat nyrefunktion, er der ingen tegn på, at kreatininclearance påvirker farmakokinetikken af forældremedicin og 5-FU. Kreatininclearance viste sig at påvirke "systemisk eksponering for 5" -DFUR (35%stigning i AUC, når kreatininclearance falder med 50%) og FBAL (114%stigning i AUC, når kreatininclearance falder med 50%). 50%). FBAL er en metabolit uden antiproliferativ aktivitet.
Ældre borgere: Baseret på populationsfarmakokinetiske analyser udført på patienter i forskellige aldre (27 til 86 år), og hvoraf 234 (46%) patienter var 65 år eller ældre, påvirker alderen ikke farmakokinetikken for 5 "-DFUR og 5 -FU . AUC for FBAL steg med alderen (en 20% stigning i alder fører til en 15% stigning i AUC for FBAL). Denne stigning skyldes sandsynligvis en ændring i nyrefunktionen.
Etniske faktorer: Efter oral administration af capecitabin 825 mg / m2 to gange dagligt i 14 dage havde japanske patienter (n = 18) cirka 36% lavere Cmax og 24% lavere AUC for capecitabin sammenlignet med kaukasiske patienter (n = 22). Japanske patienter havde også cirka 25% lavere Cmax og 34% lavere AUC for FBAL end kaukasiske patienter. Den kliniske relevans af disse forskelle er ukendt. Der var ingen signifikante forskelle i eksponering for andre metabolitter (5 "DFCR, 5" DFUR og 5-FU).
05.3 Prækliniske sikkerhedsdata
I toksicitetsundersøgelser ved gentagen dosering gav daglig oral administration af capecitabin til cynomolgusaber og mus gastrointestinale, hæmatopoietiske og lymfatiske toksiske virkninger, der er typiske for fluoropyrimidiner. Disse toksiciteter var reversible. Hudtoksicitet, karakteriseret ved degenerative / regressive ændringer på grund af capecitabin er blevet observeret. Capecitabin viste ingen tegn på lever- og CNS -toksicitet. Kardiovaskulær toksicitet (f.eks. Forlængelse af PR -intervallet og QT -intervallet) er blevet identificeret i cynomolgus -aben efter intravenøs administration (100 mg / kg), men ikke efter gentagen dosering (1379 mg / m2 / dag).) Oralt.
Et toårigt musekræftstudie med mus gav ingen tegn på kræftfremkaldende egenskaber på grund af capecitabin.
I standard fertilitetsundersøgelser udviste hunmus, der tog capecitabin, fertilitetsforstyrrelser; denne effekt var imidlertid reversibel efter en periode med lægemiddelsuspension. Desuden blev atrofiske og degenerative ændringer fundet i reproduktionsorganerne hos hannmus under en 13-ugers undersøgelse; disse virkninger var imidlertid reversible efter en lægemiddelbehandlingsperiode (se afsnit 4.6).
Undersøgelser af embryotoksicitet og teratogenicitet hos mus viste en dosisrelateret stigning i fosterresorption og teratogenicitet. I aben blev aborter og embryonal dødelighed observeret ved høje doser, men der var ingen tegn på teratogenicitet.
Capecitabin var ikke mutagent in vitro for bakterier (Ames -test) eller for pattedyrsceller (kinesisk hamster V79 / HPRT -genmutationstest). Ligesom andre nukleosidanaloger (dvs. 5-FU) var capecitabin imidlertid clastogent i humane lymfocytter (in vitro) og viste en positiv tendens i testen (in vivo) af mikrokerner i musens knoglemarv.
06.0 LÆGEMIDDELOPLYSNINGER
06.1 Hjælpestoffer
Kernen i tabletten:
vandfri lactose,
croscarmellosenatrium,
hypromellose,
mikrokrystallinsk cellulose,
magnesiumstearat.
Tabletbelægning:
hypromellose,
titandioxid (E171),
gul og rød jernoxid (E172),
talkum.
06.2 Uforenelighed
Ikke relevant.
06.3 Gyldighedsperiode
3 år.
06.4 Særlige opbevaringsforhold
Må ikke opbevares over 30 ° C.
06.5 Den umiddelbare emballages art og emballagens indhold
Natur: PVC / PVDC blister.
Indhold: 60 filmovertrukne tabletter (6 blisterpakninger med 10 tabletter).
06.6 Brugsanvisning og håndtering
Ingen særlige instruktioner.
07.0 INDEHAVER AF MARKEDSFØRINGSTILLADELSE
Roche registrering begrænset
6 Falcon Way
Shire Park
Welwyn Garden City
AL7 1TW
Storbritannien
08.0 MARKEDSFØRINGSTILLADELSESNUMMER
EU/1/00/163/001
035219017
09.0 DATO FOR FØRSTE TILLADELSE ELLER FORNYELSE AF TILLADELSEN
Dato for første godkendelse: 2. februar 2001
Dato for sidste fornyelse: 2. februar 2006
10.0 DATO FOR REVISION AF TEKSTEN
September 2015