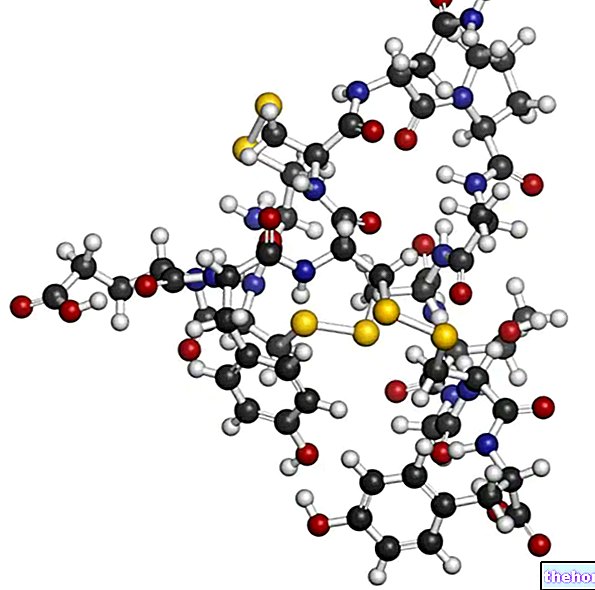
2,3 diphosphoglycerat (2,3 DPG) er en forbindelse afledt af et mellemprodukt af glycolyse; det er særligt koncentreret på erytrocytniveauet, da de røde blodlegemer - uden blødning af mitokondrier - udnytter det anaerobe laktacidmetabolisme (homolaktisk fermentering af glukose) for at opnå energi.

Hæmoglobin er et tetramerisk protein, der består af fire underenheder, to alfa og to beta, der hver består af en proteindel (globin) og en hæm (protetisk gruppe, der binder ilt). 2,3-diphosphoglycerat fæstner sig til Betakæderne og komprimerer dem og reducerer hæmoglobins affinitet for ilt.
Bindingen af 2,3 DPG til hæmoglobinet sker, når det er i deoxygeneret form, mens det opløses i lungen ved hæmoglobins binding til iltet. Faktisk når hæmoglobinet når vævene, β -kæderne er de første til at frigive ilt, og dette tab indebærer en forskydning af monomerer fra midten.Så snart det indre hydrofile hulrum åbner, kommer DPG ind og binder til tetrameren, der danner heteropolære bindinger mellem dets negativt ladede grupper og lysin og histidin rester af kæderne Beta, positivt ladede Den stabiliserede struktur kan også frigive ilt fra de to a -kæder. I lungerne finder den omvendte proces imidlertid sted; ved højt iltryk er α-kæderne de første til at binde det, og DPG'en "klemmes" og udvises fra tetrameren, hvilket muliggør en lettere Oxygen-β-kædebinding.
2,3 bisphosphoglyceratet kan ikke binde sig til føtalt hæmoglobin, da dette molekyle er blottet for de B -kæder, hvormed 2,3 DPG binder sig. Dette forklarer den større affinitet for oxygen af føtalt hæmoglobin end moderhæmoglobin, karakteristik, der gør det muligt for fosterblodet at udtrække ilt fra moderblodet.