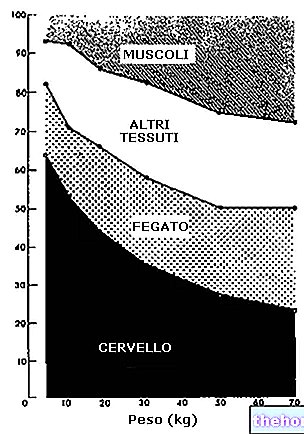
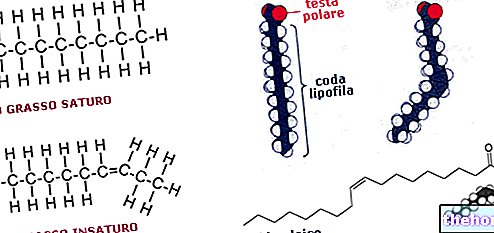
Almindelige aminosyrer og proteinsyntese
De aminosyrer, der oftest forekommer i proteinstrukturer i levende organismer, kaldes almindelige eller proteinogene aminosyrer. Selvom mere end 500 typer aminosyrer er kendt i naturen, er der kun tyve, som vi kalder almindelige. Sammen med dem er der nogle sjældnere, kaldet lejlighedsvise, som generelt stammer fra metabolismen af almindelige efter deres inkorporering i proteinkæden. I kollagen findes for eksempel lysin og prolin, to almindelige aminosyrer, i den hydroxylerede form (hydroxyprolin og hydroxylisin).
De fleste af de andre ikke-almindelige aminosyrer falder hovedsageligt inden for konstitueringen af enzymer og hormoner af proteinkarakter eller rettere peptid (husk at for at blive betragtet som sådan skal et protein bestå af mere end 100 aminosyrer, mens danner henholdsvis et oligo og et polypeptid 2 til 9 og 10 til 100 er tilstrækkeligt).
Blandt de 20 almindelige aminosyrer huskes
Alanin, Arginin, Asparagin, Aspartinsyre, Cystein, Glycin, Glutaminsyre, Glutamin, Histidin, Isoleucin, Leucin, Lysin, Methionin, Fenylalanin, Proline, Serin, Threonin, Tryptophan, Tyrosin, Valin
Eksempler på ikke-almindelige aminosyrer er:
carnitin (involveret i transport af langkædede fedtsyrer inde i mitokondrien, hvor de bruges til at producere energi);
ornithin, citrullin og homocystein (deltage i metabolismen af aminosyrer - urinstofcyklus);
hydroxyprolin og hydroxylisin (de er en del af sammensætningen af kollagen og nogle proteiner);
sarcosin (eller methylglycin).
Nogle aminosyrer kan også have en kommerciel eller farmakologisk betydning.
- Natriumglutamat bruges i fødevareindustrien som en smagsforstærker (se bouillonterning).
- L-dihydroxyphenylalanin (L-DOPA) er et lægemiddel, der bruges til behandling af Parkinsons sygdom.
- 5-hydroxytryptophan (5-HTP) er blevet brugt til behandling af neurologiske symptomer forbundet med phenylketonuri (en arvelig metabolisk sygdom, der forhindrer brug af phenylalanin, en essentiel aminosyre, på grund af særlige enzymatiske underskud; ophobning af phenylalanin i vævene er ansvarlig for alvorlig hud og neurologisk skade).
Planter og bakterier er i stand til at producere bestemte aminosyrer, som findes i peptidantibiotika, såsom nisin og alameticin.
Essentielle aminosyrer
Nogle af de 20 almindelige aminosyrer kaldes essentielle, da de ikke kan syntetiseres af kroppen fra andre forbindelser, men skal tages med mad.
For mennesker er disse phenylalanin, leucin, isoleucin, lysin, methionin, threonin, tryptophan, valin og hos børn histidin og arginin.
Almindelige aminosyrer, kemiske egenskaber

Baseret på R -radikalens kemiske egenskaber (gruppe af atomer, der danner en ikke særlig lang kæde), kan aminosyrer opdeles i forskellige kategorier.
Aminosyrer med apolar R (ikke i stand til at danne hydrogenbindinger):
med alifatisk kæde: alanin, leucin, isoleucin, valin, prolin
med aromatisk kæde: phenylalanin, tryptophan
med en kæde, der indeholder et svovlatom: methionin
Aminosyrer med polar R:
med OH -gruppe: serin, threonin, tyrosin
med SH -gruppe: cystein
med CO-NH2-gruppe: asparagin, glutamin
med H: glycin (den eneste ikke-chirale aminosyre)
Aminosyrer med basisk R:
lysin, arginin, histidin
Aminosyrer med syre R:
glutaminsyre, asparaginsyre

.jpg)