Aktive ingredienser: Oxerutina
VENORUTON 500 mg brusetabletter
VENORUTON 1000 mg brusetabletter
Venoruton indlægssedler er tilgængelige til pakningsstørrelser: - VENORUTON 500 mg brusetabletter, VENORUTON 1000 mg brusetabletter
- VENORUTON 1000 mg granulat til oral opløsning, VENORUTON 500 mg filmovertrukne tabletter, VENORUTON 2% gel
Hvorfor bruges Venoruton? Hvad er det for?
Hvad er det
VENORUTON er en vasoprotektor baseret på oxerutin, et stof hentet fra blomster og blade af Sophora Japonica.
Hvorfor bruges den
VENORUTON er indiceret til behandling af symptomer, der skyldes venøs insufficiens; tilstander af kapillær skrøbelighed.
Kontraindikationer Når Venoruton ikke bør bruges
Overfølsomhed over for oxerutin eller over for et eller flere af hjælpestofferne.
Patienter, der lider af ødem i underekstremiteter på grund af hjerte-, nyre- eller leversygdom, bør ikke tage Venoruton, da virkningen af Venoruton ikke er bevist i disse indikationer.
Venoruton anbefales ikke til børn.
Forholdsregler ved brug Hvad du skal vide, før du tager Venoruton
Venoruton anbefales ikke til børn.
Interaktioner Hvilke lægemidler eller fødevarer kan ændre virkningen af Venoruton
Fortæl det til din læge eller på apoteket, hvis du for nylig har taget anden medicin, også uden recept.
Til dato er der ikke rapporteret om nogen specifik interaktion mellem oxerutin og andre lægemidler. Laboratoriedata om en mulig modulering af leverenzymernes aktivitet med oxerutins komponenter (quercetin og rutin til stede i spor) er uoverensstemmende.
Advarsler Det er vigtigt at vide, at:
Hvad skal man gøre under graviditet og amning
Spørg din læge eller apotek til råds, før du tager medicin. Lægemidlets sikkerhed under graviditet er ikke fastlagt, derfor anbefales det ikke under graviditet. I dyreforsøg blev der fundet spor af oxerutin i modermælk. Det antages, at de små mængder orexutin, der passerer i modermælk, ikke kan betragtes som klinisk relevante for mennesker.
Dyrestudier har ikke vist nogen effekt på fertiliteten efter administration af oxerutin.
Virkninger på evnen til at føre motorkøretøj og betjene maskiner
Venoruton har ingen eller ubetydelig indflydelse på evnen til at føre motorkøretøj og betjene maskiner.
I sjældne tilfælde er træthed og svimmelhed blevet rapporteret hos patienter, der tog produktet. Berørte patienter rådes til ikke at køre bil eller betjene maskiner.
Vigtig information om nogle af ingredienserne
Dette lægemiddel indeholder 10,15 mmol (396 mg) kalium pr. Tablet. Skal tages i betragtning hos mennesker med nedsat nyrefunktion eller som følger en diæt med lavt kaliumindhold.
Dette lægemiddel indeholder 3,56 mmol (82 mg) natrium pr. Tablet. Skal tages i betragtning hos mennesker på en diætfattig diæt
Dosering og anvendelsesmåde Sådan bruges Venoruton: Dosering
Hvor mange
Venoruton 1000 mg brusetabletter: 1 tablet om dagen.
Venoruton 500 mg brusetabletter: 2 tabletter om dagen.
Advarsel: overskrid ikke de angivne doser uden lægehjælp.
Hvornår og hvor længe
Advarsel: brug kun i korte behandlingsperioder. I tilfælde af forværring af symptomer anbefales det at bruge produktet i cyklusser.
Kontakt din læge, hvis lidelsen opstår gentagne gange, eller hvis du bemærker en nylig ændring i dens egenskaber.
Synes godt om
Hver tablet skal forsigtigt opløses i et glas vand og tages før eller under måltiderne.
Overdosering Hvad skal man gøre, hvis man har taget for meget Venoruton
Der er aldrig blevet rapporteret tegn eller symptomer på overdosis Venoruton.
I tilfælde af utilsigtet indtagelse / indtagelse af en overdosis Venoruton, skal du straks underrette din læge eller gå til det nærmeste hospital.
Spørg din læge eller apotek, hvis du har spørgsmål om brugen af Venoruton
Bivirkninger Hvad er bivirkningerne af Venoruton
Som al anden medicin kan VENORUTON forårsage bivirkninger, men ikke alle får bivirkninger.
Venoruton kan i sjældne tilfælde forårsage gastrointestinale bivirkninger eller hudreaktioner såsom gastrointestinal forstyrrelse, flatulens, diarré, mavesmerter, mavebesvær, dyspepsi, udslæt, kløe eller nældefeber. Meget sjælden er forekomst af svimmelhed, hovedpine, hedeture, træthed eller overfølsomhedsreaktioner såsom anafylaktoide reaktioner.
Bivirkninger er anført nedenfor efter klassificering og hyppighed af organsystemer. Frekvenser defineres som: meget almindelig (≥ 1/10), almindelig (≥ 1/100 a
Forstyrrelser i immunsystemet
Meget sjældne Anafylaktoide reaktioner
Meget sjælden Overfølsomhedsreaktioner
Nervesystemet lidelser
Meget sjælden Svimmelhed
Meget sjælden Hovedpine
Vaskulære patologier
Meget sjælden rødme
Gastrointestinale lidelser
Sjældne gastrointestinale lidelser
Sjælden luft i maven
Sjælden diarré
Sjælden Mavesmerter
Sjælden Mavesmerter
Sjælden dyspepsi
Hud og subkutan væv
Sjælden udslæt
Sjælden kløe
Sjælden Urticaria
Generelle lidelser og tilstande på administrationsstedet
Meget sjælden Træthed
Overholdelse af instruktionerne i indlægssedlen reducerer risikoen for bivirkninger.
Indberetning af bivirkninger
Tal med din læge eller apotek, hvis du får bivirkninger, herunder mulige bivirkninger, der ikke er anført i denne indlægsseddel. Du kan også indberette bivirkninger direkte via det nationale rapporteringssystem på "https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse". Ved at rapportere bivirkninger kan du hjælpe med at give flere oplysninger om sikkerheden ved dette lægemiddel.
Udløb og opbevaring
Udløbsdato: se udløbsdatoen, der er trykt på pakken.
Udløbsdatoen refererer til produktet i intakt emballage, korrekt opbevaret. Advarsel: brug ikke medicinen efter den udløbsdato, der står på pakningen.
Opbevares ved en temperatur under 30 ° C.
Hold beholderen tæt lukket for at beskytte mod lys og fugt.
Lægemidler bør ikke bortskaffes via spildevand eller husholdningsaffald. Spørg din apotek om, hvordan du skal bortskaffe medicin, du ikke længere bruger. Dette vil hjælpe med at beskytte miljøet.
OPBEVAR DETTE LÆGEMIDLET UTILGÆNGELIG FOR BØRN.
Det er vigtigt altid at have oplysningerne om medicinen til rådighed, så behold både æsken og indlægssedlen.
Sammensætning
Venoruton 500 mg brusetabletter: En tablet indeholder: aktiv ingrediens oxerutin 500 mg Hjælpestoffer: vandfri citronsyre; kaliumcarbonat; kaliumbicarbonat; natriumbicarbonat; makrogoli; acesulfam kalium; povidon; appelsinsmag (understøttet på maltodextrin), magnesiumstearat.
Venoruton 1000 mg brusetabletter: En tablet indeholder: aktiv ingrediens oxerutin 1000 mg Hjælpestoffer: vandfri citronsyre; kaliumcarbonat; kaliumbicarbonat; natriumbicarbonat; makrogoli; acesulfam kalium; povidon; appelsinsmag (understøttet på maltodextrin), magnesiumstearat.
Sådan ser det ud
VENORUTON kommer i form af 500 mg eller 1000 mg brusetabletter, pakket i et rør med en tørrehætte. Pakken indeholder:
- 20 brusetabletter à 500 mg.
- 30 brusetabletter på 1000 mg (2 rør à 15 tabletter hver).
Indlægsseddel: AIFA (Italian Medicines Agency). Indhold offentliggjort i januar 2016. De foreliggende oplysninger er muligvis ikke opdaterede.
For at få adgang til den mest opdaterede version er det tilrådeligt at få adgang til webstedet AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttige oplysninger.
01.0 LÆGEMIDLETS NAVN
VENORUTON EFFERVESCENTE TABLETTER
02.0 KVALITATIV OG KVANTITATIV SAMMENSÆTNING
Venoruton 500 mg brusetabletter: En tablet indeholder: aktiv ingrediens oxerutin 500 mg. Hjælpestoffer med kendt effekt: kaliumcarbonat, kaliumbicarbonat, natriumbicarbonat, acesulfamkalium.
Venoruton 1000 mg brusetabletter: En tablet indeholder: aktiv ingrediens oxerutin 1000 mg. Hjælpestoffer med kendt effekt: kaliumcarbonat, kaliumbicarbonat, natriumbicarbonat, acesulfamkalium.
Den fulde liste over hjælpestoffer findes i afsnit 6.1
03.0 LÆGEMIDDELFORM
Brusetabletter
04.0 KLINISKE OPLYSNINGER
04.1 Terapeutiske indikationer
VENORUTON er indiceret til behandling af symptomer, der skyldes venøs insufficiens; tilstander af kapillær skrøbelighed.
04.2 Dosering og indgivelsesmåde
Venoruton 1000 mg brusetabletter: 1 tablet om dagen.
Venoruton 500 mg brusetabletter: 2 tabletter om dagen.
Hver tablet skal forsigtigt opløses i et glas vand og tages før eller under måltiderne.
04.3 Kontraindikationer
Overfølsomhed over for det aktive stof eller over for et eller flere af hjælpestofferne anført i pkt.6.1.
04.4 Særlige advarsler og passende forholdsregler ved brug
Vigtig information om nogle af ingredienserne
Dette lægemiddel indeholder 10,15 mmol kalium pr. Tablet. Skal tages i betragtning hos mennesker med nedsat nyrefunktion eller som følger en diæt med lavt kaliumindhold.
Dette lægemiddel indeholder 3,56 mmol natrium pr. Tablet. Skal tages i betragtning hos mennesker på en diætfattig diæt.
04.5 Interaktioner med andre lægemidler og andre former for interaktion
Ingen kendt hidtil.
04.6 Graviditet og amning
Lægemidlets sikkerhed under graviditet er ikke fastlagt, derfor tilrådes det ikke at administrere produktet under graviditet.
Der er ingen begrænsninger for brugen af præparatet under amning.
04.7 Virkninger på evnen til at føre motorkøretøj og betjene maskiner
Ingen effekt.
04.8 Bivirkninger
Selv når behandlingen blev fortsat i flere måneder, blev der aldrig rapporteret om bemærkelsesværdige uønskede virkninger.
04.9 Overdosering
Der er aldrig rapporteret om tilfælde af overdosering.
05.0 FARMAKOLOGISKE EGENSKABER
05.1 Farmakodynamiske egenskaber
Farmakoterapeutisk gruppe: kapillære beskyttende stoffer - bioflavonoider;
ATC -kode C05CA49.
Oxerutin [O- (β-hydroxyethyl) -rutosidea], den aktive ingrediens i Venoruton, tilhører flavonoidfamilien og har på grund af dets molekylære egenskaber en antioxidantvirkning. Det har også vist sig at have tropisme for det venøse endotel.
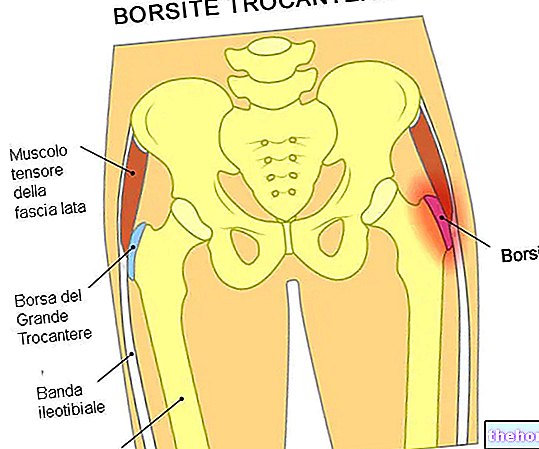
Dens tilstedeværelse på kapillærniveau tillader, især når den i tilstedeværelse af venøs insufficiens den nedsatte hastighed af blodet fremkalder lokal hypoksi, at modvirke og opfange de tilstedeværende frie radikaler. Sidstnævnte vides at være i stand til at forårsage celleskader, udgangspunktet for adhæsion af neutrofile granulocytter til endotelet med udløsning af den inflammatoriske reaktion, hvilket resulterer i stigning i kapillær permeabilitet og dannelse af ødem i underekstremiteterne.
Oxerutins antioxidante virkning på membranen i endotelcellerne og på erytrocytterne i mikrocirkulationen samt den hæmmende virkning på lipoxygenase af neutrofiler er forbundet med faldet i kapillær permeabilitet med reduktion af ødemdannelse med reduceret stimulus til adhæsion. til endotelet for neutrofile granulocytter og blodplader og til restaurering af de reologiske egenskaber ved røde blodlegemer på kapillærniveau.
Disse sidstnævnte fænomener er især korreleret med de påviste forbedringer i situationen med lokal iltning og venøs tone.
De specifikke farmakodynamiske egenskaber af oxerutin kan derfor også overføres til syndromer med patogenese svarende til venøs insufficiens, f.eks. Den for hæmorroide plexus.
05.2 Farmakokinetiske egenskaber
Venoruton brusetabletter er en farmaceutisk form præget af hurtig opløsning og relativ hurtig absorption af den aktive ingrediens. Faktisk har den fordelen ved at tillade opnåelse af et højt farmakoemia på kort tid takket være den hastighed, hvormed det frigiver det aktive princip i biologiske væsker. Absorberet i mave -tarmkanalen udskilles stoffet hovedsageligt via galdevejen.
05.3 Prækliniske sikkerhedsdata
Oxerutins [O- (β-hydroxyethyl) -rutosidea] toksikologi er blevet evalueret i flere dyrearter.
LD50 hos rotter er mellem 24.000 og 27.000 mg / kg, afhængigt af indgivelsesvejen.
I de kroniske toksicitetstest hos rotter, udført med doser på 2.850 mg / kg / dag i 90 dage, blev der ikke fundet toksisk virkning af lægemidlet.
Test af teratogenese, fertilitet og peri-postnatal toksicitet afslørede ingen anomalier hos afkommet.
06.0 LÆGEMIDDELOPLYSNINGER
06.1 Hjælpestoffer
Vandfri citronsyre; kaliumcarbonat; kaliumbicarbonat; natriumbicarbonat; makrogoli; acesulfam kalium; povidon; appelsinsmag (understøttet på maltodextrin), magnesiumstearat.
06.2 Uforenelighed
Ingen.
06.3 Gyldighedsperiode
4 år
06.4 Særlige opbevaringsforhold
Opbevares ved en temperatur under 30 ° C. Hold beholderen tæt lukket for at beskytte mod lys og fugt.
06.5 Den umiddelbare emballages art og emballagens indhold
Polypropylenrør med polyethylenhætte fyldt med silicagel som tørremiddel.
Venoruton 500 mg brusetabletter: 1 rør med 20 tabletter
Venoruton 1000 mg brusetabletter: n. 2 glas à 15 tabletter hver.
06.6 Brugsanvisning og håndtering
Ubrugt medicin og affald fra denne medicin skal bortskaffes i overensstemmelse med lokale regler.
07.0 INDEHAVER AF MARKEDSFØRINGSTILLADELSE
Novartis Consumer Health S.p.A., Origgio (Varese).
08.0 MARKEDSFØRINGSTILLADELSESNUMMER
Venoruton 500 mg brusetabletter, 20 tabletter: A.I.C. n. 017076112
Venoruton 1000 mg brusetabletter, 30 tabletter: A.I.C. n. 017076124
09.0 DATO FOR FØRSTE TILLADELSE ELLER FORNYELSE AF TILLADELSEN
Dato for seneste fornyelse: 1.6.2010
10.0 DATO FOR REVISION AF TEKSTEN
AIFA Bestemmelse af 16. april 2013



















.jpg)






