Aktive ingredienser: Beclometason (vandfrit beclometasondipropionat), Formoterol (Formoterolfumaratdihydrat)
FOSTER 100 mikrogram / 6 mikrogram inhalationspulver
Fosterpakkeindsatser fås til pakningsstørrelser:- FOSTER 100 mikrogram / 6 mikrogram inhalationspulver
- FOSTER 100/6 mikrogram pr. Aktivering, opløsning under tryk til indånding
Hvorfor bruges Foster? Hvad er det for?
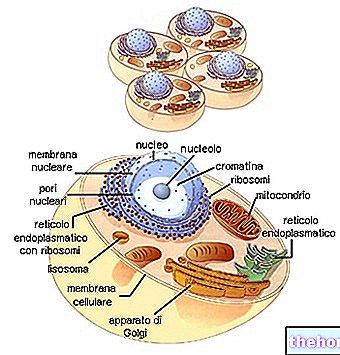
FOSTER er et pulver, der inhaleres gennem munden og frigives direkte i lungerne. Indeholder to aktive ingredienser: vandfrit beclomethason -dipropionat og formoterolfumaratdihydrat.
- Vandfrit beclomethason -dipropionat tilhører en gruppe lægemidler, der almindeligvis kaldes steroider (teknisk kortikosteroider). Steroider er i stand til at behandle og forebygge astmasymptomer, de har en antiinflammatorisk virkning og reducerer derved hævelse og irritation af væggene i de små luftveje i lungerne.
- Formoterolfumaratdihydrat tilhører en gruppe lægemidler kaldet langtidsvirkende bronkodilatatorer, som slapper af luftvejsmusklerne ved at udvide dem, hvilket gør det lettere at trække vejret ind og ud af lungerne.
Tilsammen gør disse to aktive ingredienser lettere vejrtrækning og hjælper også med at forhindre astmasymptomer, såsom hvæsen, hvæsen og hoste.
FOSTER bruges til behandling af astma hos voksne.
Hvis du har fået ordineret FOSTER, er det sandsynligt, at:
- "astma kontrolleres ikke tilstrækkeligt ved hjælp af inhalerede kortikosteroider og korttidsvirkende" efter behov "bronkodilatatorer
eller
- astma reagerer godt på behandling med både kortikosteroider og langtidsvirkende bronkodilatatorer.
Kontraindikationer Når Foster ikke bør bruges
Brug ikke FOSTER
Hvis du er allergisk over for vandfri beclomethason -dipropionat eller formoterolfumaratdihydrat eller et af de øvrige indholdsstoffer i denne medicin (angivet i afsnit 6).
Forholdsregler ved brug Hvad du skal vide, før du tager Foster
Tal med din læge, før du bruger FOSTER, hvis du har en af følgende betingelser:
- hjerteproblemer, som omfatter enhver form for kendt hjertesygdom og / eller hjertefunktion
- hjerterytmeforstyrrelser, såsom øget eller uregelmæssig puls, hurtig puls eller hjertebanken, eller hvis du har fået at vide, at dit hjertemønster er unormalt
- højt blodtryk
- indsnævring af arterierne (også kendt som arteriosklerose), eller hvis du ved, at du har et aneurisme (en unormal udvidelse af blodkarvæggene)
- overaktiv skjoldbruskkirtel
- lavt indhold af kalium i blodet
- eventuelle lever- eller nyreproblemer
- diabetes. Hvis du inhalerer høje doser formoterol, kan dit blodsukkerniveau stige, og derfor kan du blive nødt til at foretage yderligere tests for at overvåge dit blodsukkerniveau, både når du begynder at bruge denne inhalator og periodisk i hele behandlingsvarigheden.
- binyretumor (kaldet feokromocytom)
- hvis du har brug for at blive bedøvet. Afhængigt af typen af anæstesi kan det være nødvendigt at stoppe behandlingen med FOSTER mindst 12 timer før anæstesi
- hvis du tager eller har taget medicin til behandling af tuberkulose (TB), eller hvis du har kendt virusinfektioner eller svampeinfektioner i brystet.
Hvis noget af ovenstående gælder for dig, skal du altid fortælle det til din læge, før du bruger FOSTER.
Hvis du ikke er sikker på, om du kan bruge FOSTER, skal du tale med din læge, astmasygeplejerske eller apotek, inden du bruger inhalatoren.
Interaktioner Hvilke lægemidler eller fødevarer kan ændre Foster -effekten
Inden behandlingen påbegyndes, skal du fortælle det til din læge eller på apoteket, hvis du tager, for nylig har taget eller måske tager andre lægemidler, herunder inhalatorer og receptpligtige lægemidler. Dette er nødvendigt, fordi Fostair kan påvirke den måde, andre lægemidler virker på, og andre lægemidler kan også påvirke, hvordan Fostair virker.
Brug ikke denne medicin sammen med betablokkere. Betablokkere er medicin, der bruges til at behandle forskellige tilstande, herunder hjerteproblemer, forhøjet blodtryk eller glaukom (øget tryk i øjet). Hvis du bruger betablokkere (inklusive øjendråber), kan effekten af formoterol reduceres eller annulleres.
Brug af Fostair sammen med følgende medicin:
- andre lægemidler med aktivitet svarende til formoterol (dvs. beta-adrenerge lægemidler, der normalt bruges til behandling af astma)
- kinidin, disopyramid, procainamid (til behandling af unormale hjerterytmer)
- nogle antihistaminer, for eksempel terfenadin (til behandling af allergiske reaktioner)
- monoaminoxidasehæmmere eller tricykliske antidepressiva, f.eks. phenelzin, isocarboxazid, amitriptylin og imipramin; phenothiaziner (til behandling af depression eller psykiske lidelser)
- L-DOPA (til behandling af Parkinsons sygdom)
- L-thyroxin (til behandling af en underaktiv skjoldbruskkirtel)
- Lægemidler indeholdende oxytocin (som forårsager livmoderkontraktioner)
- Monoaminoxidasehæmmere (MAO -hæmmere) (til behandling af psykiske lidelser), herunder lægemidler med egenskaber, der ligner furazolidon og procarbazin
- digoxin (til behandling af hjertesygdomme)
- Andre lægemidler til behandling af astma (theophyllin, aminophyllin eller steroider)
- diuretika (tabletter til vandladning)
- Nogle bedøvelsesmidler
FOSTER med alkohol
Du bør undgå at indtage alkohol uden først at tale med din læge. Alkohol kan sænke hjertetolerancen over for et af de aktive stoffer i FOSTER, formoterol.
Advarsler Det er vigtigt at vide, at:
Tag ikke denne medicin til behandling af akutte astmasymptomer som hvæsende vejrtrækning, hvæsen og hoste, eller hvis din astma bliver værre eller til behandling af akutte astmaanfald. For at behandle symptomerne skal du bruge din hurtigtvirkende "lindrende" inhalator, som du altid skal have med dig.
Din læge kan beslutte at periodisk måle dit kaliumindhold i blodet, især hvis din astma er alvorlig. Ligesom mange bronkodilatatorer kan FOSTER forårsage et kraftigt fald i serumkaliumniveauer (hypokaliæmi). Dette skyldes, at en reduktion i ilt i blodet i forbindelse med andre behandlinger taget sammen med Fostair kan gøre reduktionen i kaliumindholdet værre.
Hvis du har taget høje doser inhalerede kortikosteroider i lange perioder, har du muligvis brug for flere kortikosteroider i stressede situationer. Stressende situationer kan omfatte at blive indlagt på hospitalet efter en ulykke, have pådraget sig alvorlige kvæstelser eller perioden før en "operation. I sådanne tilfælde vil din læge beslutte, om du vil øge din kortikosteroiddosis eller ej og kan ordinere steroider i tabletter eller steroider til injektion.
Hvis du har brug for at blive indlagt, skal du huske at tage al din medicin og inhalatorer, herunder FOSTER og medicin eller tabletter købt uden recept, i deres originale emballage, hvis det er muligt.
Børn og unge
Denne medicin bør ikke gives til børn og unge under 18 år.
Graviditet og amning
Der er ingen kliniske data om brugen af Fostair under graviditet.
Hvis du er gravid eller ammer, tror at du er gravid eller planlægger at blive gravid, skal du spørge din læge til råds, før du bruger denne medicin. Fostair bør kun bruges under graviditet, hvis din læge råder dig til at gøre det. Din læge vil beslutte, om du skal stoppe med at tage FOSTER under amning, eller om du skal tage FOSTER, men afstå fra at amme. Følg altid lægenes råd omhyggeligt.
Kørsel og brug af maskiner
Det er usandsynligt, at Fostair påvirker evnen til at føre motorkøretøj eller betjene maskiner. Hvis du bemærker bivirkninger som f.eks. Svimmelhed og / eller rysten, kan din evne til at føre motorkøretøj eller betjene maskiner imidlertid blive forringet.
FOSTER indeholder lactose
Laktose -hjælpestoffet indeholder små mængder mælkeproteiner, som kan forårsage reaktioner hos allergiske patienter.
For dem der dyrker sport:
Anvendelsen af lægemidlet uden terapeutisk nødvendighed udgør doping og kan under alle omstændigheder bestemme positive antidopingtest.
Dosis, metode og administrationstidspunkt Sådan bruges Foster: Dosering
Brug altid dette lægemiddel nøjagtigt som din læge eller apotek har fortalt dig. Hvis du er i tvivl, skal du kontakte din læge eller apotek.
FOSTER leverer et ekstra fint pulver, som tillader mere af lægemidlet i dosen at nå til lungerne. Din læge kan derefter ordinere dig en lavere dosis af denne inhalationsmedicin, end du tog sammen med andre inhalatorer.
Din læge vil kontrollere dig regelmæssigt for at sikre, at du tager den korrekte dosis Fostair. Når din astma er godt kontrolleret, kan din læge finde det hensigtsmæssigt gradvist at reducere dosis af Fostair. Under ingen omstændigheder bør du ændre dosis uden først at konsultere din læge.
Hvor meget FOSTER skal bruges:
Voksne og ældre:Den anbefalede dosis af denne medicin er 1 eller 2 inhalationer to gange dagligt.
Den maksimale daglige dosis er 4 inhalationer.
Forøg ikke dosis.
Hvis du mener, at medicinen ikke virker, skal du altid tale med din læge, før du øger dosis.
Husk: Du bør altid have din hurtigtvirkende "rednings" inhalator med dig for at behandle en forværring af symptomer eller et pludseligt astmaanfald.
Sådan bruges FOSTER:
FOSTER er beregnet til indånding. I denne pakke finder du en inhalator, kaldet Nexthaler, indesluttet i en varmeforseglet beskyttelsespose, som indeholder medicinen i form af et pulver. Nexthaler -inhalatoren giver dig mulighed for at inhalere medicinen.
Hvis det er muligt, skal du stå eller sidde oprejst, mens du indånder.
Hvis du har glemt at bruge FOSTER
Tag den glemte dosis, så snart du husker det. Hvis det er næsten tid til din næste dosis, skal du springe den glemte dosis over og tage den næste på det korrekte tidspunkt. Tag ikke en dobbelt dosis.
Hvis du holder op med at tage Fostair:
Selvom du har det bedre, skal du ikke stoppe med at bruge FOSTER eller reducere dosis. Tal med din læge, hvis du har til hensigt at gøre dette. Det er meget vigtigt, at Fostair bruges hver dag som foreskrevet af din læge, selvom du ikke har symptomer.
Hvis din vejrtrækning forbliver uændret:
Hvis dine symptomer ikke forbedres efter indånding af FOSTER, er det muligt, at du bruger enheden forkert. Kontroller derfor instruktionerne for korrekt brug af enheden i slutningen af denne indlægsseddel og / eller kontakt din læge for at forklare, hvordan du bruger den korrekt.
Hvis din astma bliver værre:
Hvis dine symptomer bliver værre eller er svære at kontrollere (f.eks. Hvis du bruger din "lindrende" inhalator oftere), eller hvis din "lindrende" inhalator ikke forbedrer dine symptomer, skal du fortsætte med at bruge FOSTER, men kontakt din læge. så hurtigt som muligt. Din læge kan beslutte at ændre din dosis Fostair eller ordinere en yderligere eller alternativ behandling.
Spørg din læge eller apotek, hvis du har yderligere spørgsmål om brugen af dette lægemiddel.
Overdosering Hvad skal man gøre, hvis man har taget for meget Foster
- Kontakt straks din læge eller nærmeste hospitals akutafdeling for at få råd. Tag medicinen med dig, så sundhedspersonalet kan forstå, hvilken medicin du har taget;
- Bivirkninger kan forekomme. Fortæl det til din læge, hvis du bemærker usædvanlige symptomer, da du muligvis skal undersøge nærmere eller træffe nødvendige behandlingstiltag.
Bivirkninger Hvad er bivirkningerne af Foster
Ligesom al anden medicin kan denne medicin forårsage bivirkninger, men ikke alle får bivirkninger.
Som med andre inhalerede behandlinger er der risiko for forværring af hvæsen, hoste og hvæsen umiddelbart efter brug af FOSTER, og dette kaldes paradoksal bronkospasme. Hvis dette sker, skal du stoppe med at bruge det med det samme. Af FOSTER og bruge din hurtigtvirkende 'lindrende' inhalator hurtigst muligt for at behandle dine symptomer. Du skal straks kontakte din læge.
Fortæl det straks til din læge, hvis du har allergiske reaktioner, herunder hudallergi, kløende hud, udslæt, rød hud, hævelse af hud eller slimhinder, især i øjne, ansigt, læber og hals.
Yderligere mulige bivirkninger af Fostair er anført nedenfor i rækkefølge efter frekvens.
Kontakt straks din læge eller apotek:
- hvis du oplever nogen af de bivirkninger, der er anført nedenfor, og hvis disse virkninger forårsager dig nød eller er svær i intensitet eller vedvarer i flere dage
- hvis han er bekymret af en eller anden grund, eller hvis der er noget, han ikke forstår.
Din læge vil vurdere din grad af astma og starte et andet behandlingsforløb, hvis det er nødvendigt. Du får måske besked på ikke at bruge FOSTER igen.
Almindelig (kan forekomme hos op til 1 ud af 10 personer):
- rysten.
Ikke almindelig (kan forekomme hos op til 1 ud af 100 personer):
- kolde symptomer, ondt i halsen
- svampeinfektioner (i mund og hals). At skylle munden eller gurgle med vand og børste tænder umiddelbart efter indånding kan hjælpe med at forhindre disse bivirkninger.
- forværring af astmasymptomer, vejrtrækningsbesvær
- hæshed
- hoste
- usædvanligt hurtig hjerterytme
- usædvanligt langsom hjerterytme
- undertrykkende smerter i brystet
- hovedpine
- følelse af at være utilpas
- føler sig træt eller nervøs
- ændring i elektrokardiogrammet (EKG)
- lavt niveau af cortisol i urinen eller blodet
- højt kaliumindhold i blodet
- højt blodsukkerniveau
- højt fedtindhold i blodet.
Bivirkninger set med lignende inhalerede lægemidler, der indeholder beclomethason -dipropionat og / eller formoterol, er:
- hjertebanken
- ujævn hjerterytme
- unormal eller ændret smag
- muskelsmerter og muskelkramper
- rastløshed, svimmelhed
- føler angst
- søvnforstyrrelser
- fald i kaliumindholdet i blodet.
Brug af inhalerede kortikosteroider i høje doser og i lange perioder kan forårsage systemiske virkninger, herunder:
- forstyrrelser i binyrernes funktion (binyresuppression)
- udtynding af knoglerne
- væksthæmning hos børn og unge
- øget tryk i øjet (glaukom), grå stær
- hurtig vægtforøgelse, især i ansigt og torso
- forstyrret søvn, depression eller bekymring, uro, nervøsitet, overspænding eller irritabilitet. Disse virkninger er mere tilbøjelige til at forekomme hos børn
- Unormal adfærd.
Tal med din læge eller apotek, hvis du får bivirkninger, herunder mulige bivirkninger, der ikke er anført i denne indlægsseddel.
Udløb og opbevaring
Opbevar denne medicin utilgængeligt for børn.
Brug ikke dette lægemiddel efter den udløbsdato, der står på kartonen, konvolutten og etiketten efter EXP. Udløbsdatoen refererer til den sidste dag i den pågældende måned.
Opbevares i den originale emballage for at beskytte mod fugt. Fjern inhalatoren først fra den første brug.
Inden posen åbnes for første gang: Denne medicin kræver ingen særlige opbevaringstemperaturer.
Efter første åbning af posen: Må ikke opbevares over 25 ° C. Efter første åbning af posen skal medicinen bruges inden for 6 måneder.
Brug etiketten på boksen til at skrive den dato, hvor konvolutten blev åbnet.
Smid ikke medicin via spildevand eller husholdningsaffald. Spørg din apotek om, hvordan du skal smide medicin, du ikke længere bruger. Dette vil hjælpe med at beskytte miljøet.
Andre_information "> Andre oplysninger
Hvad FOSTER indeholder
De aktive ingredienser er: vandfrit beclomethason -dipropionat og formoterolfumaratdihydrat.
Hver dispenseret dispensering indeholder 100 mikrogram vandfrit beclomethason-dipropionat og 6 mikrogram formoterolfumaratdihydrat. Dette svarer til en inhaleret dosis leveret gennem mundstykket på 81,9 mikrogram vandfrit beclomethason -dipropionat og 5 mikrogram formoterolfumaratdihydrat.
Øvrige indholdsstoffer er: lactosemonohydrat (som indeholder små mængder mælkeproteiner) og magnesiumstearat.
Beskrivelse af hvordan FOSTER ser ud og pakningens indhold
Denne medicin kommer som et hvidt eller næsten hvidt inhalationspulver, der er indeholdt i en plastinhalator kaldet Nexthaler.
Hver pakke indeholder en, to eller tre inhalatorer, der hver giver 120 inhalationer.
Hver inhalator er pakket i en varmeforseglet beskyttelsespose (emballage af aluminiumsfolie).
Ikke alle pakningsstørrelser er nødvendigvis markedsført.
Indlægsseddel: AIFA (Italian Medicines Agency). Indhold offentliggjort i januar 2016. De foreliggende oplysninger er muligvis ikke opdaterede.
For at få adgang til den mest opdaterede version er det tilrådeligt at få adgang til webstedet AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttige oplysninger.
01.0 LÆGEMIDLETS NAVN -
FOSTER 100 MCG / 6 MCG PULVER TIL INDÅNDING
02.0 KVALITATIV OG KVANTITATIV SAMMENSÆTNING -
Hver leveret dosis på 10 mg inhalationspulver indeholder:
100 mcg vandfrit beclomethason -dipropionat og 6 mcg formoterolfumaratdihydrat.
Dette svarer til en inhaleret dosis på 81,9 mcg vandfrit beclomethason -dipropionat og 5,0 mcg formoterolfumaratdihydrat.
Hjælpestof (er) med kendt virkning:
Hver indånding indeholder 9,9 mg lactosemonohydrat.
Den fulde liste over hjælpestoffer findes i afsnit 6.1.
03.0 LÆGEMIDDELFORM -
Pulver til indånding.
Multidosis inhalatoren indeholder et hvidt eller næsten hvidt pulver.
04.0 KLINISKE OPLYSNINGER -
04.1 Terapeutiske indikationer -
Astma
FOSTER er indiceret til regelmæssig behandling af astma, når brug af et kombinationsprodukt (inhalerede kortikosteroider og langtidsvirkende beta2-agonister) er passende:
-hos patienter utilstrækkeligt kontrolleret med inhalerede kortikosteroider og inhalerede kortvirkende beta2-agonister brugt "efter behov" eller
-hos patienter, der allerede er tilstrækkeligt kontrolleret med både inhalerede kortikosteroider og langtidsvirkende beta2-agonister.
FOSTER er indiceret til voksne patienter.
Bemærk: Betydelige kliniske data om brug af FOSTER til behandling af akutte astmaanfald er ikke tilgængelige.
KOL
Symptomatisk behandling af patienter med svær KOL (FEV1-historie med gentagne eksacerbationer, med tilstedeværelsen af betydelige symptomer på trods af regelmæssig behandling med langtidsvirkende bronkodilatatorer.
04.2 Dosering og indgivelsesmåde -
FOSTER er beregnet til indånding.
ASTMA
Doseringen af FOSTER er individuelt og skal tilpasses i forhold til sygdommens sværhedsgrad. Dette bør tages i betragtning, ikke kun når behandlingen påbegyndes med kombinationen, men også når dosis ændres. Skulle en patient kræve en kombination af andre doser end dem, der er tilgængelige med den faste kombination, bør de passende doser af beta2-agonister og / eller kortikosteroider ordineres i separate inhalatorer.
Da FOSTER er kendetegnet ved en fordeling af ekstra fine partikler, er en dosisjustering nødvendig, når en patient skifter fra en formulering med en distribution af ikke-ekstrafine partikler til FOSTER inhalationspulver. Når patienter skifter fra tidligere behandlinger, skal det overvejes, at den anbefalede samlede daglige dosis beclomethason-dipropionat til FOSTER-inhalationspulver er lavere end nuværende ikke-ekstrafine partikelprodukter, der indeholder beclomethason-dipropionat, og bør tilpasses den enkelte patients behov. Patienter, der skifter fra FOSTER inhalationsopløsning under tryk til FOSTER inhalationspulver, kræver imidlertid ikke dosisjusteringer.
Anbefalet dosering til voksne fra 18 år:
En eller to indåndinger to gange om dagen.
Den maksimale daglige dosis er 4 inhalationer om dagen.
Anbefalet dosering til børn og unge under 18 år :
FOSTERs sikkerhed og virkning hos børn og unge under 18 år er endnu ikke klarlagt. Der er ingen data tilgængelige for børn op til 11 år. Aktuelt tilgængelige data for unge mellem 12 og 17 år er beskrevet i pkt.4.8 og 5.1, men der kan ikke gives nogen anbefaling om en dosering.
Patienter bør overvåges regelmæssigt af deres læge for at sikre, at doseringen af Fostair forbliver optimal, og at den kun ændres efter råd fra lægen. Dosis bør justeres til den laveste dosis, der er i stand til at opretholde effektiv symptomkontrol. Når symptomkontrollen er opnået med den laveste anbefalede dosis, kan inhaleret kortikosteroid alene prøves som det næste trin.
Patienter bør rådes til at tage Fostair hver dag, også når de er symptomfrie.
KOL
Anbefalet dosering til voksne fra 18 år:
To indåndinger to gange om dagen.
Særlige patientgrupper
Det er ikke nødvendigt at justere doseringen hos ældre patienter.
Der er ingen tilgængelige data om brug af FOSTER til patienter med nedsat lever- eller nyrefunktion (se pkt. 5.2)..
Indgivelsesmåde
Nexthaler er en åndedrætsaktiveret inhalator. Patienter med moderat til svær astma- og KOL -patienter har vist sig at være i stand til at producere tilstrækkeligt inspiratorisk flow til at udløse dosislevering fra Nexthaler (se pkt.5.1). Leveringen af FOSTER med Nexthaler er uafhængig af det inspiratoriske flow i de værdier, som denne patientpopulation kan nå gennem inhalatoren.
Korrekt brug af Nexthaler inhalatoren er afgørende for vellykket behandling. Patienten bør rådes til at læse indlægssedlen omhyggeligt og følge den brugsanvisning, der er beskrevet der.
Når det er muligt, skal patienter stå eller sidde oprejst, når de indånder.
Med Nexthaler stilles dosis kun til rådighed til indånding, når hætten er tændt fuldstændig åben. Åbning af dækslet, indånding og lukning af dækslet i rækkefølge styrer dosistællermekanismen. Patienten skal instrueres i at lukke igen fuldstændig emhætten hver gang. Antallet af doser, der er synlige i indikatorvinduet i den nedre del af inhalatorens ydre krop, falder ikke, når hætten lukkes igen, hvis patienten ikke har inhaleret gennem inhalatoren.
Patienten skal instrueres i kun at åbne inhalatorhætten, når det er nødvendigt. Hvis patienten har åbnet inhalatoren, men ikke har inhaleret, og hætten derefter er lukket, returneres dosen til pulverbeholderen inden i. Inhalatoren; den næste dosis kan sikkert inhaleres.
Optimal lungefordeling kan opnås, hvis patienten inhalerer, mens han inhalerer hurtigt og dybt gennem inhalatoren. Det anbefales at holde vejret i 5-10 sekunder (eller lige så behageligt som det er for patienten) inden udånding.
Patienten bør rådes til at undgå udånding gennem Nexthaler -inhalatoren før eller efter inhalering af dosis, da dette kan forringe inhalatorens funktion.
Efter hver indånding skal patienterne skylle munden eller gurgle med vand eller børste tænder (se pkt. 4.4).
04.3 Kontraindikationer -
Overfølsomhed over for beclomethason -dipropionat, formoterolfumaratdihydrat eller over for et eller flere af hjælpestofferne anført i pkt.6.1.
04.4 Særlige advarsler og passende forholdsregler ved brug -
Det anbefales gradvist at reducere dosis, når behandlingen stoppes; behandlingen bør derfor ikke stoppes pludseligt.
Behandling af astma bør udføres normalt i en gradvis plan, og patientens respons bør overvåges både klinisk og ved respiratoriske funktionstest.
Læge bør udvises forsigtighed, hvis patienten ikke finder behandlingen effektiv. Den øgede anvendelse af akutte bronkodilatatorer indikerer en forværring af den underliggende tilstand og begrunder en revurdering af astmabehandling. Pludselig og gradvis forværring af astmakontrollen er potentielt livstruende, og patienten bør hurtigst muligt vurderes behovet for øget behandling med inhalerede eller orale kortikosteroider, eller start antibiotikabehandling, hvis der er mistanke om infektion.
Patienter bør ikke starte FOSTER under en forværring, eller hvis de har en væsentlig forværring eller akut forværring af astma. Alvorlige astma-relaterede bivirkninger og forværringer kan forekomme under behandling med Fostair. Patienter bør bedes fortsætte behandlingen, men søge lægehjælp, hvis astmasymptomer forbliver ukontrollerede, eller hvis de forværres efter start af FOSTER.
Som med andre inhalationsterapier kan paradoksal bronkospasme forekomme med en øjeblikkelig stigning i hvæsen, hoste og dyspnø efter administration. Dette skal straks behandles ved indånding med en hurtigtvirkende bronkodilatator. Fostair skal straks afbrydes, og patienten evalueres og om nødvendigt udsættes for alternativ behandling.
Fostair bør ikke bruges som indledende astmabehandling.
Patienter bør rådes til altid at have deres kortvirkende bronkodilatator til rådighed til behandling af akutte astmaanfald.
Patienter skal mindes om at tage Fostair dagligt som foreskrevet, selv når det er symptomfrit.
Når astmasymptomer er under kontrol, kan det overvejes at gradvist reducere dosis af Fostair. Det er vigtigt at kontrollere patienter regelmæssigt, hvis behandlingen reduceres. Den laveste effektive dosis Fostair bør anvendes (se pkt.4.2).
Lungebetændelse hos KOL -patienter
En øget forekomst af lungebetændelse, herunder lungebetændelse, der kræver hospitalsindlæggelse, er blevet observeret hos KOL -patienter, der modtager inhalerede kortikosteroider. Der er nogle tegn på en øget risiko for lungebetændelse med stigende steroiddosis, men dette er ikke endeligt påvist ved undersøgelser.Der er ingen afgørende kliniske tegn på forskelle inden for klassen i størrelsen af risikoen for lungebetændelse blandt inhalerede kortikosteroider. Læger skal forblive årvågne for den mulige udvikling af lungebetændelse hos KOL -patienter, da de kliniske manifestationer af denne type infektioner overlapper symptomerne på KOL -eksacerbationer.
Risikofaktorer for lungebetændelse hos KOL -patienter omfatter rygning, ældre alder, lavt kropsmasseindeks (BMI) og alvorlig KOL.
Systemiske virkninger kan forekomme med inhalerede kortikosteroider, især når det ordineres i høje doser i længere perioder. Disse virkninger er mindre tilbøjelige til at forekomme end ved behandling med orale kortikosteroider. Mulige systemiske effekter omfatter: Cushings syndrom, Cushingoid udseende, adrenal undertrykkelse, væksthæmning hos børn og unge, nedsat knoglemineraltæthed, grå stær, glaukom og mere sjældent en række psykologiske eller adfærdsmæssige effekter, herunder psykomotorisk hyperaktivitet, søvnforstyrrelser, angst, depression eller aggression (især hos børn). Derfor er det vigtigt, at dosis af inhaleret kortikosteroid justeres til den laveste dosis, ved hvilken effektiv astmakontrol opretholdes.
Anvendelse af højdosis inhalerede kortikosteroider i lange perioder kan forårsage binyresuppression og akut binyrekrise Børn og unge under 16 år, der inhalerer højere end anbefalede doser beclomethasondipropionat, kan have særlig risiko. Situationer, der potentielt kan udløse akut binyre kriser omfatter traumer, kirurgi, infektion eller enhver anden sag, der involverer en hurtig reduktion af doseringen. Symptomer, der opstår, er typisk vage og kan omfatte anoreksi, mavesmerter, vægttab, træthed, hovedpine, kvalme, opkastning, hypotension, nedsat bevidsthedsniveau, hypoglykæmi og anfald. Behovet for yderligere systemisk kortikosteroiddækning i perioder med stress eller elektiv kirurgi bør overvejes.
Patienter, der er blevet overført fra oral til inhaleret kortikosteroidbehandling, kan fortsat have risiko for at forværre binyrereserven i en betydelig periode. Patienter, der tidligere har haft behov for højdosis akutte kortikosteroider i en nødsituation, eller som har været behandlet i en længere periode med højdosis inhalerede kortikosteroider, kan også være i fare. Muligheden for tilbageværende svækkelse i nødstilfælde eller valgfrie stressproducerende situationer bør altid overvejes, og passende behandling med kortikosteroider bør overvejes.
Fostair bør administreres med forsigtighed til patienter med aktiv eller hvilende lungetuberkulose og virus- og svampeinfektioner i luftvejene.
Fostair bør bruges med forsigtighed (som kan omfatte overvågning) hos patienter med hjertearytmi, især i tilfælde af tredje grad atrioventrikulær blok og takyarytmi, idiopatisk subvalvulær aortastenose, hypertrofisk obstruktiv myokardiopati, hjerteiskæmi, alvorlig hjertesvigt, alvorlig arteriel hypertension og aneurisme .
Der bør også udvises forsigtighed ved behandling af patienter med kendt eller mistanke om forlængelse af QTc-intervallet, uanset om det er medfødt eller lægemiddelinduceret (QTc> 0,44 sekunder). Formoterol selv kan forårsage forlængelse af QTc-intervallet.
Forsigtighed er også påkrævet, når Fostair anvendes af patienter med thyrotoksikose, diabetes mellitus, feokromocytom og ubehandlet hypokaliæmi.
Terapi med β2-agonistiske lægemidler kan resultere i potentielt alvorlig hypokaliæmi. Særlig forsigtighed bør udvises hos patienter med alvorlig astma, da denne effekt kan forstærkes af hypoxi. Hypokaliæmi kan også forstærkes ved samtidig behandling med andre lægemidler, der kan fremkalde hypokaliæmi, såsom xanthinderivater, steroider og diuretika (se pkt. 4.5). Forsigtighed anbefales også ved "ustabil astma, når visse" rednings "bronchodilatorer kan anvendes. Det anbefales, at serumkaliumniveauer overvåges i disse tilfælde.
Indånding af formoterol kan forårsage en stigning i blodglukoseniveauerne. Derfor bør blodglukose monitoreres konstant hos diabetespatienter.
Hvis anæstesi med halogenerede bedøvelsesmidler skal udføres, skal det sikres, at FOSTER ikke administreres i mindst 12 timer før anæstesistart, da der er risiko for hjertearytmi.
Patienter bør rådes til at skylle munden eller gurgle med vand eller børste tænder efter indånding af den foreskrevne dosis for at minimere risikoen for orofaryngeale svampeinfektioner og dysfoni.
Laktose indeholder små mængder mælkeproteiner, som kan forårsage allergiske reaktioner.
04.5 Interaktioner med andre lægemidler og andre former for interaktion -
Farmakokinetiske interaktioner
Beclomethason dipropionat metaboliseres meget hurtigt af esteraseenzymer uden involvering af cytochrom P450 -systemet.
Farmakodynamiske interaktioner
Anvendelse af betablokkere (inklusive øjendråber) bør undgås hos patienter med astma.Hvis betablokkere gives af overbevisende årsager, reduceres eller annulleres effekten af formoterol.
Brug af andre beta-adrenerge lægemidler kan resultere i potentielt additive virkninger, derfor er forsigtighed påkrævet ved ordination af theophyllin eller andre beta-adrenerge lægemidler samtidig med formoterol.
Samtidig behandling med kinidin, disopyramid, procainamid, phenothiaziner, nogle antihistaminer (f.eks. Terfenadin), monoaminoxidasehæmmere og tricykliske antidepressiva kan forårsage forlængelse af QTc -intervallet og øge risikoen for ventrikulære arytmier.
Desuden kan L-dopa, L-thyroxin, oxytocin og alkohol ændre hjertets tolerance over for beta-2-sympatomimetika.
Samtidig behandling med monoaminoxidasehæmmere, herunder midler med lignende egenskaber som furazolidon og procarbazin, kan udfælde hypertensive reaktioner.
Der er en høj risiko for arytmier hos patienter, der gennemgår samtidig halogeneret kulbrintebedøvelse.
Samtidig behandling med xanthinderivater, steroider eller diuretika kan forstærke en mulig hypokaliæmi-effekt af beta2-agonister (se pkt. 4.4). Hos patienter behandlet med digitalisglycosider kan hypokaliæmi øge dispositionen for arytmier.
04.6 Graviditet og amning -
Fertilitet
Der foreligger ingen menneskelige data. I undersøgelser udført på rotter var tilstedeværelsen af højdosis beclomethason-dipropionat i kombinationsbehandling forbundet med nedsat kvindelig fertilitet og embryotoksicitet (se pkt. 5.3).
Graviditet
Der er ingen relevante kliniske data om anvendelse af FOSTER til gravide Dyrestudier med kombinationen af beclometason -dipropionat og formoterol har vist tegn på reproduktion og fostertoksicitet efter høj systemisk eksponering (se pkt. 5.3) Høje doser kortikosteroider administreret til gravide dyr vides at forårsage abnormiteter i fosterudvikling, herunder ganespalte og intrauterin væksthæmning.På grund af den tokolytiske virkning af beta2-sympatomimetiske midler skal der udvises særlig forsigtighed under arbejdet. Anvendelse af formoterol anbefales ikke under graviditet, og især sent i graviditeten eller under fødslen, medmindre der ikke findes noget andet (og sikrere) alternativ. Fostair bør kun bruges under graviditet, hvis de forventede fordele opvejer de potentielle risici.
Fodringstid
Der er ingen relevante kliniske data om brug af FOSTER under amning hos mennesker.
Selvom der ikke er data fra dyreforsøg, er det rimeligt at antage, at beclomethason -dipropionat udskilles i modermælk, ligesom andre kortikosteroider..
Selvom det ikke vides, om formoterol passerer i modermælk, er det blevet påvist i animalsk mælk.
Administration af Fostair til kvinder under amning bør overvejes, hvis de forventede fordele opvejer de potentielle risici.Der skal træffes en beslutning om, hvorvidt man skal afbryde amningen eller afbryde / afholde sig fra FOSTER-behandlingen under hensyntagen til fordelene ved amning for barnet og fordelen ved terapi for kvinden.
04.7 Virkninger på evnen til at føre motorkøretøj og betjene maskiner -
Fostair har ingen eller ubetydelig indflydelse på evnen til at føre motorkøretøj og betjene maskiner.
04.8 Bivirkninger -
Den mest almindelige bivirkning var tremor. I et 12-ugers klinisk studie med FOSTER blev tremor kun observeret ved den højere dosis (2 inhalationer to gange dagligt) og forekom hyppigere ved behandlingsstart og med mild intensitet. Ingen patient måtte afbryde undersøgelsen på grund af tremor.
Erfaring med kliniske forsøg med astmapatienter
FOSTERs sikkerhed blev evalueret i kliniske forsøg med det aktive lægemiddel sammenlignet med placebo, hvor 719 patienter på 12 år og ældre med astma af forskellig sværhedsgrad blev udsat for lægemidlet. Forekomsten af bivirkninger vist i nedenstående tabel refererer til astmapatienter i alderen 12 år og ældre og er baseret på sikkerhedsdata fra to pilotkliniske undersøgelser, hvor FOSTER blev administreret i de doser, der blev anbefalet i dette produktresumé. I en periode på 8 til 12 uger Der blev ikke observeret psykiatriske lidelser i kliniske studier med FOSTER, men disse blev ikke desto mindre rapporteret i tabellen som en potentiel klasseeffekt af inhalerede kortikosteroider.
Uønskede virkninger, der har været relateret til beclomethason -dipropionat og formoterol i fast kombination (FOSTER) er anført nedenfor, opført efter systemorganklasse. Frekvenser blev defineret som følger: meget almindelig (≥ 1/10), almindelig (≥ 1/100,
Blandt de observerede bivirkninger er de typisk forbundet med formoterol: tremor, hovedpine, takykardi, sinus bradykardi, angina pectoris, myokardiskæmi, forlængelse af QT -intervallet.
Blandt de observerede bivirkninger er de typisk forbundet med beclomethason -dipropionat: nasopharyngitis, oral candidiasis, dysfoni, halsirritation, irritabilitet, nedsat urinfrit cortisol, nedsat serumkortisol, forhøjede serumglukoseniveauer.
Yderligere bivirkninger, der ikke er observeret i klinisk erfaring med FOSTER, men typisk er forbundet med inhaleret beclomethason -dipropionat, omfatter andre orale svampeinfektioner og lungebetændelse Smagsændringer er lejlighedsvis blevet rapporteret under inhaleret kortikosteroidbehandling.
Se afsnit 4.4 vedrørende de foranstaltninger, der skal træffes for at minimere forekomsten af orale svampeinfektioner, oral candidiasis og dysfoni.
Systemiske virkninger af inhalerede kortikosteroider (f.eks. Beclomethason -dipropionat) kan især forekomme, når høje doser af lægemidlet gives over lange perioder og kan omfatte: Cushings syndrom, Cushingoid udseende, binyresuppression, nedsat knoglemineraltæthed, væksthæmning hos børn og unge, grå stær og glaukom (se også pkt.4.4).
Yderligere bivirkninger, der ikke er observeret i klinisk erfaring med FOSTER ved terapeutiske doser, men typisk forbundet med administration af beta2-agonister såsom formoterol, er hjertebanken, atrieflimren, ventrikulære ekstrasystoler, takyarytmi, potentielt alvorlig hypokaliæmi og forøgelse / fald i blodtryk Søvnløshed , svimmelhed, rastløshed og angst er lejlighedsvis blevet rapporteret under inhalationsterapi med formoterol Formoterol kan også forårsage muskelkramper, myalgi.
Overfølsomhedsreaktioner inklusive udslæt, nældefeber, kløe, erytem og ødem i øjne, ansigt, læber og hals (angioødem) er også blevet observeret.
Som med andre inhalationsterapier kan paradoksal bronkospasme forekomme med en øjeblikkelig stigning i hvæsen, hoste og dyspnø efter inhalation (se også pkt. 4.4).
Pædiatrisk population
Der er ingen tilgængelige oplysninger om sikkerheden ved Fostair hos børn op til 11 år, og der er kun begrænset information til unge i alderen 12 til 17 år. I et 12-ugers randomiseret klinisk forsøg med voksne og unge patienter modtog 162 unge i alderen 12 til 17 år med moderat til svær astma FOSTER eller den tilsvarende formulering under inhalationsopløsning under tryk i en dosis på 1 eller 2 inhalationer to gange dagligt; hyppighed, type og sværhedsgrad af bivirkninger forekom ikke anderledes hos unge end hos voksne.
Indberetning af formodede bivirkninger
Rapportering af formodede bivirkninger, der opstår efter godkendelse af lægemidlet, er vigtig, da det muliggør løbende overvågning af lægemidlets fordel / risiko -balance. Sundhedspersonale anmodes om at rapportere alle formodede bivirkninger via det nationale rapporteringssystem. "Adresse: www. .agenziafarmaco.gov.it/it/responsabili.
04.9 Overdosering -
Den højeste anbefalede dosis Fostair til en enkelt administration er 2 inhalationer. Fire kumulative inhalationer af FOSTER blev undersøgt hos astmatiske patienter (for i alt 400 mcg beclomethason-dipropionat og 24 mcg formoterol i en enkelt administration) Den kumulative behandling forårsagede ikke abnormiteter, klinisk relevante virkninger på vitale tegn, reaktioner alvorlige eller ikke-alvorlige bivirkninger (se også pkt.4.8).
Med hensyn til trykopløsningsformuleringen til inhalering er inhalationsdoser på op til tolv kumulative leverancer (for i alt 1200 mcg beclomethason -dipropionat og 72 mcg formoterol) undersøgt hos astmatiske patienter. Disse kumulative behandlinger forårsagede ikke abnormiteter på vitale tegn eller alvorlige eller ikke-alvorlige bivirkninger.
Overdrevne doser af formoterol kan resultere i virkninger, der er typiske for beta-2 adrenerge agonister: kvalme, opkastning, hovedpine, tremor, søvnighed, hjertebanken, takykardi, ventrikulær arytmi, QTc-intervalforlængelse, metabolisk acidose, hypokaliæmi, hyperglykæmi.
I tilfælde af overdosering af formoterol, er støttende og symptomatisk behandling indiceret. I alvorlige tilfælde er hospitalsindlæggelse påkrævet. Brug af kardioselektive betablokkere kan overvejes, men kun med ekstrem forsigtighed, da de kan forårsage bronkospasme. Kalium i serum bør overvåges.
Akutte inhalationer af beclomethasondipropionat ved højere doser end anbefalet kan resultere i midlertidig undertrykkelse af binyrefunktionen. I dette tilfælde er nødhjælp ikke nødvendige, da binyrefunktionen genoprettes på få dage, som det er blevet verificeret ved plasmakortisolmålingerne. Hos disse patienter bør behandlingen fortsættes med doser, der er tilstrækkelige til at kontrollere astma.
Kronisk overdosis af inhaleret beclomethason -dipropionat: risiko for adrenal suppression (se pkt. 4.4). Overvågning af binyrereserven kan være nødvendig. Behandlingen bør fortsættes med en tilstrækkelig dosis til at kontrollere astma.
Enkelt supraterapeutiske doser på op til 800 mcg beclomethason -dipropionat og 48 mcg formoterol administreret via FOSTER inhalationspulver var generelt sikre og veltolereret.
05.0 FARMAKOLOGISKE EGENSKABER -
05.1 "Farmakodynamiske egenskaber -
Farmakoterapeutisk klassifikation: Adrenergika, inhalationsmidler: formoterol og andre lægemidler mod obstruktive luftvejssygdomme.
ATC -kode: R03AK08.
Virkningsmekanismer og farmakodynamiske virkninger
FOSTER indeholder beclomethason-dipropionat og formoterol i en tør pulverformulering, som muliggør en ekstra fin aerosol med en massemedian aerodynamisk diameter (MMAD) i gennemsnit 1,4-1,5 mikron og co-deposition af de to komponenter. Aerosolpartiklerne i FOSTER er i gennemsnit meget mindre end partiklerne leveret i de ikke-ekstra fine formuleringer.
Et radiomærket lægemiddeldeponeringsundersøgelse udført hos astmatiske patienter viste, at en "høj del af lægemidlet (anslået til 42% af den nominelle dosis) deponeres i lungerne med homogen aflejring på tværs af luftvejene. Disse leveringsegenskaber understøtter" brug af et lavt dosis kortikosteroid med forbedrede lokale farmakodynamiske virkninger, som viste sig at være ækvivalent med den tilsvarende tryksatte inhalationsopløsning (se Klinisk erfaring).
De to aktive ingredienser i FOSTER har forskellige virkningsmåder: Som med andre kombinationer af inhalerede kortikosteroider og beta2-agonister observeres additive effekter i forhold til reduktion af astmaforværringer.
Beclomethason dipropionat
Beclomethasondipropionat administreret ved indånding, ved anbefalede doser, har antiinflammatorisk aktivitet typisk for glukokortikoider i lungen, med deraf følgende reduktion af symptomer og forværring af astma og mindre indtræden af bivirkninger sammenlignet med systemisk administration af kortikosteroider.
Formoterol
Formoterol er en selektiv beta-2-adrenerg agonist, der producerer afslapning af glatte bronkiale muskler hos patienter med reversible luftvejsobstruktioner. Bronchodilatatoreffekten sætter sig hurtigt ind inden for 1-3 minutter efter indånding og varer i 12 timer efter en enkelt dosis.
Klinisk erfaring
Effekten af de to komponenter i FOSTER inhalationspulver blev sammenlignet i tre forskellige undersøgelser, der sammenlignede formuleringen med 100 mcg / 6 mcg inhalationsopløsning under tryk til behandling af patienter med moderat til svær vedvarende astma. Samlet set i klinisk praksis en ækvivalent effekt af to inhalerede lægemidler forventes både ved dosis på 1 og 2 inhalationer to gange dagligt.
I en undersøgelse var det primære formål at vurdere effekten af den inhalerede kortikosteroidkomponent målt ved bronkodilatation (foruddosis FEV1). Klinisk signifikant forbedring af FEV1 før dosis fra baseline blev observeret hos 696 patienter med moderat til svær symptomatisk astma ved afslutningen af en 3-måneders behandlingsperiode, ved en dosis på 1 inhalation to gange dagligt og 2 inhalationer to gange om dagen med begge formuleringer. En gennemsnitlig stigning på mindst 250 ml blev observeret. Der var ingen klinisk relevant forskel i FEV1 før dosis mellem FOSTER inhalationspulver og inhalationsopløsning under tryk ved begge styrker. Et signifikant dosis-respons-forhold blev observeret for morgenens ekspiratoriske flow (PEF). Statistisk signifikans for dosis-respons-forholdet for FEV1 før dosis blev ikke nået. Målinger relateret til astmakontrol, såsom scoringer af astmasymptomer morgen og aften og procentdelen af symptomfrie dage, viste en signifikant forbedring fra baseline under og op til behandlingsperioden. Især for de to højeste doser af begge formuleringer .
I det andet studie var det primære mål at evaluere effekten af den langtidsvirkende beta2-agonistkomponent i FOSTER.I denne undersøgelse blev bronchodilation målt ved start og op til 12 timer efter enkeltdosisadministration. Gennem spirometriske serieevalueringer af FEV1 (AUC for FEV1 i forhold til mindst 80% af virkningsvarigheden af formoterol). En inhalation og fire inhalationer af begge formuleringer af FOSTER forbedrede signifikant FEV1 AUC0-12 sammenlignet med placebo Begge doser FOSTER inhalationspulver syntes at være ikke ringere end den tilsvarende dosis af den tryksatte inhalationsopløsning. Der blev fundet et forhold. Statistisk signifikant dosis respons mellem lav og høj dosis med begge formuleringer.
I den tredje undersøgelse, efter en 4-ugers forbehandlingsfase med den faste kombination beclomethason dipropionat / formoterol inhalationsopløsning under tryk på 1 inhalation to gange dagligt, blev 755 patienter med stabiliseret astma randomiseret til behandling i 8 uger med samme inhalator allerede i brug, med FOSTER inhalationspulver eller med beclomethason dipropionat 100 mcg inhalationspulver, alle administreret i en dosis på 1 inhalation to gange dagligt. Det primære formål var ændringen fra baseline og for varigheden af hele behandlingsperioden om morgenen Ekspiratorisk flow (PEF). Efter 8 ugers behandling var der ingen forskel i det primære endepunkt mellem de to kombinationsinhalatorer, som var signifikant bedre end beclomethason -dipropionat ved monoterapi. Der blev ikke fundet forskelle mellem de to kombinationsinhalatorer med hensyn til symptommåling, såsom scoren på astmakontrollespørgeskemaet og antallet af dage uden redningsmedicin.
Endelig blev der udført et åbent placebo-studie for at verificere, at det inspiratoriske flow, der kan genereres gennem Nexthaler-inhalatoren, ikke påvirkes af alder, patologier og sværhedsgrad af patientens patologi og derfor aktivering og levering af lægemidlet. via enheden kan være inden for rækkevidde for alle patienter. Det primære endepunkt var procentdelen af patienter i hver alder og sygdomsgruppe, der var i stand til at aktivere inhalatoren. 89 patienter i alderen 5 til 84 år, inklusive patienter med moderat til svær astma ( FEV1> 60% og ≤ 60% forudsagt henholdsvis) og patienter med moderat og svær KOL (FEV1 ≥ 50% og
I et yderligere åbent placebo-studie, som evaluerede den inspiratoriske strømningsprofil via inhalation af FOSTER, blev det vist, at patienter med mild til svær KOL effektivt kunne aktivere og bruge enheden uafhængigt af deres funktionelle begrænsning.
Pædiatrisk population
Det Europæiske Lægemiddelagentur har udsat forpligtelsen til at indsende resultaterne af astmaundersøgelser med FOSTER i undergrupper af den pædiatriske population i alderen 5 til 11 og 12 til 17 år.
I skrivende stund er der ingen klinisk erfaring med FOSTER hos børn i alderen 5 til 11 år, og der er kun begrænset information til unge i alderen 12 til 17 år.
I et 3-måneders randomiseret klinisk forsøg modtog 162 unge i alderen 12 til 17 år diagnosticeret med moderat til svær astma FOSTER eller den tilsvarende formulering under inhalationsopløsning under tryk i en dosis på 1 eller 2 inhalationer to gange dagligt. Ændringen i FEV1 før dosis ved behandlingens afslutning syntes større hos unge end hos voksne.
For information om pædiatrisk brug, se også afsnit 4.2 og 4.8.
05.2 "Farmakokinetiske egenskaber -
Beclomethason dipropionat
Beclomethasondipropionat er et prodrug med en svag bindingsaffinitet til glucocorticoidreceptoren, som hydrolyseres af esteraseenzymerne til den aktive metabolit beclomethason-17-monopropionat, som har en mere potent topisk antiinflammatorisk aktivitet end prodrug beclomethason dipropionat.
Absorption, distribution og metabolisme
Inhaleret beclomethason -dipropionat absorberes hurtigt gennem lungerne; før absorption omdannes den i vid udstrækning til dens aktive metabolit, beclomethason-17-monopropionat, af esteraseenzymer, der findes i flere væv.Den systemiske tilgængelighed af den aktive metabolit stammer fra lungerne og fra gastrointestinal absorption af den slugtede dosis. Biotilgængeligheden af slugt beclomethason-dipropionat er ubetydelig, men præ-systemisk omdannelse til beclomethason-17-monopropionat resulterer i, at en del af dosis absorberes som en aktiv metabolit.
Når den inhalerede dosis stiger, stiger systemisk eksponering cirka lineært.
Absolut biotilgængelighed efter inhalering fra en inhalator under dosering under tryk er henholdsvis ca. 2% og 62% af den nominelle dosis for umodificeret beclomethason-dipropionat og beclomethason-17-monopropionat.
Efter intravenøs administration er fordelingen af beclomethason-dipropionat og dets aktive metabolit kendetegnet ved høj plasmaclearance (henholdsvis 150 og 120 l / t) med et lille steady-state-distributionsvolumen for beclomethason-dipropionat (20 l) og en mere omfattende vævsfordeling for sin aktive metabolit (424 L.) Beclometason-dipropionat metaboliseres hovedsageligt (82%) til dets aktive metabolit, beclomethason-17-monopropionat.
Plasmaproteinbinding er moderat høj (87%).
Udskillelse
Fækal udskillelse er den vigtigste eliminationsvej for beclomethason -dipropionat, hovedsagelig som polære metabolitter.Renal udskillelse af beclometason -dipropionat og dets metabolitter er ubetydelig. De terminale eliminationshalveringstider er henholdsvis 0,5 timer og 2,7 timer for beclomethason-dipropionat og beclomethason-17-monopropionat.
Særlige populationer
Farmakokinetikken af beclomethason dipropionat hos patienter med nedsat nyre- eller leverfunktion er ikke undersøgt; da beclomethason-dipropionat imidlertid undergår hurtig metabolisme af esteraseenzymer, der er til stede i tarmvæske, serum, lunger og lever for at give anledning til de mere polære produkter beclomethason-21-monopropionat, beclomethason-17-monopropionat og beclomethason, farmakokinetikken og sikkerhedsprofilen for beclomethason dipropionat forventes ikke at blive påvirket af nedsat leverfunktion.
Da hverken beclomethason dipropionat eller dets metabolitter blev påvist i urinen, forventes der ikke en stigning i systemisk eksponering hos patienter med nedsat nyrefunktion.
Formoterol
Absorption og distribution
Efter indånding absorberes formoterol fra både lungerne og mave-tarmkanalen Fraktionen af den inhalerede dosis, der sluges efter administration med en præ-dispenseret inhalator (MDI) kan variere mellem 60% og 90%. Mindst 65% af sluges dosis absorberes fra mave-tarmkanalen. Den maksimale plasmakoncentration af det uændrede lægemiddel nås mellem 0,5 og 1 time efter oral administration Bindingen af formoterol til plasmaproteiner er 61-64% med 34% binding til albumin. Der er ingen bindingsmætning i koncentrationsværdierne opnået ved terapeutiske doser Den beregnede eliminationshalveringstid efter oral administration er 2-3 timer. Absorberingen af formoterol efter inhalation af doser på 12 til 96 mcg formoterolfumarat er lineær.
Metabolisme
Formoterol metaboliseres i vid udstrækning, hovedsageligt ved direkte konjugering af den phenoliske hydroxylgruppe. Konjugat med glucuronsyre er inaktiv. Den anden store rute involverer O-demethylering efterfulgt af konjugering af den phenoliske 2-hydroxylgruppe. Cytochrom P450 isoenzymerne CYP2D6, CYP2C19 og CYP2C9 er involveret i O-demethyleringen af formoterol. Leveren er den primære metaboliseringssted Formoterol hæmmer ikke CYP450 -enzymer ved terapeutisk relevante koncentrationer.
Udskillelse
Den kumulative urinudskillelse af formoterol efter en enkelt inhalation fra en tørpulverinhalator stiger lineært over dosisområdet fra 12 til 96 mcg. Gennemsnitligt udskilles 8% til 25% af dosis. Henholdsvis uændret formoterol og total formoterol. Baseret på plasmakoncentrationer målt efter inhalation af en enkelt dosis på 120 mikrogram til 12 raske forsøgspersoner, var den gennemsnitlige terminale eliminationshalveringstid 10 timer. Enantiomererne (RR) og (SS) repræsenterer henholdsvis ca. 40% og 60% af det uændrede lægemiddel, der udskilles i urinen. Det relative forhold mellem de to enantiomerer forbliver konstant ved de undersøgte doser, og der blev ikke observeret nogen relativ ophobning af en enantiomer. end den anden efter gentagen dosis.
Efter oral administration (40 til 80 mikrogram) hos raske forsøgspersoner blev 6% til 10% af dosis genoprettet i urinen som uændret lægemiddel; op til 8% af dosis blev genoprettet i form af glucuronid.
67% af den orale dosis af formoterol udskilles i urinen (hovedsageligt som metabolitter) og resten i fæces.Nyreclearance for formoterol er 150 ml / min.
Særlige patientpopulationer
Nedsat lever- / nyrefunktion: Formoterols farmakokinetik er ikke undersøgt hos patienter med nedsat lever- eller nyrefunktion.
Klinisk erfaring
Systemisk eksponering for beclomethason dipropionat og formoterol i kombination blev sammenlignet med eksponeringen for de enkelte komponenter Der var ingen tegn på farmakokinetisk eller farmakodynamisk (systemisk) interaktion mellem beclomethason dipropionat og formoterol.
Farmakokinetikken for FOSTER inhalationspulver blev sammenlignet med den for den tilsvarende tryksatte inhalationsopløsningsformulering. Steroidkomponentanalysen fokuserede på beclomethason-17-monopropionat, den største aktive metabolit af beclomethason-dipropionat.
Systemisk absorption og metabolisme af beclomethasondipropionat var hurtig, og Cmax blev nået inden for 5 minutter efter dosis for begge behandlinger, men var højere (+ 68%) med FOSTER inhalationspulver. L "AUCt viste sig cirka 3 gange højere efter inhalering af FOSTER via Nexthaler inhalator sammenlignet med inhalationsopløsningen under tryk. Cmax for beclomethason-17-monopropionat, den største aktive metabolit, som repræsenterer cirka 82% af det samlede blodniveau, blev opnået i gennemsnit efter 30 minutter og 15 minutter med Nexthaler og inhalation under tryk løsning, henholdsvis. Plasmakoncentrationen af beclomethason -17 -monopropionat var lavere (Cmax -49% og AUCt -29%) efter inhalation af inhalationspulveret sammenlignet med opløsningen under inhalation under tryk. Efter inhalation af FOSTER med Nexthaler inhalator blev topkoncentrationen (Cmax) for formoterol nået på 5 minutter og var højere (+ 47%) for inhalationspulveret, mens den samlede eksponering (AUCt) syntes at være sammenlignelig i de to behandlinger.
I et studie blev den relative lungefordeling evalueret ved hjælp af et aktivt kulfilter for at udelukke lægemiddelabsorption fra mave -tarmkanalen og ved at anvende en godkendt afstandsstykke, AeroChamber Plus, til referenceproduktet (inhalationsopløsningen under tryk). I denne sammenhæng viste Nexthaler inhalator og inhalationsopløsningen under tryk at være ækvivalente med hensyn til AUCt for både beclomethason-17-monopropionat og formoterol (forholdet mellem inhalationspulver / inhalationsopløsning under tryk og konfidensintervallerne på 90 % varierede fra 80 -125%); beclomethason-17-monopropionat Cmax var imidlertid lavere (-38%) efter administration fra Nexthaler-inhalatoren.
05.3 Prækliniske sikkerhedsdata -
Ikke-kliniske data for de enkelte komponenter i FOSTER afslører ingen særlig fare for mennesker baseret på konventionelle undersøgelser af sikkerhedsfarmakologi og toksicitet ved gentagne doser. Kombinationens toksicitetsprofil afspejler de enkelte komponenters, uden nogen stigning i toksicitet eller uventede hændelser.
Reproduktionsstudier på rotter har vist dosisafhængige virkninger. Tilstedeværelsen af beclomethason-dipropionat ved høje doser har været forbundet med nedsat fertilitet hos kvinder, reduceret antal implantater og embryoføtal toksicitet. Administration af høje doser kortikosteroider til drægtige dyr vides at forårsage abnormiteter i fosterudviklingen, herunder ganespalte og intrauterin væksthæmning, og det er sandsynligt, at virkningerne observeret med kombinationen beclomethason dipropionat / formoterol skyldes beclomethason dipropionat. findes kun ved høj systemisk eksponering for den aktive metabolit beclomethason-17-monopropionat (mere end 200 gange de forventede plasmaniveauer hos patienter). kan tilskrives de velkendte tokolytiske virkninger af beta2-sympatomimetika Disse virkninger blev noteret, når maternale plasmaformoterolniveauer var under dem, der forventes hos patienter behandlet med FOSTER.
Genotoksicitetsundersøgelser udført med kombinationen beclomethason dipropionat / formoterol indikerer ikke et mutagent potentiale Der er ikke udført kræftfremkaldende undersøgelser med den foreslåede kombination. Dyredata rapporteret for individuelle komponenter tyder imidlertid ikke på potentielle risici for kræftfremkaldende egenskaber hos mennesker.
06.0 LÆGEMIDDELOPLYSNINGER -
06.1 Hjælpestoffer -
Lactosemonohydrat (som indeholder små mængder mælkeprotein)
Magnesiumstearat.
06.2 Uforenelighed "-
Ikke relevant.
06.3 Gyldighedsperiode "-
3 år.
Efter første åbning af posen skal medicinen bruges inden for 6 måneder.
06.4 Særlige opbevaringsforhold -
Opbevares i den originale emballage for at beskytte mod fugt.
Fjern inhalatoren fra folieposen umiddelbart før første brug.
Inden du åbner konvolutten for første gang:
Dette lægemiddel kræver ingen særlige opbevaringstemperaturer.
Efter den første åbning af posen:
Må ikke opbevares over 25 ° C.
06.5 Den umiddelbare emballages art og emballagens indhold -
Hver æske indeholder 1, 2 eller 3 Nexthaler -inhalatorer, der indeholder 1,50 g inhalationspulver og tillader 120 pust hver. Hver inhalator er indeholdt i en varmeforseglet beskyttelsespose (aluminiumsemballage) i PET / Al / PE (Polyethylenterephthalat / Aluminium / Polyethylen) eller PA / Al / PE (Polyamid / Aluminium / Polyethylen).
Ikke alle pakningsstørrelser er nødvendigvis markedsført.
FOSTER er en multidosis inhalationsapparat. Enheden består af en ekstern krop udstyret med et vindue, der angiver antallet af doser tilbage og udstyret med en integreret hætte. Ved åbning af hætten, som også starter dosistællemekanismen, kan du se et mundstykke, gennem hvilket lægemidlet inhaleres. Enhedens ydre krop og mundstykket er lavet af acrylonitrilbutadienstyren, og hætten er lavet af polypropylen.
06.6 Brugsanvisning og håndtering -
Ubrugt medicin og affald fra denne medicin skal bortskaffes i overensstemmelse med lokale regler.
Nedenfor er instruktioner til brug af Nexthaler inhalator til gavn for sundhedspersonale.
INSTRUKTIONER TIL BRUG AF NEXTHALER -INHALATOREN
A. Pakkens indhold
Denne pakke indeholder:
• 1 instruktionsbog
• 1 Nexthaler inhalator inde i den varmeforseglede beskyttelsespose.
Hvis pakningens indhold ikke stemmer overens med ovenstående, skal du returnere inhalatoren til din leverandør og få en ny.
B. Generelle advarsler og forholdsregler
• Fjern ikke inhalatoren fra posen, hvis du ikke har til hensigt at bruge den med det samme.
• Brug kun inhalatoren som anvist.
• Hvis du ikke er sikker på, om dosistælleren er faldet en efter indånding, skal du vente til din næste planlagte dosis og tage den som normalt. Tag ikke en dobbelt dosis.
• Hold inhalatorhætten lukket, indtil du er klar til at tage din dosis.
• Når du ikke bruger inhalatoren, skal du opbevare den et rent og tørt sted.
• Forsøg ikke at tage din Nexthaler inhalator adskilt af en eller anden grund.
• Brug ikke Nexthaler inhalatoren:
eller efter udløbsdatoen
eller hvis der er gået mere end 6 måneder siden åbningen af konvolutten
eller hvis den er ødelagt
eller hvis dosistællervinduet viser "0"
eller hvis dosistælleren ikke kan læses.
I alle disse tilfælde skal inhalatoren bortskaffes korrekt eller returneres til leverandøren og en ny. Spørg din apotek om, hvordan du skal smide de inhalatorer, du ikke længere bruger.
C. Hovedtræk ved Nexthaler -inhalatoren
At tage en dosis fra din Nexthaler inhalator kræver kun tre enkle trin: Åben, indånder, lukker
D. Inden du bruger en ny Nexthaler inhalator
1. Åbn posen, og tag inhalatoren ud.
o Brug ikke inhalatoren, hvis posen er uforseglet eller beskadiget - returner den til leverandøren og få en ny.
2. Tjek din inhalator.
o Hvis din inhalator virker ødelagt eller beskadiget, skal du returnere den til din leverandør og få en ny.
3. Kontroller dosistællervinduet. Hvis inhalatoren er ny, vises tallet "120" i dosistællervinduet.
o Brug ikke en ny inhalator, hvis det viste tal er mindre end "120" - returner det til leverandøren og få en ny.
E. Sådan bruges Nexthaler inhalatoren
E.1. Visuel inspektion
1. Kontroller antallet af doser tilbage: ethvert tal mellem "1" og "120" angiver, at der stadig er doser tilbage.
o Hvis vinduet dosetæller viser "0", betyder det, at der ikke er flere doser tilbage - inhalatoren skal kasseres og en ny skal hentes.
2. Sørg for, at hætten er helt lukket, inden du bruger inhalatoren.
E.2. Åbning
1. Hold inhalatoren fast i en opretstående position.
2. Åbn emhætten helt.
3. Inhalér så meget som muligt.
o Undgå vejrtrækning gennem inhalatoren.
E.3. Indånding
Når det er muligt, skal du stå eller sidde oprejst under indånding.
1. Løft inhalatoren, før den til munden, og luk læberne omkring mundstykket.
o Dæk ikke luftindtag, mens du holder inhalatoren.
o Indånd ikke gennem luftindtaget.
2. Træk vejret hurtigt og dybt ind gennem munden.
o Du kan føle en vis smag i munden, mens du tager dosis.
o Du kan høre eller føle et 'klik', mens du tager din dosis.
o Du trækker ikke vejret gennem din næse.
o Bevæg ikke dine læber fra inhalatoren under indånding.
3. Fjern inhalatoren fra munden.
4. Hold vejret i 5 til 10 sekunder eller så længe du vil.
5. Træk vejret langsomt ud.
o Undgå vejrtrækning gennem inhalatoren.
E.4. Lukning
1. Sæt inhalatoren oprejst tilbage, og luk hætten helt.
2. Kontroller, at dosistælleren er faldet med et tal.
3. Hvis du skal tage en anden dosis, skal du gentage trin E.1 til E.4.
F. Rengøring
• Normalt er det ikke nødvendigt at rengøre inhalatoren.
• Hvis det er nødvendigt, kan du holde inhalatoren ren efter brug ved at tørre enheden af med en tør klud eller et køkkenrulle.
o Rengør ikke inhalatoren med vand eller andre væsker. Hold altid enheden tør.
G. Bevaring
• Når inhalatoren ikke bruges, skal enheden opbevares et rent og tørt sted. Du kan lægge den tilbage i posen efter brug.
o Udsæt ikke inhalatoren for varmekilder eller direkte sollys.
o Udsæt ikke inhalatoren for fugt eller våde omgivelser.
• Opbevares utilgængeligt for børn.
• Hvis der er gået mere end 6 måneder siden åbningen af posen, skal inhalatoren bortskaffes, og der skal anskaffes en ny enhed.
H. Bortskaffelse
• Bortskaf Nexthaler -inhalatoren, hvis tallet "0" vises i dosistællervinduet.
• Spørg din apotek om, hvordan du skal smide medicin, du er færdig med eller ikke længere bruger.
o Smid ikke medicin sammen med dit normale husholdningsaffald.
07.0 INDEHAVER AF "MARKEDSFØRINGSTILLADELSEN" -
CHIESI FARMACEUTICI S.p.A.
Via Palermo 26 / A
43122 Parma
Italien
08.0 MARKEDSFØRINGSTILLADELSESNUMMER -
037789031 FOSTER 100 mcg / 6 mcg inhalationspulver - 1 inhalator i ABS / PP på 120 doser
037789043 FOSTER 100 mcg / 6 mcg inhalationspulver - 2 inhalatorer i ABS / PP på 120 doser hver
037789056 FOSTER 100 mcg / 6 mcg inhalationspulver - 3 inhalatorer i ABS / PP på 120 doser hver
09.0 DATO FOR FØRSTE TILLADELSE ELLER FORNYELSE AF TILLADELSEN -
Juni 2013
10.0 DATO FOR REVISION AF TEKSTEN -
09/2016
11.0 FOR RADIOParma, FULDFØRTE DATA OM DEN INTERNE STRÅLINGSDOSIMETRI -
12.0 FOR RADIO -STOFFER, YDERLIGERE DETALJEREDE INSTRUKTIONER OM EKTEMPORÆR FORBEREDELSE OG KVALITETSKONTROL -











-cos-sintomi-cause-e-gravidanza.jpg)