Peptidbindingen er en kovalent binding, der etableres mellem to molekyler, når den ene carboxylgruppe reagerer med den andens aminogruppe gennem en kondensationsreaktion (eller dehydrering, som fører - det vil sige - til eliminering af et vandmolekyle) .
Normalt dannes peptidbindingen mellem to aminosyrer, hvilket resulterer i et dipeptid.
Da et dipeptid i dets molekyle stadig indeholder en amino- og en carboxygruppe, kan det danne en peptidbinding med en tredje aminosyre, hvilket giver anledning til et tripeptid og så videre. Når antallet af aminosyrer er relativt lille, kaldes det oligopeptid, mens hvis antallet af aminosyrer stiger, kaldes det polypeptid eller protein.

I virkeligheden er peptidbindingen på trods af figuren ikke af den simple type, men har en 60% enkeltbindingskarakter og 40% en dobbeltbindingskarakter.
I levende organismer katalyseres dannelsen af peptidbindingen af et enzym - kaldet peptidyltransferase - til stede i den store underenhed af ribosomer.
Proteinerne, der indføres i kosten, består også af aminosyrekæder, der er forbundet med peptidbindinger. Under fordøjelsen brydes disse bindinger af bestemte enzymer (peptidaser), der er til stede i maven og bugspytkirtlen. De enkelte aminosyrer, når de først er absorberet af tarmen, passerer fra blodet og opsamles af cellerne - især leveren - som forener dem gennem nye peptidbindinger for at danne de proteiner, de har brug for (ikke kun strukturelle, men også hormonelle, enzymatiske osv. Faktisk er der i naturen et stort antal proteiner med forskellige fysisk -kemiske egenskaber, som stammer fra de forskellige egenskaber ved de 20 almindelige aminosyrer og fra, hvordan de kombineres i polypeptidkæden. Tænk bare på, at et protein på 100 aminosyrer, derfor relativt små, kan den bestå af 20100 = 1,27 x 10130 mulige polypeptidkæder.Instruktionerne til opbygning af den korrekte aminosyrekæde er indeholdt i individets genom.




.jpg)

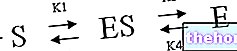















.jpg)