Almindelighed
Cyanid er det kemiske udtryk, der identificerer enhver kemisk forbindelse, der indeholder cyanogruppen (CN).
Cyangruppen er et molekyle dannet ved forening af et carbonatom og et nitrogenatom.

Eksempler på uorganisk cyanid er hydrogencyanid, natriumcyanid, kaliumcyanid og cyanogenchlorid.
Eksempler på organisk cyanid er på den anden side nitriler, der er indeholdt i kernerne af forskellige frugter (abrikoser, fersken, kirsebær osv.).
Cyanider er kemikalier, der er meget udbredt i fremstillingen, fra papirindustrien til metallurgi, plast osv.
Hvad er cyanid?
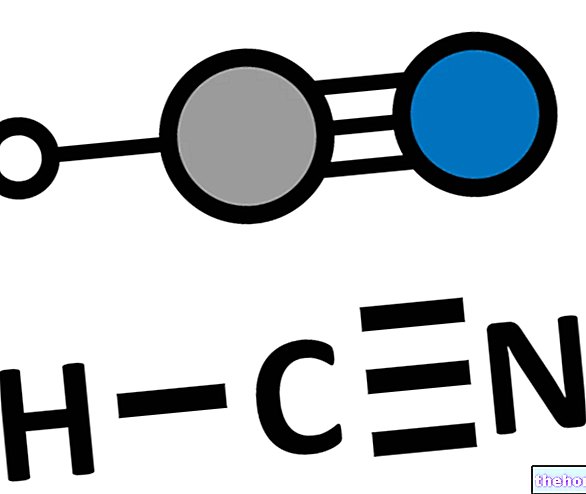
Et cyanid er en hvilken som helst kemisk forbindelse, der indeholder cyanogruppen (CN).
Cyanogruppen er resultatet af foreningen af et carbonatom (C i CN) til et nitrogenatom (N i CN). Bindingen, der forener kulstof til nitrogen, er en tredobbelt kovalent binding. Den totale ladning, der er til stede på CN -gruppen, er negativ, derfor er cyanogruppen en anion.
CYANIDE SOM GIFT: UORGANISK CYANID
I den almindelige fantasi refererer udtrykket cyanid til en kraftig gift med dødelige virkninger.
Kemisk set er de cyanider, der virker som potente giftstoffer, uorganiske cyanider, såsom natriumcyanid (NaCN), kaliumcyanid (KCN) og cyanogenchlorid (ClCN).
HVOR KOMMER UORGANISK CYANID FRA?
Enhver form for uorganisk cyanid stammer fra dissocieringen af hydrogencyanid (HCN eller hydrogencyanid) eller et af dets salt (som igen kan være et cyanid).
Hydrogencyanid er et uorganisk molekyle, resultatet af foreningen af en cyanogruppe (CN) med et hydrogenatom (H). Det er en meget giftig svag syre og kan betragtes som et særligt eksempel på uorganisk cyanid.
Bemærk venligst: natriumcyanid og kaliumcyanid er to salte af hydrogencyanid.
Cyanogenchlorid er derimod et derivat af et salt af hydrogencyanid; for at være præcis er det et derivat af natriumcyanid. Oxidationen af natriumcyanid med chlor danner cyanogenchlorid.
ØKOLOGISK CYANID
I naturen danner cyano -anionen CN også kemiske forbindelser med organiske molekyler (f.eks. Methylgrupper osv.), Hvilket giver anledning til typer af organisk cyanid.
Også kendt som nitriler, organiske cyanider er let giftige eller bliver kun giftige ved bestemte lejligheder; de er imidlertid mindre og mindre giftige end uorganiske cyanider.

Ejendom
Cyanids egenskaber afhænger af, hvilke atomer der er bundet til CN -cyanogruppen.
Hydrocyansyre er en lyseblå eller farveløs væske ved stuetemperatur, mens den er en farveløs gas ved høje temperaturer. Både i flydende og i gasform har den en lugt, der ligner den af bitre mandler.
Natriumcyanid og kaliumcyanid fremstår som hvide pulvere og afgiver - ligesom hydrogencyanid - en lugt, der kan sammenlignes med bitter mandler.
Cyanogenchlorid er en farveløs flydende gas, tungere end luft og med en særlig skarp lugt.
Hvor er det?
I naturen såvel som i kernerne af nogle frugter er cyanid også til stede i forskellige plantearter; planter holder det i bladene og / eller i barken og bruger det til at forsvare sig mod planteædere.
Ud over planter er andre levende ting, der producerer cyanid (eller stoffer, der indeholder CN -cyanogruppen) nogle bakterier og nogle svampe.
CYANIDE SOM FORBRÆDNINGSPRODUKT
Hydrogencyanid er et muligt produkt af forbrændingsprocesser.
For at være præcis er den til stede i udstødningen af forbrændingsmotorer, i cigaretrøg, der dannes under forbrændingen af sidstnævnte og i dampe, der stammer fra sammensmeltning af plastmaterialer baseret på acrylonitril (en organisk forbindelse, der indeholder en cyano gruppe CN).
Anvendelser
Ved fremstilling bruges cyanid meget. Faktisk papirindustrien (til fremstilling af papir), tekstilindustrien (til fremstilling af tekstiler osv.), Industrien til fremstilling af plast, den fotografiske industri (til at producere alle de kemiske forbindelser til udvikling af fotos), metalindustrien (til fremstilling af stål og jern, til vask af metaller og til galvanisering), industrien, der beskæftiger sig med behandling af spildevand og industrien til produktion af pesticider (mod parasitter osv.) til forskellige typer miljøer.
Af indlysende årsager kan der findes spor af cyanid i affaldsprodukterne fra alle de førnævnte aktiviteter.
SIDSTE BRUG
Tidligere fandt hydrogencyanid brug til tragiske formål.
For eksempel under anden verdenskrig brugte Nazi -Tyskland det - under navnet Zyklon B - som et giftigt middel i gaskamrene i dødslejrene.
Spredning
Cyanid har evnen til at sprede sig i vand, jord og luft (N.B: i luften er det i form af gas).
Mennesker kan komme i kontakt med cyanid ved at trække vejret forurenet luft, drikke forurenet vand, spise forurenet mad eller røre ved forurenet jord.
En "daglig" cyanidkilde - som mange mennesker udsættes for - er cigaretrøg.
Effekter
Efter eksponering tager det lidt tid for cyanid at komme ind i blodbanen og spredes gennem kroppen via blodet.
Menneskekroppen reagerer på tilstedeværelsen af cyanid på forskellige måder, afhængigt af om doserne er meget lave eller mellemhøje.
Når doser er meget lave, cyanid omdanner gennem en række cellulære reaktioner til thiocyanat, en kemisk forbindelse, der er uskadelig for helbredet, og som mennesket eliminerer gennem urinen. Desuden kombineres cyanid altid med lave doser med vitamin B12 og det resulterende binomiale synes at har gavnlige virkninger på både nerveceller og blodlegemer.
Når derimod doser er mellemstore til høje, den menneskelige organisms evne til at omdanne cyanid til thiocyanat undertrykkes (på grund af en overdreven arbejdsbyrde), og det pågældende giftige stof forhindrer cellerne i at bruge iltet. "ilt fører til cellernes død.
Hjertet, luftvejene og centralnervesystemet påvirkes mest af en stor eksponering for cyanid.
Bemærk venligst: For at undgå tvivl skal det bemærkes, at kronisk udsættelse for meget små doser cyanid kan have toksiske virkninger svarende til dem, der fremkaldes ved udsættelse for mellemhøje doser.
Toksicitet
Cyanids toksiske virkninger på menneskers sundhed afhænger af tre faktorer: Dosen af giftigt stof, som man er kommet i kontakt med, eksponeringens varighed og typen af cyanid.
Eksponering for mellemdoser af cyanid involverer typisk:
- Acceleration af vejrtrækning;
- Følelse af rastløshed;
- Svimmelhed
- Følelse af svaghed;
- Hovedpine
- Kvalme og opkastning
- Acceleration af hjerteslag.
Hvis cyaniddoserne er høje, er de førnævnte manifestationer forbundet med:
- Kramper;
- Hypotension;
- Nedsat hjerterytme
- Tab af bevidsthed;
- Åndenød og vejrtrækningsbesvær på grund af lungeproblemer
- Hjertestop.
Virkningerne af eksponering for cyanid begynder at vise sig efter bare et par sekunder / minutter.Dosen påvirker hovedsageligt hastigheden af virkningen.
Normalt opstår dødsfald på grund af cyanideksponering som følge af alvorligt respirationssvigt eller hjertestop.
LANGTidsvirkninger
Ifølge flere kliniske undersøgelser ville mennesker, der overlever "massiv cyanideksponering, have en tendens til at udvikle permanente neurologiske problemer, hvoraf nogle efterligner symptomer meget ligner dem ved Parkinsons sygdom."
LETHAL DOSE
Når doser cyanid er dødelige, taler eksperter om "død som følge af cyanidforgiftning".
For natriumcyanid og kaliumcyanid er den dødelige dosis for mennesker 200-300 mg; for hydrogencyanid er den dødelige dosis for mennesker på den anden side 50 mg.
Terapi
Eksponering for giftige doser cyanid repræsenterer en medicinsk nødsituation, der skal behandles meget hurtigt og på den mest hensigtsmæssige måde.
Generelt er de allerførste terapeutiske indikationer:
- Flyt dig væk så hurtigt som muligt fra eksponeringsstedet / miljøet, og flyt til et uforurenet sted;
- Tag dit tøj af, hvis det er forurenet, og læg det tilbage i en plastikpose;
- Vask dine øjne hvert 10-15 minut, hvis de brænder;
- Vask enhver del af huden, der er kommet i kontakt med cyanidet med sæbe og vand;
- Ring efter lægehjælp.
Når der kommer lægehjælp, vil de afslutte behandlingen og levere ilt til den pågældende person og en modgift.
Modgiftene mod udsættelse for store doser cyanid er natriumthiosulfat, natriumnitrit og hydroxocobalamin.