Introduktion
Blodplader eller trombocytter er de mindste figurerede elementer i blodet, med en diskot form og en diameter mellem 2 og 3 µm. I modsætning til hvide blodlegemer (eller leukocytter) og røde blodlegemer (eller erytrocytter) er blodplader ikke egentlige celler, men cytoplasma -fragmenter af megakaryocytter placeret i den røde marv. Disse stammer til gengæld fra forstadier kaldet megakaryoblaster og fremstår som store flerkernede celler (diameter fra 20 til 15 nm), som efter forskellige modningstrin undergår fænomener af cytoplasmatisk fragmentering, der stammer fra 2000 til 4000 blodplader. Følgelig er trombocytter blottet for kerne (som røde blodlegemer) og strukturer såsom det endoplasmatiske nethinde og Golgi -apparatet; de er imidlertid afgrænset af en membran, som gør hver blodplade uafhængig af de andre og besidder granulater, forskellige organeller cytoplasmatisk og RNA.
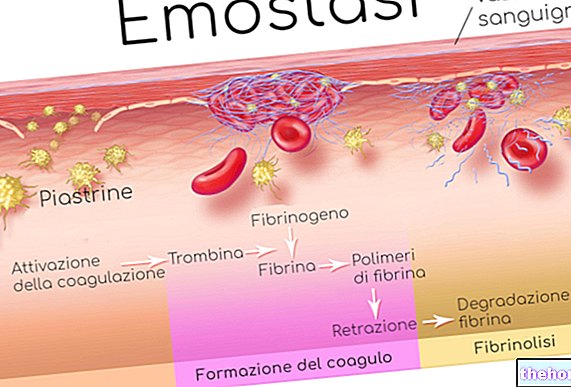
Som forventet er blodpladernes dimensioner særligt små; trods dette er deres indre struktur ekstremt kompleks, da de griber ind i en biologisk proces af primær betydning kaldet hæmostase [haima, blod + stasis blok]. I synergi med koagulationsenzymerne tillader blodpladerne passage af blod fra væsken til fast tilstand og danner en slags prop (eller trombe), der blokerer de skadede punkter i karrene.
Normale værdier i blodet
150.000 til 400.000 blodplader er normalt til stede i en milliliter blod. Deres gennemsnitlige levetid er 10 dage (sammenlignet med 120 for røde blodlegemer), i slutningen af disse fagocytiseres eller ødelægges af makrofager, især i lever og milt (i sidstnævnte er der cirka en tredjedel af den samlede trombocyttmasse) . Hver dag produceres fra 30.000 til 40.000 blodplader pr. Mm3, om nødvendigt kan denne syntese øges 8 gange.
Trombocytstruktur
Blodpladernes struktur er ekstremt kompleks, så de kun aktiveres som reaktion på præcise og velbestemte stimuli; hvis dette ikke var tilfældet, ville blodpladeaggregering under omstændigheder, der ikke er strengt nødvendige, eller en defekt på tidspunktet for behov, have meget alvorlige konsekvenser for organismen (patologisk trombogenese og blødninger).
Da forkert blodkoagulation spiller en primær rolle i dannelsen af slagtilfælde og hjerteanfald, er de biologiske mekanismer, der styrer det, stadig genstand for talrige undersøgelser.
Blodplader er altid til stede i kredsløbet, men aktiveres kun, når der er skader på kredsløbets vægge.
Blodpladernes struktur, såvel som deres form og volumen, ændrer sig dybt i forhold til graden og aktivitetsstadiet. I den inaktive form består blodplader af en lysere del (hyalomer) og en mere brydende central del (kromomer), rig på granulater indeholdende koagulationsproteiner og cytokiner. Cellemembranen er rig på proteinmolekyler og glycoproteiner, der fungerer som receptorer ved at regulere blodpladens interaktion med det omgivende miljø (adhæsion og aggregering).
Koagulation og blodplader
Blodplader er blot nogle af de mange aktører, der er involveret i koagulationsprocessen. Efter skader på et blodkar, frigivelse af nogle kemiske stoffer af endotelcellerne og eksponering af kollagen i den beskadigede væg, bestemmer aktiveringen af blodplader (endotelet er et særligt foringsvæv på den indre overflade af blodkar , som under normale forhold adskiller kollagenmatrixfibrene fra blodet, hvilket forhindrer vedhæftning af blodplader).
Blodplader klæber hurtigt til kollagen udsat for den beskadigede væg (trombocytadhæsion) og aktiveres ved at frigive bestemte stoffer (kaldet cytokiner) til læsionsområdet. Disse faktorer fremmer aktivering og sammenslutning af andre blodplader, som aggregerer for at danne en skrøbelig prop, såkaldt hvid trombe; desuden hjælper de med at forstærke den lokale vasokonstriktion, der tidligere blev udløst af nogle parakrinstoffer, frigivet af det skadede endotel med det formål at reducere blodgennemstrømning og tryk. Begge reaktioner medieres af frigivelse af stoffer indeholdt i nogle trombocytgranuler, såsom serotonin, calcium, ADP og trombocytaktiverende faktor (PAF). Sidstnævnte udløser en signalvej, der omdanner fosfolipiderne i trombocytmembranen til thromboxan A2, som har en vasokonstriktiv handling og fremmer blodpladeaggregering.
Blodplader er ekstremt skrøbelige: få sekunder efter skaden på et fartøj aggregeres og brydes de, frigiver indholdet af deres granulat i det omgivende blod og favoriserer dannelsen af en blodprop.
"Aggregeringen af trombocytter skal" naturligvis være begrænset for at forhindre, at blodpladestikket strækker sig ind i områder, der ikke er påvirket af endotelskader; trombocytadhæsion til raske karvægge er således begrænset af frigivelse af NO og prostacyclin (et eicosanoid).
Det primære blodpladestik konsolideres i den næste fase, hvor en række reaktioner hurtigt følger hinanden

Mens på den ene side prostacyclin frigivet af cellerne i det sunde endotel hæmmer vedhæftning af blodplader, på den anden side syntetiserer vores krop antikoagulantia - såsom heparin, antithrombin III og protein C - for at blokere og regulere nogle af de involverede reaktioner. koagulationskaskade, som nødvendigvis skal begrænses til det skadede område.
Vaskulær fase → reduktion af det vaskulære lumen
Sammentrækning af den vaskulære muskulatur
Perifer vasokonstriktion
Trombocytfase → dannelse af trombocytproppen
Medlemskab
Formændring
Degranulering
Aggregering
Koagulationsfase → dannelse af fibrinkoagel:
Kaskade af enzymatiske reaktioner
Fibrinolytisk fase → opløsning af blodproppen:
Aktivering af det fibrinolytiske system
Blodplader spiller en væsentlig rolle i at "stoppe" blødningen, men de griber ikke direkte ind i reparationen af det beskadigede kar, hvilket i stedet skyldes processer med cellevækst og deling (fibroblaster og vaskulære glatte muskelceller). Når lækagen er repareret, opløses blodproppen langsomt og trækker sig tilbage ved virkningen af enzymet plasmin, der er fanget inde i blodproppen.
Pistrine og blodprøver
- PLT: trombocyttal, antal blodplader pr. Blodvolumen
- MPV: middel trombocytvolumen
- PDW: fordelingsbredde for trombocytvolumener (indeks for trombocytanisocytose)
- PCT: eller trombocythæmatokrit, blodvolumen optaget af pistrinerne